 |
Применение ферментов в пищевых технологиях
|
|
|
|
Введение
С деятельностью ферментов человечество знакомо очень хорошо с глубокой древности, хотя и не догадывалось об этом. Испокон веков люди знали способы приготовления хлеба, вина, пива, сыра, различных соусов, в которых основную роль играют процессы брожения, т.е. процессы, вызываемые микроорганизмами и выделяемыми ими ферментами.
Промышленное производство ферментных препаратов началось около 100 лет назад. Изначально оно было основано на извлечении ферментов из сырья растительного и животного происхождения, а затем для этого начали активно применять микроорганизмы.
В настоящее время развитие биотехнологии, научные открытия в области энзимологии сделали ферментные препараты незаменимым участником многих пищевых технологий. Использование ферментов позволяет повышать скорость технологических процессов, ощутимо увеличивать выход готовой продукции, улучшать ее качество, экономить ценное сырье и снижать количество отходов.
Для получения ферментных препаратов пищевого назначения используются органы и ткани сельскохозяйственных животных, культурные растения, специальные штаммы микроорганизмов (плесневых грибов, бактерий).
Понятие о ферментах, их виды
Ферменты являются биологическими катализаторами белковой природы. Ферменты способны значительно (в десятки тысяч раз) повышать скорость различных реакций, в том числе и биохимических, которые непрерывно протекают в живых организмах, которые наблюдаются в ходе технологических процессов переработки сырья.
Ферменты обладают специфичностью действия, то есть действуют на определенный субстрат, тип связи. Ферменты характеризуются также высокой лабильностью, то есть, подвержены влиянию внешних факторов, таких как температура, концентрация субстрата, рН среды, присутствие активаторов или ингибиторов. Во многом лабильность ферментов связана с их белковой природой, сложной пространственной конфигурацией.
|
|
|
Ферменты повышают скорость реакций за счет значительного снижения энергетического уровня проведения реакции. Ферментативная реакция проходит в две стадии.
На первой стадии происходит образование фермент-субстратного комплекса, образованию которого соответствует значительно низкая энергия активации.
На второй стадии комплекс распадается на продукты реакции и свободный фермент, который может взаимодействовать с новой молекулой субстрата. Это выражается уравнением:
Е + S ↔ ЕS → Р + Е, где: Е- фермент, S- субстрат, ЕS- фермент-субстратный комплекс, Р продукты реакции.
Ферменты, как уже отмечалось, имеют белковую природу и обладают третичной и четвертичной структурой. Многие ферменты являются двухкомпонентными, то есть имеют белковую часть в виде апофермента и небелковую составляющую в виде кофермента.
В качестве кофермента могут выступать витамины, ароматические и алифатические углеводороды, гетероциклические соединения, нуклеотиды и нуклеозиды. Ферменты имеют некоторые специфические свойства, наиболее важные из них:
v высокая каталитическая активность (повышают скорость реакций в миллионы раз);
v специфичность действия (фермент катализирует превращение одного субстрата, реже группу родственных субстратов);
v лабильность (изменение активности под действием различных факторов: рН, температура, присутствие активаторов и ингибиторов, что связано с белковой природой и сложной пространственной конфигурацией фермента).
Все ферменты делятся на шесть классов по типу катализируемой реакции:
1 класс оксидоредуктазы – ферменты, катализирующие окислительно-восстановительные реакции (присоединение кислорода, отнятие и перенос водорода, перенос электронов);
|
|
|
2 класс трансферазы – ферменты, катализирующие перенос атомных группировок от одного соединения к другому (остатков моносахаридов, аминокислот, фосфорной кислоты, метильные группировки и т.д.);
3 класс гидролазы – ферменты, катализирующие реакции гидролиза сложных органических соединений на более простые. Реакции гидролиза проходят с участием воды.
4 класс лиазы – ферменты, катализирующие реакции негидролитического отщепления каких-либо групп от субстрата с образованием кратной связи или присоединение группировок по месту разрыва кратных связей (отщепление воды, углекислого газа, аммиака);
5 класс изомеразы – ферменты, катализирующие реакции изомеризации или образование изомерных форм молекул органических веществ в результате переноса химических группировок внутри молекулы (переход глюкозы во фруктозу);
6 класс – лигазы или синтетазы – ферменты, катализирующие реакции синтеза, сопряженные с разрывом одних связей и образованием других (С-С, С-S, С-N, С-О связей).
При переработке пищевого сырья чаще всего приходится иметь дело с ферментами 1 класса – оксидоредуктазами, такими как каталаза, полифенолоксидаза; с ферментами 3 класса – гидролазами, такими как амилазы – ферменты гидролизующие крахмал, протеиназы – ферменты, гидролизующие белок, липазы – ферменты гидролизующие липиды.
В пищевой промышленности широко применяются ферментные препараты, полученные биохимическим путем при выращивании специфических микроорганизмов, способных вырабатывать определенные ферменты.
Различают бактериальные ферментные препараты, полученные путем глубинного культивирования бактерий, и поверхностные, полученные путем поверхностного культивирования плесневых грибов.
Применение ферментов в пищевых технологиях
В процессах хранения сырья, его переработки в продукты питания и при хранении готовых продуктов происходят многочисленные изменения, связанные с действием различных ферментов. Чаще всего эти изменения связаны с действием окислительных ферментов класса оксидоредуктаз и гидролитических ферментов класса гидролаз.
|
|
|
В пищевой промышленности находят все более широкое применение ферментные препараты, полученные биохимическим синтезом с использованием различных бактерий и плесневых грибов (рис.1,2,3.). Применение ферментных препаратов позволяет интенсифицировать технологические процессы, улучшать качество готовой продукции, увеличивать ее выход, экономить исходное сырье.
Название ферментного препарата включает название основного фермента, название микроорганизма-продуцента, с окончанием «-ин». Далее отражается способ культивирования микроорганизма: Г – глубинное культивирование для бактерий и П – поверхностное для плесневых грибов, а также степень очистки – Х- неочищенный фермент, 2Х, 3Х, 10Х, 15Х,20Х. Чем больше число, тем выше степень очистки. В последние годы большое внимание уделяется степени очистке, при этом удаляются балластные вещества, повышается активность ферментов, а, следовательно, снижается норма внесения высокоочищенных ферментных препаратов.
В производстве пива широко применяются ферменты в процессе приготовления пивного сусла, для борьбы с помутнениями пива и т.д.

Рис.1. Ферменты в пищевой промышленности

Рис.2. Ферменты в пищевой промышленности

Рис.3. Типы ферментов в пищевой промышленности

Рис.4 Применение ферментов в пищевых технологиях

Рис.5 Применение ферментов в пищевых технологиях

Рис.6 Применение ферментов в пищевых технологиях
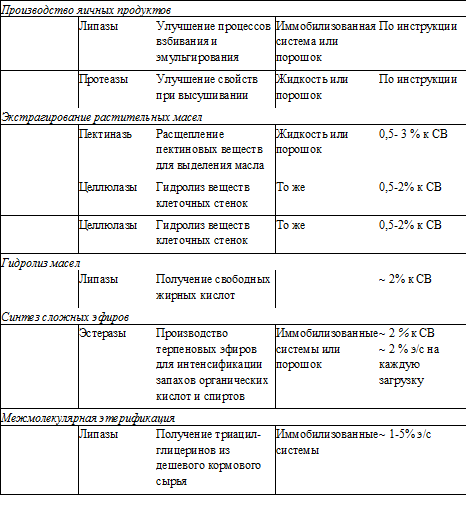
Рис.7 Применение ферментов в пищевых технологиях
Заключение
Ферментные препараты представляют собой очищенные и концентрированные продукты, содержащие определенные ферменты (энзимы) или комплекс ферментов, характерных для биологических сред и организмов — продуцентов. Они являются важным элементом в технологиях пищевых продуктов и применяются для интенсификации технологических процессов и повышения качества продуктов питания.
Ферменты высокого качества позволяют улучшить технологию, сократить затраты и даже получить новые продукты. Это один из наиболее эффективных и перспективных способов ускорения технологических процессов.
|
|
|
В соответствии с международной номенклатурой и типами катализируемых ими реакций энзимы делятся на шесть основных групп:
v оксидоредуктазы — класс ферментов, катализирующих окислительно-восстановительные реакции;
v трансферазы — ферменты, переносящие различные химические группировки;
v гидролазы — ферменты, катализирующие реакции расщепления внутримолекулярных связей, протекающие с присоединением воды в точке расщепления;
v лиазы — ферменты, удаляющие радикалы негидролитическим путем с образованием двойных связей;
v изомеразы — класс ферментов, катализирующих взаимные превращения изомеров;
v лигазы — ферменты, катализирующие присоединение друг к другу двух молекул при расщеплении пирофосфатной связи в АТФ или подобного вещества.
При выборе ферментов для пищевых производств необходимо учитывать:
v источник, форму и наличие разрешения на их использование;
v доступность качественного продукта;
v удобство в использовании (предпочтительны иммобилизованные или растворимые ферменты);
v стоимость за единицу активности фермента.
Применение ферментных препаратов в пищевой промышленности позволяет интенсифицировать технологические процессы, улучшать качество готовой продукции, увеличивать ее выход, экономить ценное пищевое сырье.
Cписок использованной литературы:
1. Авдеева, Л.В. Биохимия: Учебник / Л.В. Авдеева, Т.Л. Алейникова, Л.Е. Андрианова. - М.: ГЭОТАР-МЕД, 2013. - 768 c.
2. Крахмалева, Т.М. Пищевая химия: учеб. пособие / Т. М. Крахмалева, Э. Ш. Манеева.- Оренбург: Университет, 2012. - 155 с.
3. Нечаев, А.П. Технологии пищевых производств / под общ. ред. А.П. Нечаева. – М.: КолосС, 2007. – 767 с.
4. Материалы, опубликованные на сайте: http://www.biochemistry.ru/
|
|
|


