 |
Контрольные вопросы. Лекция 10. План лекции
|
|
|
|
Контрольные вопросы
1. Общая характеристика сырья для биотехнологических производств.
2. Приготовление и стерилизация питательных сред.
3. Основные требования и ограничения к сырью.
4. Основные компоненты питательной среды.
5. Периодическая или циклическая стерилизация.
6. Непрерывная стерилизация
7. Принципы конструирования питательных сред
8. Основные виды сырья и их сравнительная характеристика
Лекция 10
Основные технологические стадии биотехнологического процесса
Форма проведения лекции: лекция-консультация
План лекции
1. Приготовление посевного материала.
2. Культивирование микроорганизмов.
3. Кривая роста микроорганизмов.
1. В технологическом процессе используются полезные свойства штамма, следовательно, необходимо сохранять и, если возможно, улучшать его производственные качества. Поэтому в биотехнологическом производстве имеется отделение чистой культуры, в задачей которого является постоянное и надежное воспроизведение полезных свойств продуцента, найденных или достигнутых в свое время в ходе лабораторных исследований. Такое отделение проводит лабораторные операции по контролю и сохранению чистой культуры, а также маломасштабное культивирование для постоянной передачи штамма на стадию ферментации.
Фактически это микробиологическая лаборатория, с музеем штаммов-продуцентов. В ходе контрольных высевов и маломасштабных ферментаций (в пробирках, колбах и т. д. ) контролируется устойчивость всех имевшихся или приобретенных признаков, послуживших основанием для рекомендации к промышленному применению этих культур. По мере необходимости из отделения чистой культуры поступает заданная масса инокулята, идущая в производство.
|
|
|
При периодическом процессе культивирования (при производстве метаболитов) в отделении чистой культуры готовят засевную дозу клеток для каждой из операций основного производства. При непрерывном производстве кормового белка этого не требуется, однако для повышения качества продукта предпочитают время от времени вводить клетки штамма-продуцента из отделения чистой культуры. Для этого в отделении имеется ферментационная часть, где производится выращивание достаточно крупных партий микроорганизма продуцента.
Посевные дозы выращиваются последовательно в колбах и бутылях на 10-20 литров, находящихся на качалках или просто в термостатируемом помещении, и далее в последовательности ферментеров объемом (по необходимости) 10, 100, 500 и 1000 литров, в которых осуществляется перемешивание, аэрация и термостатирование культуральной жидкости с клетками.
Отделение чистой культуры должно иметь достаточно большую коллекцию штаммов продуцентов, так как возможны временные переходы с одного штамма на другой, вызванные различными причинами. Например, сезонные изменения температуры частично компенсируются подбором достаточно продуктивных термотолерантных штаммов. Кроме того, микробиологическая промышленность зачастую вынуждена использовать в качестве компонентов питательных сред отходы сельского хозяйства и пищевой промышленности (меласса, кукурузный экстракт), что ведет к сезонным изменениям сырья и предполагает адаптацию продуцента к особенностям среды. Все это делает роль микробиологической службы производства достаточно высокой.
2. Основным методом биотехнологии является культивирование, то есть выращивание микроорганизмов в специально созданных условиях.
Культивирование бывает: поверхностное, глубинное.
|
|
|
Поверхностное культивирование ведут в специальных растительных камерах, глубинное культивирование проводят в ферментерах (это аппарат, который заполнен жидкой питательной средой).
По способу организации, культивирование бывает: периодическое, непрерывное.
Также культивирование бывает: аэробным и анаэробным.
Из множества существующих организмов в промышленности используются только чистые культуры, часто селекционированные или получаемые методом генной инженерии, их называют продуцентами. Они дают нужный продукт в максимальном количестве.
Микроорганизмы должны расти на дешёвых и доступных питательных средах. Конверсия питательной среды в биомассу или в нужный продукт должна быть максимальной. Выражается это понятие экономическим коэффициентом:
(1)
где ∆ x- количество выросшей биомассы,
∆ s-количество потреблённой питательной среды
Микроорганизмы должны расти с максимально- высокой скоростью роста:
(2)
где ∆ τ - скорость роста.
(3)
где μ - удельная скорость роста.
Культивирование клеток в жидкой среде осуществляется несколькими способами. Наиболее простым и распространенным является накопительное или периодическое культивирование. Клетки растут в постоянном объеме питательной среды на установках качального или роллерного типа. Такая система закрыта для всего, кроме газов и летучих продуктов метаболизма. Оказывается при этом в колбах накапливается значительное количество углекислого газа. После замедления роста суспензия разводится до начальной плотности, и цикл выращивания повторяется. Цикл выращивания - это период от помещения инокулюма в свежую среду до следующего субкультивирования. Для накопительных культур чаще всего используются конические широкогорлые колбы разных размеров на платформенных качалках кругового или полукругового типа со скоростью вращения 60-120 оборотов в минуту. Клетки растений, несмотря на ряд специфических особенностей, подчиняются тем же законам роста, что и микроорганизмы, поэтому для их выращивания применяют технологию и аппаратуру, принятую в работе с микроорганизмами. Микроорганизмы обычно культивируют в особых аппаратах, называемых ферментерами. Накопительные культуры можно выращивать в лабораторных ферментерах рабочим объемом 0, 5-10 л. По сравнению с глубинным выращиванием в колбах на качалке при культивировании клеток в ферментерах появляются принципиально новые возможности, связанные с их конструкцией.
|
|
|
На культуру клеток в ферментерах можно в любой момент воздействовать различными факторами (температура, свет, газовый режим, физиологически активные вещества, рН и др. ) и отбирать пробы клеток для определения динамики роста и метаболизма популяции в цикле выращивания. То есть, не нарушая режима асептики, можно контролировать рост и продуктивность биомассы, изучать влияние на эти процессы различных воздействий. Вместе с тем культивирование растительных клеток в ферментерах сопряжено с трудностями, вытекающими из специфических особенностей клеток высших растений. Наличие вакуоли и целлюлозно-пектиновой оболочки, придающей клеткам не только прочность, но и хрупкость, обуславливает их подверженность механическому стрессу при перемешивании и аэрации. Опасность механического стресса усиливается на стадии растяжения клеток.
Ферментеры различных конструкций обеспечивают перемешивание и аэрацию по-разному: вращаясь вокруг собственной оси, будучи в наклонном состоянии, перемешиванием магнитными и механическими мешалками, продуванием сжатого стерильного воздуха через суспензию. Конструкция лопастей мешалок бывает разной, и вращаются они с разной скоростью.
Высокая скорость перемешивания ведет к разрушению клеток, снижение интенсивности перемешивания может привести к оседанию части клеток к их гибели. Рост биомассы, которого так стараются добиться в работе ученые, ведет к возрастанию вязкости, что так осложняет культивирование. В отличие от микроорганизмов растительные клетки слипаются между собой и с поверхностями культиватора. Кроме того, они могут скапливаться в верхней части сосуда, образуя пену. Перечисленные особенности растительных клеток заставляют исследователей очень тщательно подходить к выбору типа культиваторов и режиму перемешивания в зависимости от целей и задач экспериментов с суспензионной культурой.
|
|
|
Способ, при котором клетки выращиваются в проточном режиме, называется непрерывным культивированием. В основу создания проточных систем легли опыты, в которых было обнаружено, что добавление в суспензию в фазу экспоненциального роста культуры порций свежей питательной среды позволяет долго поддерживать деление клеток. Непрерывное культивирование может осуществляться в закрытой проточной, полупроточной и открытой проточной системах.
В закрытой проточной системе суспензионная культура непрерывно снабжается свежей средой, приток которой сбалансирован оттоком равного количества использованной среды. В такой системе хорошо изучать влияние различных факторов на метаболизм клеток.
При полупроточном режиме выращивания определенная часть суспензии время от времени отбирается и оставшаяся часть разбавляется свежей средой.
Применяется для получения большой биомассы с целью ее биохимического исследования.
Открытая проточная система устроена так, что обеспечивает баланс между притоком свежей питательной среды и удалением равного объема клеточной суспензии. Скорость удаления части клеток из системы должна соответствовать скорости образования новых клеток в результате деления, это создает равновесное состояние между ростом клеток (постоянством скорости клеточного деления) и биосинтезом (постоянством состава и метаболической активности).
В открытой проточной системе исследуются взаимосвязи между процессами роста и метаболизма, те изменения, которые происходят при переходе клеток от одного состояния к другому, а также условия оптимального режима культивирования для получения максимального количества вторичных метаболитов. В основу непрерывного культивирования могут быть положены принципы хемостата и турбидостата, разработанные при культивировании микроорганизмов (рис. 4).
В хемостатном режиме непрерывное культивирование идет под воздействием лимитирующего рост фактора. Хемостатная культура представляет собой перемешиваемую суспензию, в которую с постоянной скоростью поддается свежая среда с заданной концентрацией какого-то лимитирующего рост компонента и с такой же скоростью отбирается часть культуры. Общий объем суспензии остается постоянным. При выращивании клеточных суспензий в хемостатном режиме скорость размножения клеток регулируется концентрацией лимитирующего фактора. Скорость роста и плотность клеточной популяции проходят в соответствии с заданной скоростью поступления среды (скорость разбавления), т. е. подачей лимитирующего фактора и других компонентов среды. Это приводит популяцию в стационарное состояние, для которого характерны выравненность физиологического состояния, постоянства концентрации лимитирующего фактора и других компонентов среды.
|
|
|
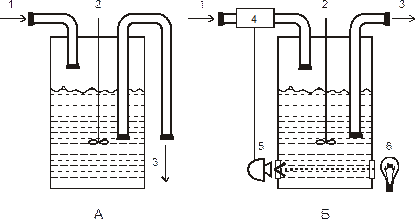
А – хемостат; Б – турбидостат с автоматической регуляцией оптической
плотности.
1 – поступление среды, 2 – мешалка, 3 – сток культуры, 4 – насос,
5 – фотоэлемент, 6 – источник света
Рисунок 4. Схемы биореакторов для проточного культивирования
микроорганизмов
Принцип турбидостата предусматривает непрерывное культивирование без внешнего лимитирования, рост клеток популяции поддерживается на определенном уровне регулированием оптической плотности культуры. Для этого подходят суспензии с низкой плотностью клеток и высокой удельной скоростью роста, т. е. популяции в начальные фазы роста. Турбидостат представляет собой хемостат, дополненный фотоэлектрическим элементом, чувствительным к мутности культуры. Рост клеточной популяции поддерживается на заданном уровне автоматически с помощью фотометрической регуляции подачи среды.
Хемостатный и турбидостатный режимы применяют с целью стабилизации клеточной популяции в определенном состоянии роста и поддержания его неограниченное время. Эти приемы культивирования очень ценны для изучения регуляции роста и метаболизма клеток в строго стандартных условиях под влиянием различных лимитирующих и ингибирующих факторов. Однако, таких работ очень мало, что связано с новизной метода и техническими трудностями. Препятствием к культивированию клеток высших растений в проточном режиме является их высокая чувствительность к повреждениям, агрегированность, длительное время генерации.
3. Рост клеток описывается S-образной кривой. Она получается, если число клеток в культуре или их массу представить как функцию времени, прошедшего с момента их высева (рис. 5). Кривая характерна для популяции клеток, культивируемых как поверхностным способом, так и в жидкой среде, и состоит из следующих фаз: 1) латентная фаза, или лаг-фаза, во время которой отсутствует видимый рост, но идет активный процесс поглощения воды, питательных веществ и подготовки к делению; 2) экспоненциальная, или логарифмическая, фаза роста, в которой по любому принятому критерию возрастает удельная скорость роста; 3) линейная фаза - очень короткая, удельная скорость роста в этой фазе постоянная; 4) фаза замедления роста, в которой скорость роста уменьшается; 5) стационарная фаза, в которой по любому принятому критерию рост постоянен; 6) фаза гибели клетки. Однако форма реальных ростовых кривых может значительно отличаться от моделей продолжительностью фаз. Это зависит как от генотипа, так и от условий выращивания и количества инокулюма и транспланта.
|
Рисунок 5. Кривая ростового цикла клеток in vitro
|
|
|



