 |
Химические реагенты.
|
|
|
|
Для приготовления промывочных жидкостей применяются разные по составу глины и вода, в связи с этим свойства растворов могут быть весьма разнообразными.
Кроме того, в процессе бурения под действием солей, присутствующих в подземных водах и частиц выбуренной породы параметры промывочных жидкостей сильно меняются. Для придания раствору определенных технологических свойств, отвечающих требованиям конкретных геологических условий, производят обработку промывочных жидкостей различными химическими реагентами.
Химические реагенты могут вызвать пептизацию глинистых частиц, что приведет к увеличении коллоидных частиц в составе глинистого раствора. Это повышает их стабильность, усиливает структурообразование, повышает устойчивость к действию растворимых солей.
Регулирование свойств глинистых растворов основано на двух основных принципах:
- изменение физико-химического состояния дисперсной системы, свойств поверхности раздела твердой и жидкой фаз;
- изменение состава и концентрации твердой фазы.
Изменение состояния дисперсной системы достигается вводом в глинистый раствор соответствующих химических реагентов, а регулирование состава и концентрации дисперсной фазы достигается разбавлением водой, механическим удалением части твердой фазы, вводном специальных добавок без изменения физико-химического состояния дисперсной системы.
Для регулирования свойств глинистых растворов применяют химические реагенты двух групп по химической природе: неорганические реагенты – электролиты и органические реагенты, – защитные коллоиды.
Краткая характеристика и действие наиболее часто применяемых реагентов - электролитов приводится ниже.
|
|
|
Кальцинированная сода (карбонат натрия – Na2CO3) представляет собой белый порошок, хорошо растворимый в воде, плотность 2, 53 г/см3. Перед вводном в промывочную жидкость ее предварительно растворяют в воде, но возможен ввод в сухом виде.
Назначение:
- связывание двухвалентных катионов, поступающих в раствор при перебуривании гипса, ангидрита, цемента или с пластовой минерализованной водой;
- ухудшение свойств глинистых растворов, приготовленных из местных глин невысокого качества;
- повышение качества глинопорошков из небентонитовых глин, увеличение выхода глинистого раствора;
- повышение щелочности глинистого раствора.
При вводе кальцинированной соды в раствор из кальциевой глины анионы CO3--взаимодействуют с катионами Ca++, образуя диффузный слой на поверхности глинистой частицы. При этом образуется нерастворимый карбонат кальция:
 (6. 14)
(6. 14)
На поверхности глинистых частиц то же адсорбируются катионы Na++, то есть идет катионный обмен, которому способствуют анионы CO3--, а глина из кальциевой превращается в натриевую:
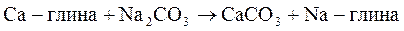 (6. 15)
(6. 15)
Это способствует увеличению толщины диффузного слоя катионов, улучшению гидратации глины и агрегативной устойчивости глинистой суспензии.
При обработке глинистой суспензии, загрязненной сульфатом кальция (гипс, ангидрит), анионы CO3-- связывают агрессивные катионы кальция:
 , (6. 16)
, (6. 16)
Продукты реакции не влияют на свойства глинистой суспензии. При разбуривании цемента гидрооксид кальция вызывает коагуляцию раствора, которую можно избежать путем обработки кальцинированной содой:
 , (6. 17)
, (6. 17)
То же самое происходит при попадании в раствор хлоридов кальция из минерализованных води растворимых пород:
|
|
|
 , (6. 18)
, (6. 18)
Каустическая сода (гидроксид натрия - NaOH) применяется для обработки почти всех видов промывочных жидкостей на водной основе. Это твердое вещество белого цвета, легко растворимое в воде с выделением тепла. Плотность 2, 13 г/см3. Твердый гидроксид поглощает из воздуха пары воды и CO2. Поставляется в твердом виде в металлических барабанах массой 200 кг или в виде 40 – 50 % раствора.
Назначение:
- нейтрализация сероводорода, поступающего из перебуриваемых пород;
- растворение органических реагентов;
- связывание двухвалентных катионов;
- повышение щелочности растворов.
При разбуривании хемогенных отложений или попадании в раствор пластовой воды происходит реакция хлоридов с каустической содой, например:
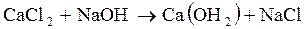 , (6. 19)
, (6. 19)
При поступлении в раствор сероводорода идет реакция:
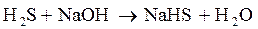 (6. 20)
(6. 20)
В первом случае образуется слаборастворимый гидроксид кальция, а во втором – безвредный сульфид натрия.
Гидроксид кальция (гашеная известь – Ca(OH2)) – широко применяется для регулирования свойств глинистых растворов.
Назначение:
- загущение глинистых растворов при их гидрофильной коагуляции и повышении структурных свойств;
- увеличение содержания катионов кальция в фильтрате;
- повышение щелочности глинистых растворов.
Гашеная известь – порошок белого цвета, плотность 2, 24 г/см3, слабо растворимый в воде.
Вводится в глинистый раствор в виде известкового молочка – насыщенного раствора Ca(OH2), содержащего во взвешенном состоянии нерастворимый гидроксид кальция.
Действие органических реагентов – защитных коллоидов связано с тем, что при их вводе в глинистый раствор молекулы этих реагентов адсорбируются на поверхности глинистых частиц и предотвращают взаимное слипания. Это приводит к повышению агрегативной устойчивости глинистой суспензии, подавляет способность глинистого раствора к структурообразованию.
Органические реагенты имеют относительно небольшую молекулярную массу, разжижают глинистые суспензии за счет значительного снижения интенсивности структурообразования.
Старейшими органическими реагентами являются химические реагенты на основе гуминовых кислот – гуматы. Гуматные реагентами являются натриевые или калиевые соли гуминовых кислот, содержащихся в буром угле и торфе. Экстрагируя эти кислоты в виде солей гуминовых кислот с помощью едкого натра, получаются водо-растворимые соединения, дающие коллоидный раствор в воде. Приготовление углещелочного (УЩР) и торфо-щелочного (ТЩР) реагентов сводится к воздействию щелочи NaOH на бурый уголь или торф в составе водной среды, нагреваемой периодически до кипения в течении 24 часов, что необходимо для щелочной вытежки гуминовых кислот. Наиболее эффективными реагентами являются такие, которые получены при соотношении 10 – 15 % бурого угля или торфа, и 1 – 3 % щелочи.
|
|
|
Гуматные реагенты предназначены для снижения показателя фильтрации и вязкости пресных или слабоминерализованных (до 2, 5 % NaCl) раствора.
При производстве буровых работ УЩР применяется в виде водного раствора, а также пасто- и порошкообразном виде.
Наибольшее применение получил порошкообразный УЩР, который получается путем сменшивания сухого бурого угля с концентрированной 20 – 45 % щелочью. После просушивания реагент в виде порошка расфасовывается в мешки. Активность УЩР оценивается по способности снижать показатель фильтрации. У реагента высокой активности показатель фильтрации не должен превышать 2 – 3 см3 за 30 мин.
Нитрогуматный реагент (НГР) получают при обработке бурого угля азотной кислотой (HNO3) с последующей нейтрализацией кислоты с помощью щелочи NaOH, расход которой составляет до 40 % от массы продукта. В пресных и слабоминенрализованых растворах НГР снижает вязкость и показатель фильтрации (до 1 – 2 %). Для растворов с высокой минерализацией (NaCl более 5 %) такой реагент более эффективно снижает те же параметры до 5 – 10 %.
Сульфированный нитрогуматный реагент (СНГР) получается при обработке бурого угля 8 % - ной азотной кислотой с последующим сульфированием бисульфитом натрия (Na2SO3) в присутствии едкого натра в течения 3 часов. Применяется для регулирования свойств пресных и слабоминерализованных растворов (NaCl до 5 %), в которых более эффективно, чем УЩР или ТЩР, СНГР снижает вязкость, статическое напряжение сдвига и показатель фильтрации (до 5 – 8 %).
|
|
|
Лигносульфонаты – являются высокомолекулярными органическими реагентами, способствуюми повышению агрегативой устойчивости глинистых суспензий за счет образования на глинистых частицах защитных оболочек из молекул реагентов.
Лигносульфонаты применяются для разжижения глинистых растворов, кроме того эти реагенты понижают водоотдачу за счет дополнительного диспергирования глины и повышения концентрации коллоидной фракции твердой фазы в глинистом растворе. Адсорбирируясь на глинистых частиц, молекулы реагентов обеспечивают снижение водоотдачи, образуя при фильтрации менее проницаемую глинистую корочку при затруднении отделения фильтрата.
Сульфит – спиртовая барда (ССБ) – побочный продукт производства целлюлозы из древесины, представляющий собой смесь органических веществ, в которой преобладают соли лигносульфоновых кислот: лигносульфонаты кальция, натрия, алюминия.
ССБ хорошо растворима в воде, образует коллоидный раствор. Поставляется в виде 40 – 50 %-ного водного раствора, реже в виде твердой вароподобной аморфной массы или порошкообразного продукта.
Основное назначение ССБ – разжижение кальциевых глинистых растворов, в отличие от натриевых глинистых суспензий, где катионы кальция вызывают коагуляцию таких растворов. Одновременно ССБ способствует снижению водоотдачи.
ССБ используется совместно с каустической содой (5 весовых частей NaOH на 30 частей ССБ) для разжижения глинистых суспензий в щелочной среде.
Конденсированная сульфит – спиртовая барда (КССБ) представляет собой модификацию ССБ при нагревании ее в присутствии формалина и серной кислоты.
Разновидности КССБ:
- КССБ – 1 – для понижения водоотдачи пресных глинистых растворов при температурах до 120ОС, эффективно снижает вязкость растворов из приготовленных из кальциевых глин;
- КССБ – 2 – понижает водоотдачу глинистых растворов при минерализации до 100 г/л NaCl и температуре до 150ОС;
- КССБ – 4 – для понижения водоотдачи пресных и минерализованных глинистых растворов. В пресных растворах реагент эффективен при температурах до 185 – 200ОС.
Окисленная сульфит – спиртовая барда (ОССБ) – это хромлигносульфонат, который приготовляется путем смешивания ССБ с хромпиком (Na2Cr2O7x2H2O) и выдерживания в течение 14 – 18 часов.
ОССБ способна разжижать глинистые растворы при содержании более 200 мг/л катионов кальция и высоких температурах.
|
|
|
Природный водорастворимый полисахарид – крахмал, является смесью полисахаридов с общей формулой (C6H10O5)n.
Промышленность выпускает для нужд бурения модифицированный крахмал МК –1, который получают путем нагрева крахмальной суспензии до 160ОС в присутствии алюмокалиевых квасцов – KAl(SO4)2∙ 12H2O. Реагент МК – 1 представляет собой белый порошок. Постепенное растворение модифицированного крахмала происходит при циркуляции глинистого раствора. Основное назначение МК – 1 – понижение водоотдачи сильноминерализованных глинистых растворов, особенно в присутствии соединений кальция и магния.
Карбоксиметилцеллюлоза (КМЦ) – является водорастворимым эфиром целлюлозы, представляющей собой нерастворимый в воде полисахарид [C6H7O2(OH)3]n.
КМЦ получается из целлюлозы при обработке ее NaOH и монохлоруксусным натрием. Её общая формула имеет вид:
[C6H7O2(OH)3-x – (OCH2COONa)x]n
Разновидности КМЦ отличается степенью замещения (СЗ), степенью полимеризации (СП), а также по виду замещений в формуле эфира целлюлозы – [C6H7O2(OH)3-x – (OCH2COOH)x]n – водородной формы КМЦ.
Натриевая, калиевая и аммонийная соли КМЦ хорошо растворимы в воде (при СЗ> 40) и сокращенно Na – КМЦ, K – КМЦ и NH4 – КМЦ соответственно. Наибольшее распространение получила Na – КМЦ или просто КМЦ.
Оптимальной степенью замещения является 80 – 90, при этом рост степени полимеризации до 800 способствует возрастанию стабилизирующей способности, а также термо- и солестойкости КМЦ.
Для бурения выпускают три марки технической КМЦ: КМЦ – 500, КМЦ – 600 и КМЦ – 700. КМЦ – 500 применяют в концентрации до2, 5 % для снижения водоотдачи при насыщении раствора по NaCl и температуре до 145ОС; КМЦ – 600 в концентрации до 2 % применяют для снижения водоотдачи сильноминерализованных растворов и температуре до 160ОС; КМЦ – 700 в концентрации до 1, 8 % применяют для снижения водоотдачи сильноминерализованных и малоглинистых растворов при температуре до 180ОС.
Минерализованные растворы при добавлении КМЦ разжижаются за счет того, что этот реагент образует на глинистых частицах защитные оболочки и подавляет структурообразование.
Способность КМЦ понижать водоотдачу глинистых суспензий зависит от щелочности среды. Наиболее эффективно этот реагент понижает водоотдачу при pH = 8, 5 – 10.
|
|
|


