 |
Определение изменения энтропии при нагреве
|
|
|
|
И плавлении олова
Цель и задача работы: изучение I и II законов термодинамики, определение приращения энтропии при фазовом переходе первого рода на примере плавления олова.
Общие сведения
Все процессы в природе необратимы. Всякий процесс, при котором система переходит из одного состояния в другое, протекает таким образом, что нельзя провести его в обратном направлении без изменений в окружающих телах. Это связано с рассеянием части энергии в любом процессе за счет трения, излучения и других причин. В любом из них изменяется состояние в целом, часть энергии системы рассеивается. Для характеристики этого общего для всех систем свойства вводится физическая величина — энтропия, которая является мерой бесполезности внутренней энергии с точки зрения совершения работы (мера беспорядка).
Слово энтропия в переводе с греческого языка означает слово вовнутрь, возвращение. Имеется в виду преобразование энергии в обратимых процессах. Термин энтропия был предложен Клаузиусом для обозначения функции состояния термодинамической системы
 , (1)
, (1)
где  - энтропия, Дж/К; Q – теплота, полученная данной системой или отданная ею, Дж; Т – абсолютная температура, К. Энтропией (
- энтропия, Дж/К; Q – теплота, полученная данной системой или отданная ею, Дж; Т – абсолютная температура, К. Энтропией ( ) называется функция состояния системы, дифференциал которой в элементарном обратимом процессе равен отношению бесконечно малого количества тепла dQ, сообщенного системе, к абсолютной температуре Т.
) называется функция состояния системы, дифференциал которой в элементарном обратимом процессе равен отношению бесконечно малого количества тепла dQ, сообщенного системе, к абсолютной температуре Т.
Общее изменение энтропии в любом процессе
 . (2)
. (2)
Во всех случаях в результате передачи теплоты Q от нагретого тела к холодному происходит выравнивание их температур. При этом снижается возможность совершения работы, уменьшается предельно высокий КПД. Вместе с тем повышается доля связанной энергии, увеличивается энтропия. При полном выравнивании температур КПД становится равным нулю. При этом энтропия достигает максимума, а энергия системы целиком не может быть использована для совершения работы. Полное значение энтропии в системе не поддается учету, но в изолированной системе можно найти изменение энтропии в любом процессе.
|
|
|
Описание установки и вывод расчетной формулы
Схема установки для определения изменения энтропии приведена на рисунке 1.

Рисунок 1 Схема установки: 1 – электропечь; 2 – тигель с оловом;
3 – термопара; 4 – прибор для измерения температуры
Установка состоит из электропечи 1, в которую помещают тигель с оловом 2, в олово введена термопара, соединенная с прибором для измерения температуры 4 (логометром или милливольтметром). Питание осуществляется от электросети с напряжением 220 В.
Для определения общего изменения энтропии олова в процессе нагрева и плавления необходимо вычислить количество тепла, сообщенное данной массе олова в каждом из этих процессов
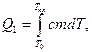 (3)
(3)
где  - теплота, переданная данному телу при нагреве, Дж; с – удельная теплоемкость олова, Дж/кг×K; m – масса олова, кг;
- теплота, переданная данному телу при нагреве, Дж; с – удельная теплоемкость олова, Дж/кг×K; m – масса олова, кг;  - комнатная температура, К;
- комнатная температура, К;  - температура плавления олова, К.
- температура плавления олова, К.
 , (4)
, (4)
где 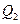 - теплота, переданная данной массе олова при плавлении, Дж;
- теплота, переданная данной массе олова при плавлении, Дж;  - удельная теплота плавления, Дж/кг; m – масса олова, кг.
- удельная теплота плавления, Дж/кг; m – масса олова, кг.
Подставляя значения  и
и 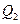 в формулу (1) получим
в формулу (1) получим
 ; (5)
; (5)

 . (6)
. (6)
Так как
Q=  +
+ 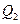 ,
,
то общее изменение энтропии
 . (7)
. (7)
Порядок выполнения работы и требования
К оформлению результата
3.1 При подготовке к лабораторной работе необходимо изучить и законспектировать следующие библиографические источники:
- для неинженерных специальностей С. 232–244 /1/.
- для инженерных специальностей С. 110–114 /2/; С. 89–123 /3/.
3.2 Поместить в тигель кусочки олова.
|
|
|
3.3 Привести в контакт термопару с оловом.
3.4 Включить электронный потенциометр.
3.5 Записать комнатную температуру  .
.
3.6 Включить одновременно цепь печи и секундомер, отмечая показания потенциометра через каждые полминуты.
3.7 Данные внести в таблицу 1. Измерения проводить до тех пор, пока температура не достигнет постоянной величины  , а затем начнет увеличиваться.
, а затем начнет увеличиваться.
Таблица 1 Результаты измерений
| Обозн. физ. вел. | Полученные результаты | ||||||||
 мин. мин.
| |||||||||

|
3.8 Выключить цепь печи и проводить аналогичные измерения при охлаждении олова.
3.9 Построить график 
3.10 По полученному графику определить температуру плавления олова  . Затем перевести в К:
. Затем перевести в К:  .
.
3.11 Вычислить по формулам (5 - 7) приращение энтропии при нагревании и плавлении олова т. е.:  ,
,  ,
,  . Параметры, необходимые для вычислений, приведены в таблице 2.
. Параметры, необходимые для вычислений, приведены в таблице 2.
Таблица 2 Однократно измеренные величины
| Обозначения физических величин | |||||||

| 
| 
| 
| 
| 
| 
| 
|
(20,0±0,1)10-3 кг 
| (250±0,5) Дж/кг | (5,80±0,05) 103 Дж/кг К | 
|
3.12 Определить абсолютные погрешности по формулам:
 ; (8)
; (8)
 ; (9)
; (9)
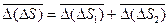 . (10)
. (10)
3.13 Записать окончательный результат в виде:
 . (11)
. (11)
4 Контрольные вопросы
4.1 Какие формулировки второго закона термодинамики Вам известны?
4.2 Какие два толкования энтропии Вы знаете?
4.3 Какие термодинамические процессы называются круговыми, обратимыми и необратимыми?
4.4 Как изменяется энтропия при различных процессах?
4.5 Что Вы знаете о вечном двигателе второго рода?
4.6 По какому признаку можно безошибочно отличить кристаллическое тело от аморфного?
4.7 Как выглядят графики плавления аморфного тела и тела кристаллического?
4.8 Что такое приведенная теплота?
4.9 Каков физический смысл неравенства Клаузиуса?
4.10 Можно ли уменьшить энтропию тела, входящего в замкнутую систему?
4.11 Может ли изменяться энтропия при неизменной температуре?
Лабораторная работа №6
|
|
|


