 |
Энергия характеризует способность тела (или система тел) совершать работу.
|
|
|
|
Различают два вида механической энергии – кинетическая Ек и потенциальная Еп.
Кинетическая энергия -энергия тела, обусловленная его движением (скоростью)., где m — масса тела (кг), h -высота тела на Землей (м).Это энергия взаимодействия тела с Землей.
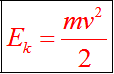
| Потенциальная энергия – энергия тела, обусловленная взаимным расположением взаимодействующих между собой тел., где m — масса тела (кг), V — скорость (м/с2)
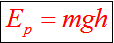
|
Обратим внимание, что у работы и энергии одинаковые единицы измерения. Это означает, что работа может переходить в энергию. Например, для того, чтобы тело поднять на некоторую высоту, тогда оно будет обладать потенциальной энергией, необходима сила, которая совершит эту работу. Работа силы по поднятию перейдет в потенциальную энергию.
Полная механическая энергия замкнутой системы тел равна сумме потенциальной и кинетической энергий системы: Е = Ек +Еп.
Закон сохранения механической энергии гласит: В изолированно системе, в которой действуют консервативные силы, механическая энергия сохраняется: Е = Ек +Еп = const.

Энергия не создается и не уничтожается, а только превращается из одной формы в другую: из кинетической в потенциальную и наоборот. Учитывая значение Ек и Еп, закон сохранения механической энергии можно записать так:
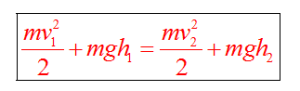
 В состоянии 2 тело обладает кинетической энергией (так как уже развило скорость), но при этом потенциальная энергия уменьшилась, так как h2 меньше h1. Часть потенциальной энергии перешло в кинетическую.
В состоянии 2 тело обладает кинетической энергией (так как уже развило скорость), но при этом потенциальная энергия уменьшилась, так как h2 меньше h1. Часть потенциальной энергии перешло в кинетическую.
Состояние 3 — это состояние перед самой остановкой. Тело как бы только-только дотронулось до земли, при этом скорость максимальная. Тело обладает максимальной кинетической энергией. Потенциальная энергия равна нулю (тело находится на Земле).
|
|
|
Полные механические энергии равны между собой, если пренебрегать силой сопротивления воздуха.
7. Механические колебания, свободные и вынужденные колебания, резонанс, превращение энергии при механических колебаниях.
Механические колебания – это движения, которые точно или приблизительно повторяются через определенные интервалы времени. (например, колебание ветки на дереве, маятника часов, автомобиля на рессорах и так далее)
Колебания бывают свободными и вынужденными.
Колебания, возникающие в системе под действием внутренних сил, называются свободными. Все свободные колебания затухают. (например: колебание струны, после удара)
Колебания, совершаемые телами под действием внешних периодически изменяющихся сил, называются вынужденными (например: колебание металлической заготовки при работе кузнеца молотом).
Условия возникновения свободных колебаний:
· При выведении тела из положения равновесия в системе должна возникнуть сила, стремящаяся вернуть его в положение равновесия;
· Силы трения в системе должны быть очень малы (т.е. стремиться к нулю).
 В реальных колебательных системах всегда происходят потери энергии при свободных колебаниях. Механическая энергия расходуется на совершение работы по преодолению сил сопротивления воздуха. Под влиянием силы трения происходит уменьшение амплитуды колебаний, затем колебания прекращаются. Колебания, энергия которых уменьшается с течением времени за счет действия сил сопротивления, называются затухающими.
В реальных колебательных системах всегда происходят потери энергии при свободных колебаниях. Механическая энергия расходуется на совершение работы по преодолению сил сопротивления воздуха. Под влиянием силы трения происходит уменьшение амплитуды колебаний, затем колебания прекращаются. Колебания, энергия которых уменьшается с течением времени за счет действия сил сопротивления, называются затухающими.
 Вынужденные колебания являются незатухающими. Поэтому необходимо восполнять потери энергии за каждый период колебаний. Вынужденные колебания совершаются с частотой, равной частоте изменения внешней силы.
Вынужденные колебания являются незатухающими. Поэтому необходимо восполнять потери энергии за каждый период колебаний. Вынужденные колебания совершаются с частотой, равной частоте изменения внешней силы.
Любое колебание характеризуется:
1. Xm (А)– модуль максимального смещения точки от положения равновесия называется амплитудой (м);
|
|
|
2. T – время одного полного колебания называется периодом (с); 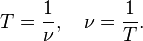
3. Число колебаний в единицу времени называется частотой (ν):
 Резонанс – это явление резкого возрастания амплитуды вынужденных колебаний при совпадении частоты изменения внешней силы, действующей на систему, с частотой свободных колебаний (
Резонанс – это явление резкого возрастания амплитуды вынужденных колебаний при совпадении частоты изменения внешней силы, действующей на систему, с частотой свободных колебаний (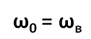 ).
).
Явление резонанса учитывается в акустике, радиотехнике и технике. В строительстве, например, при сооружении мостов и других сооружений, которые подвержены механическим колебаниям и действию внешней силы.
Существует несколько колебательных систем – математический маятник (шарик на тонкой длинной нити) и пружинный маятник (тело на пружине).
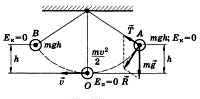
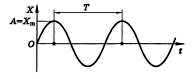 Самый простой вид колебательного движения — гармонические колебания, при которых физическая величина периодически изменяется со временем по закону синуса или косинуса (рис.).При гармонических колебаниях периодически происходит переход потенциальной энергии в кинетическую и обратно:
Самый простой вид колебательного движения — гармонические колебания, при которых физическая величина периодически изменяется со временем по закону синуса или косинуса (рис.).При гармонических колебаниях периодически происходит переход потенциальной энергии в кинетическую и обратно:
… Екин → Ер → Екин →…
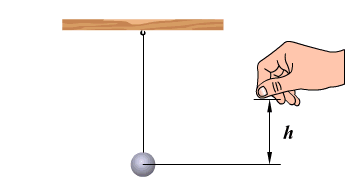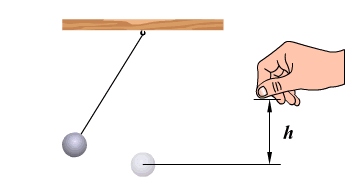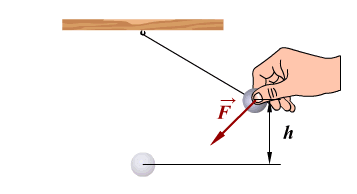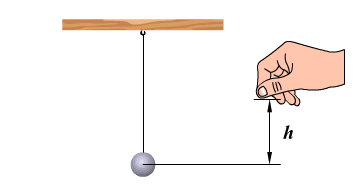
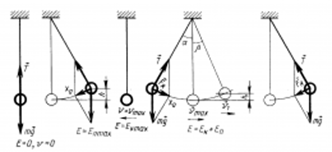 На примере колебаний тела на нити видим превращение энергии. В 1 положении наблюдаем равновесие колебательной системы. Скорость и, следовательно, кинетическая энергия тела максимальны. При отклонении маятника от положения равновесия он поднимается на высоту h относительно нулевого уровня, следовательно, в точке А маятник обладает потенциальной энергией Ер. При движении к положению равновесия, к точке О, уменьшается высота до нуля, а скорость груза увеличивается, и в точке О вся потенциальная энергия Ер превратится в кинетическую энергию Екин. В положении равновесия кинетическая энергия имеет максимальное значение, а потенциальная энергия минимальна. После прохождения положения равновесия по инерции происходит превращение кинетической энергии в потенциальную, скорость маятника уменьшается и при максимальном отклонении от положения равновесия становится равной нулю. Екин = 0, Ер = max
На примере колебаний тела на нити видим превращение энергии. В 1 положении наблюдаем равновесие колебательной системы. Скорость и, следовательно, кинетическая энергия тела максимальны. При отклонении маятника от положения равновесия он поднимается на высоту h относительно нулевого уровня, следовательно, в точке А маятник обладает потенциальной энергией Ер. При движении к положению равновесия, к точке О, уменьшается высота до нуля, а скорость груза увеличивается, и в точке О вся потенциальная энергия Ер превратится в кинетическую энергию Екин. В положении равновесия кинетическая энергия имеет максимальное значение, а потенциальная энергия минимальна. После прохождения положения равновесия по инерции происходит превращение кинетической энергии в потенциальную, скорость маятника уменьшается и при максимальном отклонении от положения равновесия становится равной нулю. Екин = 0, Ер = max
Закон сохранения механической энергии: сумма кинетической и потенциальной энергий остается неизменной: Екин = Ер = const
8. Возникновение атомистической гипотезы строения вещества и её экспериментальные доказательства, идеальный газ, основное уравнение молекулярно-кинетической теории идеального газа, абсолютная температура как мера средней кинетической энергии теплового движения частиц вещества.
|
|
|
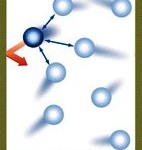 Модель идеального газа
Модель идеального газа
Атомистическая теория — современная теория строения вещества — зародилась еще в Древней Греции. Основное направление мысли древнегреческих философов основывалось на представлении о непрерывности материи (взгляд Аристотеля). Однако некоторые древнегреческие философы, особенно Демокрит, не соглашались с такой точкой зрения и считали, что материя состоит из мельчайших неделимых частиц. Демокрит называл их атомами, что значит “неделимые”. То, что вещество состоит из мельчайших частиц – молекул и атомов экспериментально доказывают броуновское движение и явление диффузия.
Идеальный газ — это физическая модель реального газа, взаимодействие, между молекулами которого пренебрежимо мало. Модель введена для математического описания поведения газов. Реальные разреженные газы (верхние слои атмосферы) ведут себя как идеальный газ.
Свойства идеального газа:
· молекулы — это упругие шары;
· расстояние между молекулами намного больше размеров молекул- диаметра (r>d);
· силы отталкивания возникают только при их соударении;
· движение молекул подчиняется законам Ньютона;
· давление газа на стенки сосуда оказывается за счет ударов молекул газа.
Давление газа на стенки сосуда пропорционально произведению концентрации молекул на среднюю кинетическую энергию поступательного движения молекулы.
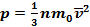 или
или 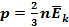 — выражения основного уравнения МКТ, где р — давление газа на стенки сосуда (Па); n — концентрация молекул, т.е. число молекул в единице объема n=N/V, (1/м3); m0 — масса одной молекулы (кг);
— выражения основного уравнения МКТ, где р — давление газа на стенки сосуда (Па); n — концентрация молекул, т.е. число молекул в единице объема n=N/V, (1/м3); m0 — масса одной молекулы (кг);  — средняя квадратичная скорость движения газовых молекул (м/с); ρ — плотность газа (кг/м3);
— средняя квадратичная скорость движения газовых молекул (м/с); ρ — плотность газа (кг/м3); 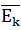 — средняя кинетическая энергия молекул (Дж).
— средняя кинетическая энергия молекул (Дж).
Основное уравнение МКТ идеального газа связывает микро параметры частиц (массу молекулы, средний квадрат скорости молекул) с макро параметрами газа (р — давление, V — объем, Т — температура).
|
|
|
Температура характеризует степень нагретости тела, тепловое равновесие, указывает направление теплообмена. Измеряют температуру термометром. При измерении температуры используется зависимость изменения какого-либо макроскопического параметра (объема, давления, электрического сопротивления и т.д.) вещества от температуры. В жидкостных термометрах — это изменение объема жидкости. В процессе измерения температура тела и термометра приходят в состояние теплового равновесия.
 Абсолютная шкала температурвведена англ. физиком У. Томсоном(Кельвином). Ее называют шкалой Кельвина или термодинамической температурной шкалой. В ней нет отрицательных температур. Абсолютная шкала температуры называется так, потому что мера нижнего предела температуры — абсолютный ноль, то есть наиболее низкая возможная температура, при которой молекулы вещества перестают двигаться. Единица абсолютной температуры в СИ: [T]=1K (Кельвин). Нулевая температура абсолютной шкалы – это абсолютный ноль 00К = −273.15 °C (точно). По величине 1К = 10С. Шкала температур Кельвина — это шкала, в которой начало отсчёта ведётся от абсолютного нуля.
Абсолютная шкала температурвведена англ. физиком У. Томсоном(Кельвином). Ее называют шкалой Кельвина или термодинамической температурной шкалой. В ней нет отрицательных температур. Абсолютная шкала температуры называется так, потому что мера нижнего предела температуры — абсолютный ноль, то есть наиболее низкая возможная температура, при которой молекулы вещества перестают двигаться. Единица абсолютной температуры в СИ: [T]=1K (Кельвин). Нулевая температура абсолютной шкалы – это абсолютный ноль 00К = −273.15 °C (точно). По величине 1К = 10С. Шкала температур Кельвина — это шкала, в которой начало отсчёта ведётся от абсолютного нуля.
В формулах абсолютная температура обозначается буквой «Т», а температура по шкале Цельсия буквой «t». T = t+273 (K).
После введения абсолютной температуры получаем выражение: 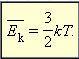 — средняя кинетическая энергия поступательного движения молекул, где
— средняя кинетическая энергия поступательного движения молекул, где 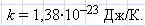 — постоянная Больцмана, устанавливает связь между энергетическими и температурными единицами.
— постоянная Больцмана, устанавливает связь между энергетическими и температурными единицами.
Температура – мера средней кинетической энергии теплового движения частиц вещества.
9. Давление газа, уравнение состояния идеального газа (уравнение Менделеева - Клайперона), изопроцесы.
Давление газа возникает в результате столкновений молекул со стенками сосуда (и на помещенное в газ тело), в котором находится беспорядочно движущиеся молекулы газа. Чем чаше удары, тем они сильнее – тем выше давление. Если масса и объем газа неизменны, то его давление в закрытом сосуде всецело зависит от температуры. Давление зависит и от скорости поступательно движущихся газовых молекул. Единица измерения давления — паскаль p(Па). Измеряют давление газа манометром (жидкостным, металлическим и электрическим).
Идеальный газ – это модель реального газа. За идеальный газ принимают газ в сосуде, когда молекула, пролетая от стенки до стенки сосуда не испытывает столкновения с другими молекулами. Точнее, Идеальный газ – это газ, взаимодействие между молекулами которого пренебрежимо мало ⇒ Eк >> Eр.
Основное уравнение МКТ связывает макроскопические параметры (давление p, объём V, температура T, масса m) газовой системы с микроскопическими параметрами (масса молекулы, средняя скорость их движения): 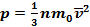
|
|
|
, где n — концентрация, 1/м3; m — масса молекулы, кг; 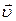 — средняя квадратичная скорость молекул, м/с.
— средняя квадратичная скорость молекул, м/с.
Уравнение состояния идеального газа — формула, устанавливающая зависимость между давлением, объёмом и абсолютной температурой идеального газа, характеризующее состояние данной системы газа. 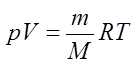 — уравнение Менделеева — Клапейрона (для произвольной массы газа). R = 8,31 Дж/моль·К — универсальная газовая постоянная. pV = RT – (для 1 моля).
— уравнение Менделеева — Клапейрона (для произвольной массы газа). R = 8,31 Дж/моль·К — универсальная газовая постоянная. pV = RT – (для 1 моля).
Часто необходимо исследовать ситуацию, когда меняется состояние газа при его неизменном количестве (m=const) и в отсутствие химических реакций (M=const). Это означает, что количество вещества ν=const. Тогда:
Для постоянной массы идеального газа отношение произведения давления на объем к абсолютной температуре в данном состоянии есть величина постоянная: 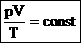 — уравнение Клапейрона.
— уравнение Клапейрона.
Термодинамический процесс (или просто процесс) — это изменение состояния газа с течением времени. В ходе термодинамического процесса меняются значения макроскопических параметров — давления, объёма и температуры. Особый интерес представляют изопроцессы — термодинамические процессы, в которых значение одного из макроскопических параметров остаётся неизменным.Поочерёдно фиксируя каждый из трёх параметров, мы получим т ри вида изопроцессов.
Последнее уравнение называют объединённым газовым законом. Из него получаются законы Бойля — Мариотта, Шарля и Гей-Люссака. Эти законы называют законами для изопроцессов:
Изопроцессы – это процессы, которые совершаются при одинаковом параметре или Т-температуре, или V-объеме, или р-давлении.
 Изотермический процесс —
Изотермический процесс — 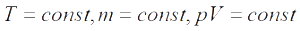
— закон Бойля — Мариотта (при постоянной температуре и данной массы газа произведение давления на объем есть величина постоянная)
 Изобарный процесс —
Изобарный процесс —
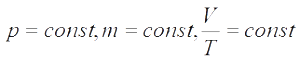
— закон Гей-Люссака (при постоянном давлении для данной массы газа отношение объема к температуре есть величина постоянная)
 Изохорный процесс —
Изохорный процесс —
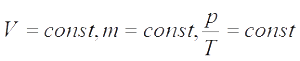
— закон Шарля (при постоянном объеме для данной массы газа отношение давления к температуре есть величина постоянная.
Вывели газовые законы из уравнения Менделеева — Клапейрона. Но исторически всё было наоборот: газовые законы были установлены экспериментально, и намного раньше. Уравнение состояния появилось впоследствии как их обобщение.
10. Испарение и конденсация, насыщенные и ненасыщенные пары, влажность воздуха.
В природе все реальные газы (кислород, азот, водород и т. д.) при определенных условиях способны превращаться в жидкость. Однако превращение газа в жидкость может происходить только при температурах ниже определенной, так называемой критической температуры. При комнатной температуре (20 — 250С) вода может находиться и в жидком, и в газообразном состояниях, а азот и кислород существуют только в виде газов. Парообразование — процесс превращения жидкости в пар.
Испарение — процесс парообразования с поверхности жидкости или твердого тела. Заключается он в вылетании частиц (молекул, атомов), кинетическая энергия которых превышает потенциальную энергию их связи с остальными частицами вещества. Испарение происходит при любой температуре и не требует постоянного притока тепла. Скорость испарения зависит от:
1. площади поверхности жидкости;
2. температуры;
3. движения молекул над поверхностью жидкости или газа;
4. рода вещества.
Может случиться, что через некоторое время молекула пара вернётся обратно в жидкость. Процесс перехода вещества из газообразного состояния в жидкое состояние называется конденсацией. Конденсация пара — процесс, обратный испарению жидкости.
Над свободной поверхностью жидкости всегда имеются пары этой жидкости. Если сосуд с жидкостью не закрыт, то всегда найдутся молекулы пара, которые удаляются от поверхности жидкости и не могут вернуться назад в жидкость. В закрытом сосуде жидкость и ее пар могут находиться в состоянии динамического равновесия, когда число молекул, вылетающих из жидкости, равно числу молекул, возвращающихся в жидкость из пара, т. е. когда скорости процессов испарения и конденсации одинаковы. Пар, находящийся в равновесии со своей жидкостью, называют насыщенным.
Пар, находящийся при давлении ниже насыщенного, называют ненасыщенным.
Вследствие постоянного испарения воды с поверхностей водоемов, почвы и растительного покрова, а также дыхания человека и животных в атмосфере всегда содержится водяной пар. Поэтому атмосферное давление представляет собой сумму давления сухого воздуха и находящегося в нем водяного пара. Давление водяного пара будет максимальным при насыщении воздуха паром. Насыщенный пар в отличие от ненасыщенного не подчиняется законам идеального газа. Так, давление насыщенного пара не зависит от объема, но зависит от температуры.
Под влажностью воздуха понимается содержание водяных паров в воздухе. (За год на Земле испаряется 4,25∙1014т Н20)
1. Абсолютную влажность измеряют как плотность водяного пара, выраженную в килограммах на метр кубический (ρ).
2. Большинство явлений, наблюдаемых в природе, например быстрота испарения, высыхание различных веществ, увядание растений, зависит не от количества водяного пара в воздухе, а от того, насколько это количество близко к насыщению, т. е. от относительной влажности, которая характеризует степень насыщения воздуха водяным паром.
Относительная влажность показывает, сколько процентов составляет абсолютная влажность от необходимой для насыщения воздуха при данной температуре:
3. Температура, при которой воздух в процессе своего охлаждения становится насыщенным водяными парами, наз. точкой росы. При достижении точки росы в воздухе или на предметах, с которыми он соприкасается, начинается конденсация водяного пара. Для определения влажности воздуха используются приборы, которые называются гигрометрами и психрометрами. Психрометр состоит из двух термометров — сухого и влажного. Влажный термометр показывает температуру ниже, чем сухой, так как его резервуар обмотан тканью, смоченной в воде, которая, испаряясь, охлаждает его. Интенсивность испарения зависит от относительной влажности воздуха. По показаниям сухого и влажного термометров находят относительную влажность воздуха по психрометрическим таблицам.

Гигрометр — от греч.Hygros -влажный.

Психрометр — от греч. Psychros — холодный + Metreo — измеряю
Относительная влажность воздуха — важный экологический показатель среды. При слишком низкой или слишком высокой влажности наблюдается быстрая утомляемость человека, ухудшение восприятия и памяти. Оптимальная влажность в квартире по ГОСТу должна быть равной 30–45%, не превышая отметки в 60%.
Влажность учитывается в метеорологии, при хранении продуктов и материалов, в хранении произведений искусств и т.д.
11. Работа в термодинамике, внутренняя энергия, первый закон термодинамики, адиабатный процесс, второй закон термодинамики.
В термодинамике рассматривается перемещение частиц макроскопического тела относительно друг друга. При совершении работы меняется объем тела. Скорость самого тела остается равной нулю, но скорости
 Рис. 1. A’ = p∆V
Рис. 1. A’ = p∆V
молекул тела меняются! Поэтому меняется и температура тела. Причина в том, что при столкновении с движущимся поршнем (сжатие газа) кинетическая энергия молекул изменяется — поршень отдает часть своей механической энергии. При столкновении с удаляющимся поршнем (расширение) скорости молекул уменьшаются, газ охлаждается. При совершении работы в термодинамике меняется состояние макроскопических тел: их объем и температура.
Газ, находящийся в сосуде под поршнем, действует на поршень с силой F’ = pS, где p — давление газа, S — площадь поршня. Если при этом поршень перемещается, то газ совершает работу. Предположим, что газ расширяется при постоянном давлении p. Тогда сила F’, с которой газ действует на поршень, также постоянна. Пусть поршень переместился на расстояние ∆x (рис.1). Работа газа равна: A’ = F’ ∆x = pS∆x = p∆V. – работа газа при изобарном расширении. Если V1 и V2 — начальный и конечный объём газа, то для работы газа имеем: A’ = p(V2 − V1). При расширении работа газа положительна. При сжатии — отрицательна. Таким образом: A’ = pΔV — работа газа. A= — pΔV — работа внешних сил.
 Работа т/д сист. при изобарном процессе
Работа т/д сист. при изобарном процессе
В изобарном процессе площадь под графиком в координатах p,V численно равна работе (рис. 2). Внешняя работа над системой равна работе системы, но с противоположным знаком А = — А’.
В изохорном процессе объем не меняется, следовательно, в изохорном процессе работа не совершается! A=0
Любое тело (газ, жидкость или твердое) обладает энергией, даже если тело не имеет скорости и находится на Земле. Эта энергия называется внутренней, обусловлена она хаотическим (тепловым) движением и взаимодействием частиц, из которых состоит тело. Внутренняя энергия состоит из кинетической и потенциальной энергии частиц поступательного и колебательного движений микрочастиц системы. Внутренняя энергия одноатомного идеального газа определяется по формуле: 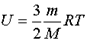 Внутренняя энергия тела может изменяться только в результате его взаимодействия с другими телами. Существует два способа изменения внутренней энергии: теплопередача и совершение механической работы (например, нагревание при трении или при сжатии, охлаждение при расширении).
Внутренняя энергия тела может изменяться только в результате его взаимодействия с другими телами. Существует два способа изменения внутренней энергии: теплопередача и совершение механической работы (например, нагревание при трении или при сжатии, охлаждение при расширении).
Теплопередача — это изменение внутренней энергии без совершения работы: энергия передается от более нагретых тел к менее нагретым телам. Теплопередача бывает трех видов: теплопроводность (непосредственный обмен энергией между хаотически движущимися частицами взаимодействующих тел или частей одного и того же тела); конвекция (перенос энергии потоками жидкости или газа) и излучение (перенос энергии электромагнитными волнами). Мерой переданной энергии при теплопередаче является количество теплоты (Q).
Эти способы количественно объединены в закон сохранения энергии, который для тепловых процессов читается так: изменение внутренней энергии замкнутой системы равно сумме количества теплоты, переданной системе, и работы внешних сил, совершенной над системой.  , где ΔU — изменение внутренней энергии, Q — количество теплоты, переданное системе, А — работа внешних сил. Если система сама совершает работу, то ее условно обозначают А’. Тогда закон сохранения энергии для тепловых процессов, который называется первым законом термодинамики, можно записать так:
, где ΔU — изменение внутренней энергии, Q — количество теплоты, переданное системе, А — работа внешних сил. Если система сама совершает работу, то ее условно обозначают А’. Тогда закон сохранения энергии для тепловых процессов, который называется первым законом термодинамики, можно записать так: 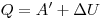 (количество теплоты, переданное системе, идет на совершение системой работы и изменение ее внутренней энергии).
(количество теплоты, переданное системе, идет на совершение системой работы и изменение ее внутренней энергии).
Рассмотрим применение первого закона термодинамики к изопроцессам, происходящим с идеальным газом.
В изотермическом процессе температура постоянная, следовательно, внутренняя энергия не меняется. Тогда уравнение I закона термодинамики примет вид: Q = А’, т. е. количество теплоты, переданное системе, идет на совершение работы при изотермическом расширении, именно поэтому температура не изменяется.
В изобарном процессе газ расширяется и количество теплоты, переданное газу, идет на увеличение его внутренней энергии и на совершение им работы: Q = ΔU +А’
При изохорном процессе газ не меняет своего объема, следовательно, работа им не совершается, т. е. А = 0. Уравнение I закона имеет вид Q = ΔU (переданное количество теплоты идет на увеличение внутренней энергии газа).
Адиабатным называют процесс, протекающий без теплообмена с окружающими телами. Пример теплоизолированного сосуда — термос. При адиабатном процессе Q = 0, следовательно, газ при расширении совершает работу за счет уменьшения его внутренней энергии, следовательно, газ охлаждается, А’= — ΔU. Если заставить газ совершить достаточно большую работу, то охладить его можно очень сильно. Именно на этом основаны методы сжижения газов. И наоборот, в процессе адиабатного сжатия будет А’ < 0, поэтому ∆U > 0: газ нагревается. Адиабатное нагревание воздуха используется в дизельных двигателях для воспламенения топлива
 |
Практически все реальные процессы происходят с теплообменом: адиабатические процессы — это редкое исключение.
Наглядные примеры адиабатных процессов:
1. В закрытом пробкой с продетым шлангом насоса сосуде находится капельки воды. После нагнетания в сосуд определенно количества воздуха, пробка быстро вылетает и в сосуде наблюдается туман (рис.).
2. В закрытом подвижным поршнем цилиндре находится небольшое количество топлива. После быстрого нажатия на поршень топливо воспламеняется.
12. Взаимодействие заряженных частиц, закон Кулона, закон сохранения электрического заряда, электрическое поле.
 Электрический заряд — физическая величина, определяющая интенсивность электромагнитных взаимодействий.
Электрический заряд — физическая величина, определяющая интенсивность электромагнитных взаимодействий.
Носителями отрицательных зарядов в атоме являются электроны, носителями положительных зарядов — протоны.
Все тела в обычном состоянии не заряжены. Чтобы тело получило заряд, его нужно наэлектризовать: отделить отрицательный заряд от связанного с ним положительного. Простейший способ электризации – трение.
При электризации тел трением происходит перераспределение имеющихся электронов между нейтральными, в первый момент телами, т.е в теле возникает избыток или недостаток электронов. При этом новые частицы не возникают, а существовавшие ранее не исчезают.
При электризации тел выполняется закон сохранения электрического заряда. Он справедлив для изолированной системы. В изолированной системе алгебраическая сумма зарядов всех частиц сохраняется:
q1 + q2 + q3 + … + qn = const
В природе существует только два вида электрических зарядов: положительные и отрицательные. Одноимённые заряды отталкиваются, разноимённые – притягиваются: 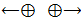

Взаимодействие между заряженными частицами называется электромагнитным.
Неподвижные точечные электрические заряды q1 и q2 взаимодействуют в вакууме согласно закону Кулона с силой 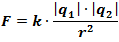 где коэффициент
где коэффициент 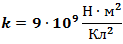 , q — заряд выражается в кулонах (Кл), r — расстояние между заряженными телами (м).
, q — заряд выражается в кулонах (Кл), r — расстояние между заряженными телами (м).
Сила взаимодействия двух точечных неподвижных заряженных тел в вакууме прямо пропорциональна произведению модулей этих зарядов и обратно пропорциональна квадрату расстояния между ними. Это основной закон электростатики Шарлем Кулоном был экспериментально установлен в 1785 г. и носит его имя.
Существует минимальный заряд, называемый элементарным, которым обладают все заряженные элементарные частицы: 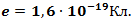
Взаимодействие зарядов осуществляется посредством электрического поля. Электрическим полем называют вид материи, посредством которой происходит взаимодействие электрических зарядов. Поле неподвижных зарядов называется электростатическим.
Свойства электрического поля:
· порождается электрическим зарядом;
· обнаруживается по действию на ток;
· действует на заряды с некоторой силой.
Напряженность поля определяет силу, действующую на заряд: 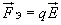
Напряженность — силовая характеристика электрического поля..
Напряженность — векторная физическая величина, численно равная отношению силы, действующей на заряд, помещенный в данную точку поля, к величине этого заряда. 
 |
,
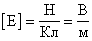 Напряженность не зависит от величины заряда, помещенного в поле.
Напряженность не зависит от величины заряда, помещенного в поле. 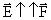 , если q>0.
, если q>0. 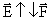 , если q<0. Т.е. вектор напряженности направлен от положительного заряда и к отрицательному.
, если q<0. Т.е. вектор напряженности направлен от положительного заряда и к отрицательному.
Напряженность полей, созданных отдельными зарядами, складываются геометрически (принцип суперпозиции): 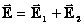 . Поле можно представить при помощи линий напряженности (силовых линий).
. Поле можно представить при помощи линий напряженности (силовых линий).
13. Конденсаторы, электроемкость конденсаторов, энергия заряженного конденсатора, применение конденсаторов.
 Электроемкость — это скалярная величина, характеризующая способность проводника накапливать электрический заряд.
Электроемкость — это скалярная величина, характеризующая способность проводника накапливать электрический заряд.
Электроемкость
— не зависит от q и U;
— зависит от геометрических размеров проводника, их формы, взаимного расположения, электрических свойств среды между проводниками.
Электрической емкостью проводника наз. отношение заряда проводника к его потенциалу: 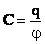 .
.
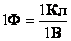 единица измерения емкости в СИ: Ф (фарад)
единица измерения емкости в СИ: Ф (фарад)
Конденсатор обладает свойством накапливать и сохранять электрическую энергию.
Конденсатор представляет собой систему из двух проводников, разделенных слоем диэлектрика, толщина которого мала по сравнению с размерами проводников. Проводники наз. обкладками конденсатора. Если заряды пластин конденсатора одинаковы по модулю и противоположны по знаку, то под зарядом конденсатора понимают абсолютное значение заряда одной из его обкладок.
Электроемкостью конденсатора называют отношение заряда конденсатора к разности потенциалов между обкладками: 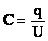
 Обозначение на электрических схемах:
Обозначение на электрических схемах:
Все электрическое поле сосредоточено внутри конденсатора.
Заряд конденсатора — это абсолютное значение заряда одной из обкладок конденсатора.
Виды конденсаторов:
1. по виду диэлектрика — воздушные, слюдяные, керамические, электролитические
2. по форме обкладок — плоские, сферические.
3. по величине емкости — постоянные, переменные (подстроечные). 
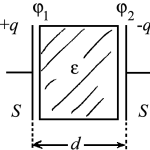 Электроемкость плоского конденсатора
Электроемкость плоского конденсатора 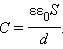
где S — площадь пластины (обкладки) конденсатора
d — расстояние между пластинами
εо — электрическая постоянная
ε — диэлектрическая проницаемость диэлектрика
Конденсатор — это система заряженных тел обладает энергией.
Энергия любого конденсатора: 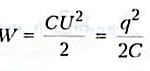
где С — емкость конденсатора, (Ф) W— энергия (Дж)
q — заряд конденсатора, (Кл)
U — напряжение на обкладках конденсатора, (В)
Энергия конденсатора равна работе, которую совершит электрическое поле при сближении пластин конденсатора вплотную, или работе по разделению положительных и отрицательных зарядов необходимой при зарядке конденсатора.
Конденсаторы применяются для накопления электрической энергии и использования ее при быстром разряде (фотовспышка), для разделения цепей постоянного и переменного тока, в радиотехнике: колебательный контур, выпрямитель и других радиоэлектронных устройствах.
14. Электрический ток, работа и мощность в цепи постоянного тока, закон Ома для полной цепи.
Цепи
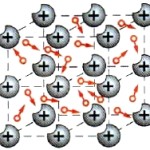 Кристаллическая решётка
Кристаллическая решётка
Электрический ток. Все металлы являются проводниками электрического тока. Они состоят из пространственной кристаллической решетки, узлы которой совпадают с центрами положительных ионов. Вокруг ионов хаотически движутся свободные электроны.
В металлах электронная проводимость
Электрическим током в металлах называется упорядоченное движение свободных электронов. За направление тока принимают направление движения положительно заряженных частиц.
Электрические заряды могут двигаться упорядоченно под действием электрического поля, поэтому условием для существования эл. тока является налич
|
|
|


