 |
Тема : Способы выражения состава растворов. Приготовление растворов.
|
|
|
|
Министерство здравоохранения и социального развития Российской Федерации
Государственное бюджетное образовательное учреждение высшего профессионального образования
ПЕРВЫЙ МОСКОВСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ
УНИВЕРСИТЕТ имени И.М. СЕЧЕНОВА

ОБУЧАЮЩАЯ ЛАБОРАТОРНАЯ ТЕТРАДЬ
ПО КУРСУ ОБЩЕЙ ХИМИИ

СТУДЕНТА_____________________ ГРУППЫ
__________________________ФАКУЛЬТЕТА
__________________________ОТДЕЛЕНИЯ
ФАМИЛИЯ _____________________________
ИМЯ ___________________________________
ОТЧЕСТВО _____________________________
ПРЕПОДАВАТЕЛЬ ______________________
Учебный год
Москва
ОСНОВНЫЕ ПРАВИЛА РАБОТЫ В ХИМИЧЕСКОЙ ЛАБОРАТОРИИ
И ТЕХНИКА ВЫПОЛНЕНИЯ ХИМИЧЕСКОГО ЭКСПЕРИМЕНТА
Правила поведения в химической лаборатории и технику безопасности:
ü к эксперименту приступают только после ознакомления со всеми его этапами;
ü на лабораторном столе должны находиться только необходимые для эксперимента приборы, оборудование лабораторный журнал;
ü в лаборатории работают только в халате;
ü нельзя брать руками вещества и пробовать их на вкус;
ü опыты с ядовитыми и летучими веществами, концентрированными растворами кислот и щелочей проводят под тягой;
ü при приливании реактивов нельзя наклоняться над отверстием сосуда во избежание попадания брызг на лицо и одежду;
ü нельзя работать с легковоспламеняющимися жидкостями вблизи включенных электрических и нагревательных приборов;
ü нельзя выливать в раковину остатки кислот, щелочей и огнеопасных веществ их следует сливать в специально предназначенные для этого склянки;
ü для засасывания кислот и щелочей в пипетку пользуются резиновыми грушами;
|
|
|
ü разбавляя концентрированные кислоты, осторожно вливают кислоту в воду, а не наоборот.
При несоблюдении правил техники безопасности в лаборатории, бывают несчастные случаи, требующие первой неотложной помощи, для ее оказания в лаборатории должна быть аптечка. Основные правила скорой помощи следующие:
- при термическом ожоге кожу обрабатывают спиртом или свежеприготовленным раствором перманганата калия, а затем смазывают мазью от ожогов или присыпают танином;
- при химических ожогах глаз обильно промывают глаза водой, используя глазную ванночку, после этого следует обратиться к врачу;
- при ожогах кислотой необходимо омыть реактив большим количеством воды, затем обработать кожу растворам соды;
- при ожогах щелочью необходимо смыть реактив большим количеством воды, затем промыть участок кожи разбавленной уксусной кислотой, а затем снова водой.
Прежде чем приступить к эксперименту, студенты должны изучить соответствующий раздел учебника, лекций, а также ознакомиться с описанием работы и ответить на вопросы для самоподготовки.
С правилами поведения в химической лаборатории и техникой безопасности ознакомилась(ся)
Фамилия _____________________ Имя_________________ Отчество _______________________
Дата: Подпись:
_____._____20____ ____________________
Занятие 1. Дата ____.____. 20 ___
Тема: Способы выражения состава растворов. Приготовление растворов.
Теоретический материал к занятию:
Эквивалент – это реальная или условная частица вещества Х, которая в данной кислотно-основной реакции эквивалентна одному иону водорода или в данной окислительно-восстановительной реакции одному электрону.
Массовая доля растворенного вещества 
Х – растворенное вещество
Молярная концентрация, 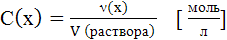
Молярная концентрация эквивалента 
Фактор эквивалентности, 
Молярная масса эквивалента, 
|
|
|
Плотность раствор, 
Моляльная концентрация, 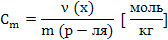
Формулы перехода от одних способов выражения состава раствора к другим
| Обозначение | w (Х) | с(Х) | сm(X) |
| Массовая доля w (Х) | w | с(Х) М(Х) 1000 r | ____с(Х) М(Х)______ 1000 + с(Х) М(Х) |
| Молярная концентрация с(Х), моль/л | w(Х) r 1000 М(Х) | с | сm(X) r 1000 1000 + сm(Х)М(Х) |
| Моляльная концентрация сm(X), моль/л | 1000 w(Х)__ (1 - w(Х)) М(Х) | ___1000 с(Х)__ 1000r - с(Х)М(Х) | сm |
Задача.
Какой объем соляной кислоты ( ρ =1,070 г/мл) и воды необходим для приготовления раствора HCl объемом 200 мл и молярной концентрацией 0,1 моль/л для кислотно-основного титрования натрия тетрабората.
| Дано | Решение |
| V (р-р) =200 мл = 0,2 л С (HCl) = 0,1 моль/л ρ (р-р) = 1,07 г/мл М (HCl) = 36,5 г/моль _____________________ m (р-р HCl) и V (H2O) =? | 1. Объем исходного раствора соляной кислоты можно рассчитать по формуле
 (m (р-р HCl) – неизвестна)
(m (р-р HCl) – неизвестна)
|
2. Массу исходного раствора HCl можно рассчитать по формуле:
m (p-p HCl) = m (HCl) / V (HCl) (m (HCl) и V (HCl) – неизвестны)
3. Массовую долю ω можно найти в справочнике, зная плотность ρ исходного раствора HCl. Массу HCl можно рассчитать зная молярную массу вещества и количество вещества
m (HCl) = M (HCl) · n (HCl) (n (HCl) – неизвестно)
4. Количество вещества HCl можно рассчитать зная объем раствора и его концентрацию
n (HCl) = V (p-p) · C(HCl) (обе величины даны в условии задачи)
4.1 n (HCl) = 0,2 л · 0,1 моль/л = 0,02 моль
4.2 m (HCl) = 36,5 г/моль · 0,02 моль = 0,73 г
4.3 ω (%) = 14% или ω (в долях) = 0,14 (по таблице №14)
4.4 m (p-p HCl) = 0,73 г / 0,14 = 5,2 г
4.5 V (р-р HCl) = 5,2 г / 1,07 г/мл = 5мл
4.6 V(H2О) = 200 мл - 5 мл = 195 мл
|
|
|


