 |
13.5. Второе начало термодинамики. Термодинамические потенциалы
|
|
|
|
13. 5. Второе начало термодинамики. Термодинамические потенциалы
13. 5. 1. Второе начало термодинамики
Как показал человеческий опыт, первого начала термодинамики недостаточно для того, чтобы объяснить своеобразие различных явлений в природе.
На основании первого начала термодинамики, внутренняя энергия системы может изменяться только в результате совершения работы или передачи некоторого количества теплоты. Работа может совершаться или внешними силами, действующими на систему, или системой над внешними силами. Количество теплоты либо передается от каких-либо тел, не входящих в систему, либо отбираться от самой системы внешними телами. Следовательно, в изолированной системе внутренняя энергия не изменяется.
В различных термодинамических системах можно представить различные процессы. Первое начало термодинамики позволяет выбрать из многообразия процессов такие, которые с точки зрения энергетических соотношений возможны. Однако оно не дает способа различия, какие процессы в действительности возможны, а какие нет.
Так, например, при смешении двух порций жидкости с разной температурой с точки зрения первого начала термодинамики возможен любой процесс, в результате которого температура смеси установится и будет равна t, при этом должно выполняться соотношение
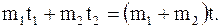 (13. 58)
(13. 58)
В то же самое время, возможен и такой процесс, при котором жидкость массой (m1 + m2), имеющая температуру t, самопроизвольно разделится на две порции массами m1 и m2 с различными температурами t1 и t2, при этом будет выполняться соотношение:
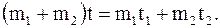 (13. 59)
(13. 59)
Однако в действительности последний процесс невозможен.
|
|
|
Точно также при смешении водного раствора какой-либо соли с чистой водой всегда наблюдается диффузия, которая приводит к выравниванию концентрации раствора во всей жидкости. Однако, никогда не наблюдается, чтобы растворенное в какой-либо жидкости вещество (соль) самопроизвольно собралось бы в одной ее части, в то время как во второй части оказался бы чистый растворитель.
Таким образом, возможные с точки зрения первого начала термодинамики процессы оказываются неравноценными в отношении их протекания: одни из них возможны, а другие нет.
На различие таких процессов и указывает второе начало термодинамики, которое можно сформулировать так: " В изолированной системе возможны только такие процессы, при которых энтропия системы возрастает". Т. е.
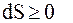 или
или 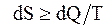 . (13. 60)
. (13. 60)
Следовательно, чтобы ответить на вопрос, возможен ли в изолированной системе тот или иной процесс, необходимо рассчитать изменение энтропии системы, которым сопровождается этот процесс и если оно положительно, то данный процесс возможен, если отрицательно - нет.
Формулировок второго начала термодинамики несколько, но все они приводят к одним и тем же выводам: " В изолированной системе при всех реальных процессах энтропия возрастает. Или невозможен процесс, единственным результатом которого является превращение в работу теплоты, полученной от нагревателя".
Таким образом, второе начало термодинамики определяет направление термодинамических процессов и указывает на физический смысл энтропии: энтропия - мера рассеяния энергии, т. е. характеризует ту часть энергии, которую нельзя превратить в работу.
Надо отметить, что вывод о невозможность превращения всего тепла, полученного от нагревателя, в работу справедлив не только для тепловой машины, работающей по циклу Карно, но и для тепловой машины, работающей по любому циклическому принципу. Это связано с тем, что любой произвольный замкнутый процесс (цикл) можно представить в виде элементарных циклов Карно. Для каждого элементарного цикла справедливо соотношение
|
|
|
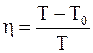 =
= 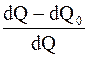 .
.
Откуда 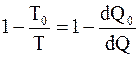 , или
, или 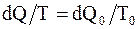 т. е.
т. е.  , следовательно,
, следовательно,  и
и 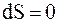 .
.
Таким образом, энтропия S системы это однозначная функция ее состояния. Приращение (изменение) энтропии не зависит от характера и последовательности процессов при переходе системы из одного состояния в другое, а определяется лишь исходным и конечным состояниями. С другой стороны в каждом элементарном цикле Карно некоторое количество тепла 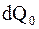 передается холодильнику. Таким образом, тепловая машина, работающая по любому циклическому принципу, не может полностью превратить получаемое от нагревателя тепло в работу.
передается холодильнику. Таким образом, тепловая машина, работающая по любому циклическому принципу, не может полностью превратить получаемое от нагревателя тепло в работу.
Принято называть тепловую машину, которая была бы в состоянии полностью превратить получаемое от нагревателя тепло в полезную работу, вечным двигателем второго рода.
На основании вышеизложенного, можно сделать вывод о том, что любая конструкция, реализующая вечный двигатель второго рода, нереалистична.
|
|
|


