 |
Ответом к заданиям В9, В10 является число. Запишите это число в текст работы, а затем перенесите его в бланк ответов № 1 без указания единиц измерения.
|
|
|
|
Единый государственный экзамен по ХИМИИ
Демонстрационный вариант 2005 г.
Инструкция по выполнению работы
На выполнение экзаменационной работы по химии дается 3 часа (180 минут). Работа состоит из 3 частей и включает 50 заданий.
Часть 1 включает 35 заданий (А1 – А35). К каждому заданию дается 4 варианта ответа, из которых только один правильный.
Часть 2 состоит из 10 заданий (В1 – В10), на которые надо дать краткий ответ в виде числа или последовательности букв. В этой части используются задания на установление соответствия, на выбор нескольких правильных ответов из предложенных, а также расчетные задачи.
Часть 3 содержит 5 самых сложных заданий по общей, неорганической и органической химии. Задания C1 – C5 требуют полного (развернутого) ответа.
Внимательно прочитайте каждое задание и предлагаемые варианты ответа, если они имеются. Отвечайте только после того, как вы поняли вопрос и проанализировали все варианты ответа.
Выполняйте задания в том порядке, в котором они даны. Для экономии времени пропускайте задание, которое не удается выполнить сразу, и переходите к следующему. К пропущенному заданию вы сможете вернуться после выполнения всей работы, если останется время.
При выполнении работы вы можете пользоваться периодической системой химических элементов Д.И. Менделеева, таблицей растворимости солей, кислот и оснований в воде, электрохимическим рядом напряжений металлов (они прилагаются к тексту работы), а также непрограммируемым калькулятором, который выдается на экзамене.
За выполнение различных по сложности заданий дается один или более баллов. Баллы, полученные вами за выполненные задания, суммируются. Постарайтесь выполнить как можно больше заданий и набрать наибольшее количество баллов.
|
|
|
Желаем успеха!
Часть 1
При выполнении заданий этой части в бланке ответов № 1 под номером выполняемого вами задания (А1 – А35) поставьте знак « ´ » в клеточку, номер которой соответствует номеру выбранного вами ответа.
| A1 |
У атома серы число электронов на внешнем энергетическом уровне и заряд ядра равны соответственно
| 1) | 4 и + 16 | 2) | 6 и + 32 | 3) | 6 и + 16 | 4) | 4 и + 32 |
| A2 |
B главных подгруппах периодической системы восстановительная способность атомов химических элементов растет c
| 1) | увеличением числа энергетических уровней в атомах |
| 2) | уменьшением радиуса атомов |
| 3) | уменьшением числа протонов в ядрах атомов |
| 4) | увеличением числа валентных электронов |
| A3 |
Соединениями с ковалентной полярной и ковалентной неполярной связью являются соответственно
| 1) | вода и сероводород |
| 2) | бромид калия и азот |
| 3) | аммиак и водород |
| 4) | кислород и метан |
| A4 |
Степень окисления азота в ионе NН4+ равна
| 1) | – 1 | 2) | – 3 | 3) | + 3 | 4) | + 5 |
| A5 |
Атомную кристаллическую решетку имеет каждое из двух веществ:
| 1) | оксид кремния (IV) и оксид углерода (IV) |
| 2) | алмаз и кремний |
| 3) | хлор и иод |
| 4) | хлорид калия и фторид железа (III) |
| A6 |
К основным оксидам относится
| 1) | ZnO | 2) | SiO2 | 3) | BaO | 4) | Al2O3 |
| A7 |
В ряду натрий – магний – алюминий
элементы расположены в порядке увеличения
| 1) | атомного радиуса |
| 2) | электроотрицательности |
| 3) | металлических свойств |
| 4) | числа энергетических уровней |
| A8 |
Какой из металлов не вытесняет водород из разбавленной серной кислоты?
| 1) | железо | 2) | хром | 3) | медь | 4) | цинк |
| A9 |
Оксиды с общей формулой R2O3 и R2O5 образуют элементы подгруппы
|
|
|
| 1) | углерода | 2) | азота | 3) | серы | 4) | фтора |
| A10 |
Наиболее энергично реагирует с водой
| 1) | Al | 2) | Mg | 3) | Ca | 4) | К |
| A11 |
Bодород проявляет свойства окислителя при взаимодействии с
| 1) | кислородом |
| 2) | азотом |
| 3) | кальцием |
| 4) | хлором |
| A12 |
При нагревании оксида железа (II) с оксидом углерода (II) образуются углекислый газ и
| 1) | Fe | 2) | FeO | 3) | Fe2O3 | 4) | Fe3O4 |
| A13 |
При нагревании гидроксида меди (II) образуются
| 1) | Cu и H2O | 2) | СuO и Н2 | 3) | CuO и Н2О | 4) | Сu2O и Н2О |
| A14 |
Хлороводородная (соляная) кислота реагирует с
| 1) | Сu | 2) | Hg | 3) | Ag | 4) | Zn |
| A15 |
Соль и щелочь образуются при взаимодействии растворов
| 1) | K2CO3 и Ba(OH)2 |
| 2) | AlCl3 и NaOH |
| 3) | H3PO4 и KOH |
| 4) | MgBr2 и Na3PO4 |
| A16 |
В схеме превращений
Al(OH)3  X
X  Al(OH)3
Al(OH)3
веществами «А» и «В» могут быть соответственно
| 1) | K2SO4 и KOH |
| 2) | NaCl и HCl |
| 3) | Na2SO4 и H2SO4 |
| 4) | HNO3 и NaOH |
| A17 |
Какой вид изомерии нехарактерен для спирта, формула которого C5H11OH?
| 1) | углеродного скелета |
| 2) | положения гидроксильной группы |
| 3) | межклассовая |
| 4) | положения кратной связи |
| A18 |
К соединениям, имеющим общую формулу СnH2n, относится
| 1) | бензол | 2) | циклогексан | 3) | гексан | 4) | гексин |
| A19 |
B молекуле ацетилена имеются
| 1) | две s- и две p-связи |
| 2) | две s- и три p-связи |
| 3) | три s- и одна p-связь |
| 4) | три s- и две p-связи |
| A20 |
Фенол взаимодействует с
| 1) | соляной кислотой |
| 2) | гидроксидом натрия |
| 3) | этиленом |
| 4) | метаном |
| A21 |
Уксусный альдегид реагирует с каждым из двух веществ:
| 1) | аммиачным раствором оксида серебра (I) и кислородом |
| 2) | гидроксидом меди (II) и оксидом кальция |
| 3) | соляной кислотой и серебром |
| 4) | гидроксидом натрия и водородом |
| A22 |
При взаимодействии карбоновых кислот и спиртов образуются
| 1) | простые эфиры |
| 2) | сложные эфиры |
| 3) | углеводы |
| 4) | аминокислоты |
| A23 |
Реакция, уравнение которой
Zn(OН)2 + H2SO4 = ZnSO4 + 2H2O,
относится к реакциям
| 1) | обмена | 2) | соединения | 3) | разложения | 4) | замещения |
|
|
|
| A24 |
Для увеличения скорости взаимодействия железа с хлороводородной (соляной) кислотой следует
| 1) | добавить ингибитор |
| 2) | понизить температуру |
| 3) | повысить давление |
| 4) | увеличить концентрацию НС1 |
| A25 |
Изменение давления смещает равновесие в системе
| 1) | 3H2(г) + N2(г)  2NH3(г) 2NH3(г)
|
| 2) | H2(г) + S(тв)  H2S(г) H2S(г)
|
| 3) | N2(г) + O2(г)  2NO(г) 2NO(г)
|
| 4) | H2(г) + Cl2(г)  2HCl(г) 2HCl(г)
|
| A26 |
Степень диссоциации уксусной кислоты в водном растворе увеличится, если
| 1) | интенсивно перемешать этот раствор |
| 2) | добавить в раствор CH3COONa |
| 3) | разбавить раствор CH3COOH водой |
| 4) | увеличить концентрацию CH3COOH |
| A27 |
Сокращенное ионное уравнение
Fe2+ + 2OH– = Fe(OH)2
соответствует взаимодействию веществ:
| 1) | Fe(NO3)3 и KOH |
| 2) | FeSO4 и LiOH |
| 3) | Na2S и Fe(NO3)2 |
| 4) | Ba(OH)2 и FeCl3 |
| A28 |
В реакции, уравнение которой
3P + 5HNO3 + 2H2O = 3H3PO4 + 5NO,
фосфор
| 1) | окисляется |
| 2) | восстанавливается |
| 3) | принимает электроны |
| 4) | не изменяет степень окисления |
| A29 |
Среда раствора карбоната калия
| 1) | щелочная |
| 2) | кислая |
| 3) | нейтральная |
| 4) | слабокислая |
| A30 |
И бутан, и бутилен реагируют с
| 1) | бромной водой |
| 2) | раствором KMnO4 |
| 3) | водородом |
| 4) | хлором |
| A31 |
Для получения уксусной кислоты в одну стадию используют
| 1) | гидролиз карбида кальция |
| 2) | гидратацию этилена |
| 3) | окисление формальдегида |
| 4) | окисление ацетальдегида |
| A32 |
Аминокислоты не реагируют ни с одним из двух веществ:
| 1) | NaOH и CH3OH |
| 2) | CH3NH2 и Na |
| 3) | NaCl и CH4 |
| 4) | NH3 и H2O |
| A33 |
Сильными антисептическими свойствами обладает
| 1) | этановая кислота |
| 2) | раствор фенола |
| 3) | диметиловый эфир |
| 4) | бензол |
| A34 |
Полипропилен получают из вещества, формула которого
| 1) | СН2 = СН2 |
| 2) | СН º СН |
| 3) | СН3 – СН2 – СН3 |
| 4) | СН2 = СН – СН3 |
| A35 |
В результате реакции, термохимическое уравнение которой
|
|
|
С2H5OH + 3O2  2CO2 + 3H2O + 1374 кДж,
2CO2 + 3H2O + 1374 кДж,
выделилось 687 кДж теплоты. Количество вещества этанола равно
| 1) | 0,5 моль | 2) | 1 моль | 3) | 1,5 моль | 4) | 2 моль |
Часть 2
Ответом к заданиям этой части (В1 – В10) является набор букв или число, которые следует записать в бланк ответов № 1 справа от номера соответствующего задания, начиная с первой клеточки. Каждую букву, цифру и запятую в записи десятичной дроби пишите в отдельной клеточке в соответствии с приведенными в бланке образцами.
В заданиях В1 – В5 на установление соответствия запишите в таблицу буквы выбранных вами ответов, а затем получившуюся последовательность букв перенесите в бланк ответов № 1 без пробелов и других символов. (Буквы в ответе могут повторяться.)
| B1 |
Установите соответствие между названием вещества и классом (группой) веществ, к которому(-ой) оно принадлежит.
| ВЕЩЕСТВО | КЛАСС (ГРУППА) ВЕЩЕСТВ | ||
| 1) | гидроксид хрома (VI) | A) | кислая соль |
| 2) | гидросульфат кальция | Б) | основание |
| 3) | хлорат калия | в) | амфотерный гидроксид |
| 4) | гидроксид хрома (III) | г) | кислота |
| Д) | средняя соль |
| B2 |
Установите соответствие между исходными веществами и продуктами, которые преимущественно образуются в ходе реакций.
| ИСХОДНЫЕ BЕЩЕСТBА | ПРОДУКТЫ РЕАКЦИИ | ||
| 1) | Fe + Cl2 
| А) | FeCl2 |
| 2) | Fe + HCl 
| Б) | FeCl3 |
| 3) | Cu + HNO3(конц.) 
| B) | FeCl2 + H2 |
| 4) | Cu + HNO3(разб.) 
| Г) | Cu(NO3)2 + H2 |
| Д) | Cu(NO3)2 + NO+ H2O | ||
| Е) | Cu(NO3)2 + NO2+ H2O |
| B3 |
Установите соответствие между исходными веществами, вступающими в реакции обмена, и сокращенными ионными уравнениями этих реакций.
| ИСХОДНЫЕ BЕЩЕСТBА | СОКРАЩЕННЫЕ ИОННЫЕ УРАBНЕНИЯ | ||
| 1) | H2SO4 и BaCl2 | А) | Al3+ + 3OH– = Al(OH)3 |
| 2) | Ba(OH)2 и K2CO3 | Б) | Ba2+ + SO42– = BaSO4 |
| 3) | Al(NO3)3 и KOH | B) | Na+ + Br – = NaBr |
| 4) | BaBr2 и Na2SO4 | Г) | Ba2+ + CO32– = BaCO3 |
| Д) | К+ + NO3– = KNO3 |
| B4 |
Установите соответствие между уравнением реакции и веществом-окислителем, участвующим в данной реакции.
| УРАВНЕНИЕ РЕАКЦИИ | ОКИСЛИТЕЛЬ | ||
| 1) | 2NO + 2H2 = N2 + 2H2O | А) | H2 |
| 2) | 2NH3 + 2Na = 2NaNH2 + H2 | Б) | N2 |
| 3) | H2 + 2Na = 2NaH | В) | NO |
| 4) | 4NH3 + 6NO = 5N2 + 6H2O | Г) | NH3 |
| B5 |
Установите соответствие между формулой соли и молекулярно-ионным уравнением гидролиза этой соли.
| ФОРМУЛА СОЛИ | МОЛЕКУЛЯРНО-ИОННОЕ УРАВНЕНИЕ | ||
| 1) | CuSO4 | A) | CH3COO– + H2O  CH3COOH + OH– CH3COOH + OH–
|
| 2) | K2CO3 | Б) | NH4+ + H2O  NH3×H2O + H+ NH3×H2O + H+
|
| 3) | CH3COONa | В) | Сu2+ + H2O  Cu(OH)+ + H+ Cu(OH)+ + H+
|
| 4) | (NH4)2SO4 | Г) | СO32– + H2O  HCO3– + OH– HCO3– + OH–
|
| Д) | Сu2+ + 2H2O  Cu(OH)2 + 2H+ Cu(OH)2 + 2H+
|
|
|
|
Ответом к заданиям В6 – В8 является последовательность букв. Запишите выбранные буквы в алфавитном порядке сначала в текст работы, а затем перенесите их в бланк ответов № 1 без пробелов и других символов.
| B6 |
Формальдегид взаимодействует с:
| а) | N2 |
| б) | FeCl3 |
| в) | HNO3 |
| г) | Cu(OH)2 |
| д) | CH3COOH |
| е) | [Ag(NH3)2]OH |
Ответ: _____________.
| B7 |
Глюкоза вступает в реакцию с:
| а) | NH3 |
| б) | HCl |
| в) | KOH |
| г) | Na2CO3 |
| д) | Cu(OH)2 |
| е) | [Ag(NH3)2]OH |
Ответ: _____________.
| B8 |
Реактивами на белок являются:
А) NH3∙H2O
Б) HBr
В) HNO3 (конц.)
Г) лакмус
Д) FeCl3
Е) CuSO4 + NaOH (изб.)
Ответ: _____________.
Ответом к заданиям В9, В10 является число. Запишите это число в текст работы, а затем перенесите его в бланк ответов № 1 без указания единиц измерения.
| B9 |
К 180,0 г 8%-ного раствора хлорида натрия добавили 20 г NaCl. Массовая доля хлорида натрия в образовавшемся растворе равна _____________ %. (Запишите число с точностью до десятых.)
| B10 |
При взаимодействии 10 л метана и 8 л хлора образуется хлорметан (н.у.) объемом _____________ л.
(Запишите число с точностью до целых.)
Не забудьте перенести все ответы в бланк ответов № 1
Часть 3
| Для записи ответов к заданиям этой части (С1 – С5) используйте бланк ответов № 2. Запишите сначала номер задания (С1 и т.д.), а затем полное решение. Ответы записывайте четко и разборчиво. |
| C1 |
Напишите уравнения реакций, протекающих на катоде и аноде, и общее уравнение электролиза водного раствора сульфата натрия на инертных электродах.
| C2 |
В цепочке превращений
Al  X
X  Y
Y 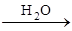 X
X  Z
Z 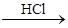 Al(OH)3
Al(OH)3
определите формулы алюминийсодержащих продуктов X, Y, Z. Напишите соответствующие уравнения реакций.
| C3 |
Напишите уравнения реакций, с помощью которых можно осуществить превращения:
 .
.
Укажите условия протекания 1, 2, 3-й реакций.
| C4 |
Газообразный аммиак, выделившийся при кипячении 160 г 7%-ного раствора гидроксида калия с 9,0 г хлорида аммония, растворили в 75 г воды. Определите массовую долю аммиака в полученном растворе.
| C5 |
При сгорании 9 г первичного амина выделилось 2,24 л азота (н.у.). Определите молекулярную формулу амина, приведите его название.
|
|
|


