 |
Задача №2.Расчёт политропного процесса сжатия газовой смеси в компрессоре.
|
|
|
|
Задача №1. Расчёт газовой смеси.
Газовая смесь состоит из нескольких компонентов, содержание которых в смеси задано в процентах по объёму: СО2 = 18%; CО = 10%; N2 = 72%.
Определить: 1)кажущуюся молекулярную массу смеси; 2) газовую постоянную смеси; 3) средние мольную, объёмную и массовую теплоёмкости смеси при постоянном давлении в пределах температур от t1 = 1260C до t2 = 5280C.
Решение:
1.Кажущаяся молекулярная масса смеси.
μСМ = ∑(ri * μi),
где μi - молекулярная масса компонентов смеси;
ri - объёмные доли компонентов смеси.
μСМ = r(СО2)*μ(СО2) + r(CO)*μ(CO) + r (N2)*μ(N2) = 0,18*44 + 0,10*28 + +0,72*28= 30,88.
2.Газовая постоянная смеси.
RСМ = R / μСМ,
где R = 8314 Дж/(кг*К) – универсальная газовая постоянная.
RСМ = 8314 / 30,88 = 269 Дж/(кг*К).
3.Перевод объёмных долей в массовые.
gi = ri * μi / (∑(ri * μi),
g(CО2) = r (СО2)*μ(СО2) /[r(СО2)*μ(СО2) + r(CO)*μ(CO) + r (N2)*μ(N2)]= =0,18*44/30,88 = 0,257;
g(CO) = r(CO)*μ(CO) /[r(СО2)*μ(СО2) + r(CO)*μ(CO) + r (N2)*μ(N2)] = =0,10*28/30,88 = 0,091;
g(N2) = r (N2)*μ(N2)/[r(СО2)*μ(СО2) + r(CO)*μ(CO) + r (N2)*μ(N2)]= =0,72*28/30,88 = 0,652.
4.Средние мольная, объёмная и массовая теплоёмкости смеси при постоянном давлении в пределах температур от t1 = 1260C до t2 = 5280C.
Средняя массовая теплоёмкость смеси при постоянном давлении:
(Cpmсм)  =(Cpmсм2*t2 - Cpmсм1*t1) / (t2 – t1);
=(Cpmсм2*t2 - Cpmсм1*t1) / (t2 – t1);
(Cpmсм1) 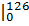 = gCO2* (CpmCO2)
= gCO2* (CpmCO2) 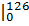 +gN2*(CpmN2)
+gN2*(CpmN2) 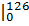 +gCO*(CpmCO)
+gCO*(CpmCO) 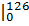 = =0,257*0,8773+ 0,652*1,0324 + 0,091*1,0429 =0,994 кДж/(кг*К);
= =0,257*0,8773+ 0,652*1,0324 + 0,091*1,0429 =0,994 кДж/(кг*К);
(Cpmсм2)  = gCO2* (CpmCO2)
= gCO2* (CpmCO2)  +gN2*(CpmN2)
+gN2*(CpmN2)  +gCO* (CpmCO)
+gCO* (CpmCO)  = =0,257*1,0203 + 0,652* 1,0598 + 0,091*1,0779 = 1,051кДж/(кг*К);
= =0,257*1,0203 + 0,652* 1,0598 + 0,091*1,0779 = 1,051кДж/(кг*К);
(Cpmсм) 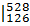 = (1,051*528 - 0,994*126)/(528 - 126) = 1,069 кДж/(кг*К).
= (1,051*528 - 0,994*126)/(528 - 126) = 1,069 кДж/(кг*К).
Средняя мольная теплоёмкость смеси при постоянном давлении:
(μCpmсм)  = (Cpmсм)
= (Cpmсм) 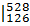 *μСМ = 1,069*30,88 = 33,011кДж/(кмоль*К).
*μСМ = 1,069*30,88 = 33,011кДж/(кмоль*К).
Средняя объёмная теплоёмкость смеси при постоянном давлении:
(C* pmсм)  = (μCpmсм)
= (μCpmсм) 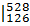 /22,4 = 33,011/22,4 = 1,474кДж/(м 3*К).
/22,4 = 33,011/22,4 = 1,474кДж/(м 3*К).
Ответы на вопросы
1.Что называется газовой постоянной? Как определяется универсальная газовая постоянная? Единицы измерения.
|
|
|
Газовая постоянная R = 8314/μ – отнесена к 1 кг конкретного газа[Дж/(кг*К)], представляет собой удельную работу изменения объема, совершаемую 1 кг рабочего тела при изменении его температуры на 1 К в изобарном процессе.
Универсальная газовая постоянная R = 8314 Дж/(кмоль*К) – отнесена к 1 кмолю - это работа изменения объема, совершаемая 1 кмолем газа при изменении его температуры на 1 К в изобарном процессе.
2.Что представляет собой массовая, объёмная и мольная теплоёмкости? Каковы единицы их измерения в системе СИ? Какова связь между указанными теплоёмкостями?
Удельная молярная теплоемкость(mС) – количество тепла, которое необходимо сообщить 1 кмолю вещества, чтобы повысить его температуру на один градус[кДж/(кмоль*К)].
Удельная массовая теплоемкость (C) – количество тепла, которое необходимо сообщить 1 кг вещества, чтобы повысить его температуру на один градус[кДж/(кг*К)].
Удельная объемная теплоемкость (С¢) -– это количество теплоты, которое необходимо подвести к 1 м3 вещества, чтобы нагреть его на один градус [кДж/(м3*К.)].
Взаимную связь массовой, объемной и мольной теплоемкостей можно выразить следующими соотношениями:
 ;
;  ;
; 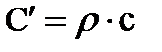
где r - плотность газа;
μ – молярная масса газа.
3.Какие факторы влияют на величину теплоёмкости?
На величину теплоёмкости влияют: температура, давление, количество вещества.
Задача №2.Расчёт политропного процесса сжатия газовой смеси в компрессоре.
Рабочее тело – газовая смесь состава в процентах по объёму: СО2 = 18%; CO = 10%; N2 = 72%. Первоначальный объём, занимаемый газовой смесью V1 = 40 м3. Начальные параметры состояния: давление Р1 = 0,1 МПа, температура t1 = 270С. Процесс сжатия происходит при показателе политропы n= 1,22. Давление смеси в конце сжатия Р2 = 0,9 МПа.
Определить: 1) массу газовой смеси; 2) удельный объём смеси в начале и в конце процесса; 3) объём, занимаемый смесью в конце процесса; 4) температуру в конце процесса; 5) работу сжатия в процессе; 6) работу, затрачиваемую на привод компрессора; 7) изменение внутренней энергии газовой смеси; 8) массовую теплоёмкость рабочего тела в данном процессе; 9) количество тепла, участвующего в процессе; 10) изменение энтропии в процессе.
|
|
|
Построить рассмотренный процесс в координатах p-v и T-s.
Решение:
1.Масса газовой смеси.
Из уравнения состояния
Mсм = P1* V1 /(Rсм*T1) = 0,1*106*40/(269*300) = 49,57 кг.
2.Объём, занимаемый смесью в конце процесса.
Из соотношения для политропного процесса
V2n = Р1*V1n/ Р2 → V21,22 = 0,1*401,22/0,9 =10,006→ V2 = 6,61 м3.
3.Удельный объём смеси в начале и в конце процесса.
v1 = V1/ Mсм= 40/49,57 = 0,81 кг/ м3;
v2 = V2/ Mсм= 6,61/49,57 = 0,13 кг/ м3.
4.Температура газовой смеси в конце процесса.
Из уравнения состояния
Т2 = V2*Р2/(Rсм* Mсм) = 6,61*0,9*106/(269*49,57) = 446K.
5.Работа сжатия в процессе.
Lсж = [n/(n-1)]*(P2*V2 – P1*V1) = [1,22/(1,22 -1)]*(0,9*106*6,61 –
- 0,1*106*40) = 10808090 Дж.
6.Работа, затрачиваемая на привод компрессора.
Lk = [M*n*R*T1/(n-1)]*[(P2/P1)n-1/n -1] = [49,57*1,22*269*300/(1,22-
-1)]*[(0,9/0,1)1,22-1/1,22 -1] = 10785550 Дж.
7.Массовая изохорная теплоёмкость рабочего тела в данном процессе.
Cvmсм = gCO*CvmCO + gN2*CvmN2 + gCO2*CvCO2 = 0,091*0,7427 + +0,652*0,7352 +0,257*0,6259 = 0,708 кДж/(кг*К).
8. Массовая изобарная теплоёмкость рабочего тела в данном процессе:
Cрmсм = gCO*CрmCO + gN2*CрmN2 + gCO2*CрCO2 = 0,091*1,0396 + +0,652*1,0304 +0,257*0,8148 = 0,976 кДж/(кг*К).
9. Показатель адиабаты смеси:
k = Cрmсм / Cvmсм = 0,976/0,708 = 1,38.
10.Изменение внутренней энергии газовой смеси.
∆U = [(n – 1)/(1 – k)]*L = [(1,22 – 1)/(1 – 1,38)]* 10785550 = - 6244266 Дж.
11.Количество теплоты, участвующее в процессе.
Q = [(k – n)/(k – 1)]*L =[(1,38 – 1,22)/(1,38 – 1)]* 10785550 = 4541284 Дж.
12. Изменение энтропии в процессе.
∆S = M*Cvmсм* [(n – k)/(n – 1)]* ln(T2/T1),
∆S = 49,57*708* [(1,22 – 1,38)/(1,22 – 1)]*ln(446/300) = - 10121 Дж/К.
Изображение процесса в координатах p-v и T-s координатах.
| V,м3 |
| 11 1 |
| Р, МПа |
| S,кДж/(кг*К) |
| T,К |
Ответы на вопросы
1.В каких пределах может изменяться показатель политропного процесса?
В общем случае показатель политропы сжатия может быть любым, однако на практике реализуется показатель политропы от k до 1 (1<n<k).
n=1 – изотермически компрессор;
n=k – адиабатный компрессор.
2.В каких пределах может изменяться теплоёмкость рабочего тела в политропном процессе?
Численно теплоемкость изменяется в пределах от -∞ до +∞, зависит от показателя политропы и адиабаты: С = Cv*[(n-k)/(n-1)].
|
|
|
3.Как выглядит уравнение 1-го закона термодинамики применительно к рассмотренному в задаче процессу?
Так как в политропном процессе происходит изменение внутренней энергии и совершается работа, то 1 закон термодинамики имеет вид:
Q = L + ∆U.
4.Как зависит работа, затрачиваемая на привод компрессора, от показателя политропы, почему?
С увеличением показателя политропы работа, затрачиваемая на привод компрессора, согласно уравнению Lk = [n*R*T1/(n-1)]*[(P2/P1)n-1/n -1], уменьшается.
|
|
|


