 |
Выполнить задания из проверочной работы «Кислотные и основные свойства органических соединений».
|
|
|
|
Медицинский институт
Государственного бюджетного образовательного учреждения профессионального образования «СЫКТЫВКАРСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
ИМЕНИ ПИТИРИМА СОРОКИНА»
Кафедра биохимии и экстремальной медицины
Методические указания для студентов 1 курса
Специальности (направления подготовки) 060101 – Лечебное дело
к практическому (лабораторному) занятию
по дисциплине Биоорганическая химия
ТЕМА: Кислотность. Основность.
ЦЕЛЬ: Сформировать знания кислотно-основных свойств органических соединений, определяющих большинство химических реакций в живом организме.
ЗАДАЧИ: Научиться определять кислотные и основные центры в соединениях; сравнивать силу кислот и оснований; применять принцип ЖМКО. Выполнить проверочную работу по теме «Кислотные и основные свойства органических соединений».
СТУДЕНТ ДОЛЖЕН ЗНАТЬ:
- до изучения темы: Из школьного курса химии понятия «кислота» и «основание», теорию Бренстеда-Лоури.
- после изучения темы: Кислотно-основные свойства органических соединений, зависимость силы кислоты и основания от различных факторов; принцип ЖМКО.
СТУДЕНТ ДОЛЖЕН УМЕТЬ: Сравнивать силу кислотности и основности биологически важных соединений; использовать принцип ЖМКО при выборе антидотов.
СОДЕРЖАНИЕ ЗАНЯТИЯ:
1. Вводный контроль – ответить на вопросы самоконтроля:
- Что такое «кислота» и чем отличается это понятие по теории Бренстеда-Лоури от теории Льюиса?
- Какие факторы влияют на кислотные свойства органических соединений?
- Какое из соединений более основно: виниламин или аллиламин. Дать объяснения.
Ответить на тестовые задания:
1. Окрашивает лакмус в синий цвет водный раствор:
|
|
|
а) 2-аминопропана; б) бромид этиламмония; в) нитробензола; г) триэтиламина; д) анилина.
2. Фенолфталеин остается бесцветным в растворе:
а) глицилаланина; б) метилэтиламина; в) фенола; г) анилина; д) этанола.
3. Окрашивает лакмус в синий цвет водный раствор:
а) бромид этиламмония; б) нитробензол; в) триэтиламин; г) 2-аминопропан; д) анилин.
4. Раствор диаминомонокарбоновой кислоты изменяет окраску фенолфталеина на:
а) малиновую; б) синюю; в) зеленую; г) желтую; д) красную.
5. Раствор моноаминодикарбоновой кислоты изменяет окраску лакмуса на:
а) синюю; б) желтую; в) красную; г) фиолетовую; д) малиновую.
6. Амфотерными свойствами обладают:
а) белок; б) анилин; в) аминоуксусная кислота; г) глицерин; д) фенол.
7. Укажите самый сильный центр основности в молекуле:

а) 1; б) 2; в) 3; г) 4; д) 5.
8. Связь О-Н наиболее полярна в:
а) воде; б) метаноле; в) феноле; г) пропаноле-2; д) муравьиной кислоте.
9. Основные свойства первичных аминов описываются уравнением:

10. Пиридоксамин может максимально прореагировать с … моль соляной кислоты:
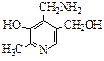
а) одним; б) двумя; в) тремя; г) четырьмя; д) пятью.
11. Наиболее сильными кислотными свойствами обладает:
а) HCOOH; б) C6H5OH; в) CH3COOH; г) CCl3COOH; д) С6Н5СООН.
12. Наибольшей константой диссоциации в водном растворе обладает:
а) H2C=CH-COOH; б) CH3-CH2-COOH; в) HC≡C-COOH;
г) (CH3)3C-COOH; д) Н-СООН.
13. Кислотные свойства выражены наиболее сильно у соединения:

14. Кислотные свойства уменьшаются в ряду:
а) пропанол-2, ацетилен, фенол;
б) муравьиная кислота, этанол, метилфенол;
в) 1,1-дихлороэтанол, 1-хлороэтанол, этанол;
г) уксусная кислота, хлороуксусная кислота, бромоуксусная кислота;
д) фтороуксусная кислота, бромоуксусная кислота, акриловая кислота.
15. Наибольшей константой диссоциации в водном растворе обладает:
а) CH≡C-COOH; б) H2C=CH-COOH; в) CH3CH2COOH;
г) (CH3)2CH-COOH; д) Н2С=СН-СН2СООН.
16. Самой сильной кислотой является:
а) С6Н5ОН; б) СН3СН2ОН; в) Н2О; г) СН3ОН; д) CH3NH2.
|
|
|
17. Самой сильной кислотой в водном растворе является:
а) уксусная; б) триметилуксусная; в) трихлороуксусная; г) пропановая; д) аминоуксусная.
18. Наиболее сильной из бензойных кислот является:

19. Выберите амин с самыми слабыми основными свойствами:
а) пропиламин; б) триэтиламин; в) анилин; г) дифениламин; д) диметиламин.
20. Выберите амин с самыми сильными основными свойствами:
а) фениламин; б) метиламин; в) дифениламин; г) N-метилфениламин; д) трифениламин.
21. Основные свойства выражены сильнее, чем у аммиака, в молекуле:
а) анилина; б) метиламина; в) диэтиламина; г) гидроксиламина; д) метилфениламина.
22. Самое слабое основание – это

23. Самым сильным основанием является:

24. Расположите указанные соединения в порядке увеличения кислотных свойств:
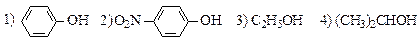
а) 3 4 2 1; б) 1 3 4 2; в) 4 3 1 2; г) 2 3 1 4; д) 4 3 2 1.
25. Кислотность соединений в растворе уменьшается в последовательности:
CH3OH (1); (CH3)2CH-OH (2); H2O (3).
а) 1,2,3; б) 3,2,1; в) 2,1,3; г) 3,1,2; д) 1,3,2.
26. Кислотность соединений в растворе уменьшается в последовательности:
1) С2H5SH 2) (CH3)2CH-SH 3) CH3-SH 4) (CH3)3C-SH 5) H2S
а) 5>3>1>2>4; б) 4>2>3>1>5; в) 3>1>5>4>2; г) 5>2>3>4>1; д) 3>5>2>1>4.
27. Расположите соединения в порядке уменьшения основных свойств:
1) CH3NHCH3, 2) CH3NH2, 3) C6H5NH2, 4) (CH3)3N.
а) 1>4>2>3; б) 1>2>3>4; в) 4>3>2>1; г) 3>4>1>2; д) 2>1>4>3.
28. Расположите соединения в порядке увеличения их основности:

а) 2<3<1<4; б) 3<1<2<4; в) 1<3<4<2; г) 3<1<4<2; д) 2<4<1<3.
29. Порядок возрастания основных свойств наблюдается в ряду:
а) аммиак – метиламин - гидроксиламин; б) гидроксиламин – метиламин - аммиак;
в) метиламин – аммиак - гидроксиламин; г) гидроксиламин – аммиак - метиламин.
д) метиламин - гидроксиламин - аммиак.
30. Жесткими основаниями Льюиса являются:
а) CH2=CH2; б) C2H5OC2H5; в) C2H5OH; г) C2H5SH; д) С6Н6.
31. Соединения серебра будут растворяться в:
а) бензоле; б) пиридине; в) воде; г) эфире; д) диметилсульфиде.
32. Основанием Льюиса является:

33. Способность отщеплять протон или предоставлять свободную орбиталь называется ………
34. Способность молекулы или частицы образовывать ковалентную связь с протоном за счет неподеленной электронной пары гетероатома, электронов π–связи или отрицательного заряда, называется ………
|
|
|
35. Соединение, способное оторвать протон от кислотного центра, называется …..…
36. Вещество, которое может принять электронную пару с образованием ковалентной связи, называется ………
Беседа по теме занятия
Характеристика кислот и оснований в сравнении двух теорий Бренстеда и Льюиса (сходство и различия). Принцип жестких и мягких кислот и оснований, использование знаний принципа ЖМКО в медицине при назначении противоядий.
Практическая работа
1. Сравнить кислотность следующих соединений и написать формулы сопряженных им оснований:

2. Сравнить основность атомов азота в следующих парах соединений:



3. Определите, в каком порядке возрастает основность атома азота в следующем соединении:

4. Соотнесите значения рКа с формулами соответствующих кислот: 1.29; 2.86; 4.76; 10.10; 16.00:
а) СН3OH б) CH3–С6Н4-OH в) ClCH2–COOH г) СH3СООH д) Cl2CH-COOH
1.0; 4.0; 7.2; 10.0; 18.0:

5. Соотнесите значения рКВН+ с формулами соответствующих оснований.
1.10; 4.58; 9.25; 10.60; 11.00:

1.10; 4.58; 5.15; 9.25; 10.60:

6. Какие из солей растворяются в изопропиловом спирте: а) MnCl2; б) AgI; в) FeCl3; г) ZnBr2. Что лучше растворяется?
7. Какие из солей будут растворяться в бензоле, а какие в спирте: а) CuBr; б) CaCl2; в) HgCl2; г) FeCl2. Что лучше растворяется?
Выполнить задания из проверочной работы «Кислотные и основные свойства органических соединений».
1. Какие из солей будут растворяться в бензоле: а) FeCl3; б) AgBr; в) ZnCl2; г) HgI2.
2. Напишите формулы сопряженных оснований для следующих кислот:

3. Сравните основные свойства следующих аминов:

4. Ощущение сладкого вкуса возникает при одновременном наличии в соединении слабых кислотного и основного центров, находящихся на определенном расстоянии друг от друга и образующих водородные связи с вкусовыми рецепторами. Укажите кислотные и основные центры в молекуле 5-нитро-2-протоксианилина, который слаще свекловичного сахара в 3100 раз.
Рекомендуемая литература:
Основная:
1. Биоорганическая химия. Учебник. /Тюкавкина Н.А., Бауков Ю.И., Зурабян С.Э. /М.: ГЭОТАР. Медиа. - 2014. – С.80-85, 108-109, 145, 149, 319-324.
|
|
|
|
|
|


