 |
Способы выражения концентрации растворов
|
|
|
|
После изучения темы студент должен
– знать: способы выражения концентрации веществ в растворах, способы приготовления растворов заданной концентрации;
– уметь: пользоваться физическим и химическим оборудованием; определять концентрации растворов по экспериментальным данным, находить концентрации растворов теоретически (решение задач);
– владеть: навыками самостоятельной работы с учебной, научной и справочной литературой по химии; вести поиск и делать обобщающие выводы;навыками безопасной работы в химической лаборатории с реактивами, посудой, аппаратурой; навыком проведения наблюдений за протеканием химических реакций и представления данных экспериментальных исследований в виде законченного протокола исследований.
Важнейшей характеристикой раствора является его состав. Количество растворенного вещества, содержащееся в определенном количестве раствора или растворителя, называется концентрацией.
Рассмотрим некоторые способы выражения концентрации растворов.
Массовая доля или процентная концентрация компонента (w) –отношение массы растворенного вещества к массе раствора, выраженное в долях или процентах:
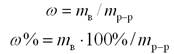 |
где m в – масса растворенного вещества, г; m р-р – масса раствора, г.
Молярная концентрация или молярность (СМ) равна числу моль растворенного вещества, содержащихся в 1 л раствора. Молярная концентрациявыражается в моль/л. Например, раствор, содержащий в 1 л 1 моль растворенного вещества, называется одномолярным и обозначается 1 М; а раствор, содержащий в 1 л 0,1 моль растворенного вещества, называется децимолярным и обозначается 0,1 М. Молярную концентрацию можно рассчитать по формуле:
|
|
|

где n в – количество растворенного вещества, моль;
V р-p – объем раствора, л;
m в – масса растворенного вещества, г;
М в – молярная масса растворенного вещества, г/моль.
Эквивалентная концентрация или нормальность (С н) равна числу моль-эквивалентов растворенного вещества, содержащихся в 1 л раствора и выражается в моль-экв/л. Раствор называется однонормальным, если в 1 л его содержится 1 моль-экв растворенного вещества (1н раствор); а если в 1 л раствора содержится 0,1 моль-экв растворенного вещества, он называется децинормальным (0,1н раствор). Нормальную концентрацию можно рассчитать по формуле:
 |
где n в – количество растворенного вещества, моль;
V р-р – объем раствора, л;
m в – масса растворенного вещества, г;
М в – молярная масса растворенного вещества, г/моль;
f – фактор эквивалентности.
Фактор эквивалентности f – число, показывающее, какая доля реальной или условной частицы вещества эквивалентна одному иону водорода или одному электрону в данной реакции, т.е. доля, которую составляет эквивалент от молекулы, иона, атома или формульной единицы вещества.
Фактор эквивалентности можно рассчитать по следующим формулам:
f (оксида) = 1/(n Э вЭ)
где n Э – число атомов элемента, образовавшего 1 молекулу оксида,
вЭ – валентность элемента.
Например, f (Cr 2 O 3) = 1/(2 × 3) = 1/6
f (кислоты) = 1/ n (Н+)
где n (Н+) – число ионов водорода, входящих в состав одной молекулы кислоты.
Например, f (H 2 SO 4) = 1/2
f (основания) = 1/ n (ОН–)
n (ОН-) – число гидрокси-групп, входящих в состав 1 молекулы основания.
Например, f (Fe (OH)3) = 1/3
f (соли) = 1/(n Ме × вМе)
n Ме – число молекул металла, входящих в состав 1 молекулы соли
вМе – валентность металла
Например, f (Fe 2 (SO 4)3) = 1/(2 × 3) = 1/6
Моляльная концентрация или моляльность (С m) равна числу моль растворенного вещества в 1 кг растворителя. Ее можно рассчитать по формуле:

|
|
|
n в – количество растворенного вещества, моль;
m в – масса растворенного вещества, г;
M в – молярная масса растворенного вещества, г/моль;
m р-ль – масса растворителя, кг.
Часто для реакций, протекающих в растворах, используют закон эквивалентов, согласно которому количества реагирующих веществ равны:
n 1 = n 2 ⇒ С1 V 1 = C 2 V 2
|
|
|


