 |
Схема Н-катионирования с «голодной» регенерацией фильтров.
|
|
|
|
Если имеет место соотношение
Жса ³  - Щостн, г-экв/м3 (3.59)
- Щостн, г-экв/м3 (3.59)
где Жса – кальциевая жесткость исходной воды, г-экв/м3;
 - содержание бикарбонатного иона в исходной воде, г-экв/м3;
- содержание бикарбонатного иона в исходной воде, г-экв/м3;
Щостн – остаточная щелочность воды после водород-катионирования с «голодной» регенерацией фильтров, г-экв/м3.
то за рабочий цикл фильтра удаляется только кальций, который при регенерации серной кислотой сбрасывается в виде CaSO4. Его количество в час определяется по из формуле:
 =
=  (3.60)
(3.60)
где  - эквивалентная масса СаSO4;
- эквивалентная масса СаSO4;
n – число регенераций фильтра в сутки:
а – количество работающих фильтров.
Если в исходной воде
Жса <  - Щостн, г-экв/м3 (3.61)
- Щостн, г-экв/м3 (3.61)
то Н-катионитными фильтрами задерживается весь кальций, содержащийся в исходной воде (ЖСа), и часть магния, определяемая из уравнения:
ЖMgн =  - Щостн - ЖСа, мг-экв/л (3.62)
- Щостн - ЖСа, мг-экв/л (3.62)
где Щостн – остаточная щелочность воды после водород-катионитных фильтров, г-экв/м3;
ЖСа – кальциевая жесткость исходной воды, мг-экв/л.
Часовой сброс сульфата кальция определяется по формуле:
 =
=  (3.63)
(3.63)
где aСаг – доля катионов кальция в ионах, задержанных водород-катионитным фильтром
 (3.64)
(3.64)
Часовой сброс сульфата магния определяется по формуле:
 =
=  (3.65)
(3.65)
где 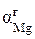 - доля катионов магния в ионах, задержанных водород-катионитным фильтром
- доля катионов магния в ионах, задержанных водород-катионитным фильтром
 (3.66)
(3.66)
Сброс избытка серной кислоты возможен при дозах H2SO4 более 49,04 г/г-экв и принимается в соответствии с расчетом водоподготовки.
Сброс избытка H2SO4 от одной регенерации
 = 0,001 × (qкг – 49,04) × Vкат × Ерн, кг (3.67)
= 0,001 × (qкг – 49,04) × Vкат × Ерн, кг (3.67)
Часовой сброс избытка H2SO4
 =
=  , кг/ч (3.68)
, кг/ч (3.68)
Последовательное Н-катионирование
Расчет массы загрязняющих веществ, образующихся при последовательном Н-катионировании, проводится по формулам (3.58) – (3.68). При этом в формуле (3.68) удельный расход Н2SO4 принимается по рис. 3.4.
|
|
|
Параллельное Н-катионирование
Подсчет сбрасываемых стоков проводится раздельно для Na- и Н-катионитных фильтров без учета второй ступени катионирования.
Сброс сернокислых солей СаSО4 и MgSO4 от одной регенерации фильтра определяется по формулам:
 = Жсн × aСа, г-экв (3.69)
= Жсн × aСа, г-экв (3.69)
 = Жсн × aМg, г-экв (3.70)
= Жсн × aМg, г-экв (3.70)
где aСа и aМg – соответственно доля солей кальция и магния в общем
количестве сбрасываемых солей жесткости.
Часовой сброс продуктов регенерации определяется по формулам:
 (3.71)
(3.71)
 кг/ч (3.72)
кг/ч (3.72)
Избыток серной кислоты, сбрасываемой при регенерации Н-катионитных фильтров подсчитывается по формулам (3.67) и (3.68).
Натрий-хлор-ионирование
Расчет сброса стоков от первой стадии обработки — натрий-катионировании производится в соответствии с указаниями, приведенными выше.
При регенерации натрий-хлор-ионитных в дренаж сбрасываются: избыток поваренной соли NaCI; продукты регенерации анионита Na2SO4, NaHCO3.
Сбрасываемый избыток соли за одну регенерацию хлор-ионитного или натрий-хлор-ионитного фильтра определяется по формуле:
 (3.73)
(3.73)
где Vан – объем анионита, загруженного в фильтр, м3;
ЕрCl - рабочая обменная способность анионита при хлор-ионировании по НСОз-, г-экв/м3 (ЕрCl =300 г-экв/м3);
gc - удельный расход соли на регенерацию анионита, г/г-экв
gc = 217 г/г-экв;
ЭNaCl – эквивалентная масса NaCl (теоретически необходимая), расходуемая на регенерацию 1 г-экв солей жесткости, г/г-экв;
Gхво - производительность всех хлор-ионитных фильтров, м3/ч;
 - содержание сульфат-иона в исходной воде, г-экв/м3.
- содержание сульфат-иона в исходной воде, г-экв/м3.
n - количество регенераций хлор-ионитного фильтра в сутки.
Избыток соли, сбрасываемый от регенерации натрий-хлор-ионитных фильтров в час, определяется по формуле:
 кг/ч (3.74)
кг/ч (3.74)
Количество сбрасываемого в час при регенерации сульфата натрия определяется по формуле:
 кг/ч (3.75)
кг/ч (3.75)
где  - эквивалентная масса Na2SO4.
- эквивалентная масса Na2SO4.
|
|
|
Количество сульфата натрия, сбрасываемого за одну регенерацию определяется по формуле:
 =
=  (3.76)
(3.76)
Количество NaHCO3, сбрасываемого за одну регенерацию, определяется по формуле:
 = Vан × ЕрCl, г-экв (3.77)
= Vан × ЕрCl, г-экв (3.77)
Количество NaHCO3, сбрасываемого от натрий-хлор-ионитных фильтров в час определяется по формуле:
 кг/ч (3.78)
кг/ч (3.78)
где  - эквивалентная масса NaHCO3.
- эквивалентная масса NaHCO3.
|
|
|


