 |
Кислотно-основные взаимодействия - Попытка 4
|
|
|
|
Весовой анализ - Попытка 6
Начало формы
Question1
Весовая форма - это
| соединение точно известного состава, по весу которого можно судить о количественном содержании определяемого вещества |
В виде какого соединения лучше осадить  при количественном определении весовым методом
при количественном определении весовым методом
  ) = ) = 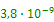
|
QuestionФорма осаждения - это
| осадок точно известного состава, в виде которого производится осаждение определяемого компонента и выделение его из смеси |
QuestionКаковы условия осаждения кристаллических осадков?
| Осаждение кристаллических осадков необходимо проводить из горячих разбавленных растворов горячими разбавленными растворами осадителя, который приливается медленно при постоянном перемешивании | ||
Question5
Правило произведения растворимости (ПР) для труднорастворимых не бинарных электролитов
ПР= 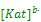 
| ||
ПР= 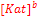 ·[An] ·[An]
|
Question6
Чему равен фактор пересчета F весовой формы  на алюминий
на алюминий
| 0,529 | ||
Question7
Избыток осадителя при осаждении осадка
| необходим ввиду того, что в этих условиях уменьшается растворимость осадка, т.к. добавляются одноименные ионы | ||
Question8
Определите, сколько граммов  будет содержаться в 1 л его насыщенного раствора, если ПР(
будет содержаться в 1 л его насыщенного раствора, если ПР( )=7,5×
)=7,5×  .
.
Ответ:
Question9
Определите растворимость (мг/л) AgCl в его насыщенном растворе, если  .
.
Ответ:0,0000133
Question10
Рассчитайте навеску  , необходимую для его определения весовым методом
, необходимую для его определения весовым методом 
| Навеска берется произвольно | ||

|
|
|
|
Question11
Приведите правило произведения растворимости (ПР) для труднорастворимых бинарных электролитов?
| ПР=[Kat]·[An] | ||
Question12
Каковы условия осаждения аморфных осадков?
| При осаждении аморфных осадков необходимо осаждение вести быстро, из горячих концентрированных растворов при перемешивании, осадок необходимо фильтровать вскоре после осаждения | ||
Question13
Рассчитайте, какой объем (мл) раствора хлорида бария концентрации 60 мг/мл необходим для полного осаждения сульфат - иона, из 1 г чистого сульфата натрия.
Ответ: 24,4
Question14
В насыщенном растворе сульфида олова [  ]=[
]=[ 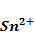 ] = 0,5×
] = 0,5×  моль/л. Определите
моль/л. Определите  .
.
Ответ:
Question16
Форма осаждения 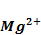 - ионов при их количественном определении весовым методом
- ионов при их количественном определении весовым методом

|
Question18
Для определения содержания серы в чугуне взяли навеску 6,0204 г. После соответствующей обработки получен сульфид меди, при прокаливании которого образовалось 0,0584 г CuO. Чему равна массовая доля (%) серы в чугуне?
Ответ:
0,4
Гетерогенные равновесия и титрование по методу осаждения - Попытка 1
Начало формы
Question1
Какая масса  требуется для приготовления 250 мл раствора 0,05 M концентрации.
требуется для приготовления 250 мл раствора 0,05 M концентрации.
Ответ:1,4
Question3
Навеску технического  массой 0,3838 г оттитровали 23,80мл раствора
массой 0,3838 г оттитровали 23,80мл раствора 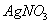 [T(
[T( ) = 0,003546]. Вычислить массовую долю (%)
) = 0,003546]. Вычислить массовую долю (%)  в образце.
в образце.
Ответ:
Question4
Для приготовления 500 мл раствора 0,1н концентрации,  требуется ______
требуется ______ 
Ответ:6,1
Question5
Какая масса 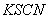 требуется для приготовления 250 мл раствора 0,1M концентрации.
требуется для приготовления 250 мл раствора 0,1M концентрации.
Ответ:2,4
Question6
Какие ионы можно определить методом Мора

|
Question7
Навеску технического  массой 0,2058 г растворили в воде, к раствору прибавили 40,00 мл 0,09980 М
массой 0,2058 г растворили в воде, к раствору прибавили 40,00 мл 0,09980 М 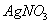 . На титрование избытка
. На титрование избытка 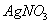 израсходовали 21,20мл раствора
израсходовали 21,20мл раствора 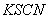 . Вычислить массовую долю (%) примесей в образце, если 1,00 мл раствора
. Вычислить массовую долю (%) примесей в образце, если 1,00 мл раствора 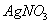 эквивалентен 1,06 мл раствора
эквивалентен 1,06 мл раствора 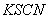 .
.
|
|
|
Ответ:
Question8
Какая масса 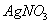 требуется для приготовления 250 мл раствора 0,1M концентрации.
требуется для приготовления 250 мл раствора 0,1M концентрации.
Ответ:4,25
Question9
На раствор, содержащий равные количества хлоридов и иодидов, подействовано раствором 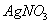 ; произведения растворимости
; произведения растворимости 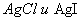
 и
и  соответственно. Какая соль осаждается первой
соответственно. Какая соль осаждается первой

|
Question10
Определение хлоридов и бромидов по методу Фольгарда возможно в _____ среде.
Ответ:
Question11
Какой объем рассола, содержащего около 60г/л NaCl, следует взять для приготовления 200,0 мл раствора, чтобы на титрование 25,00 мл его расходовалось 20,00 мл 0,0500 н. раствора  ?
?
Ответ:
Question12
К раствору, содержащему 0,2266 г технического хлорида магния, прилили 25,00мл 0,1121М 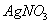 , избыток которого оттитровали 11,10мл 0,0579 М
, избыток которого оттитровали 11,10мл 0,0579 М  . Вычислить массовую долю (%)
. Вычислить массовую долю (%) 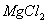 в образце; сравнить с теоретическим расчетом для
в образце; сравнить с теоретическим расчетом для  .
.
Ответ:45,27
Question13
Какая масса 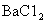 требуется для приготовления 250 мл раствора концентрации 0,05M
требуется для приготовления 250 мл раствора концентрации 0,05M
Ответ:
Question14
Какая масса  содержится в 1 л раствора, если после разбавления 25,00 мл его до 250,0мл на титрование пробы объемом 20,00 мл израсходовали 24,37 мл 0,09850 М
содержится в 1 л раствора, если после разбавления 25,00 мл его до 250,0мл на титрование пробы объемом 20,00 мл израсходовали 24,37 мл 0,09850 М 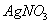 ?
?
Ответ:43,8
Question15
Какая масса 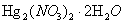 требуется для приготовления 500 мл раствора 0,05 М концентрации,
требуется для приготовления 500 мл раствора 0,05 М концентрации,  .
.
Ответ:
Question16
Указать среду, в которой возможно определение хлоридов и бромидов по методу Фольгарда
| кислая | ||
Question17
Какая масса  требуется для приготовления 250 мл раствора 0,05 M концентрации.
требуется для приготовления 250 мл раствора 0,05 M концентрации.
Ответ:
Question18
Как влияет увеличение рН на титрование с адсорбционным индикатором
| интенсивность окраски возрастает |
Question20
Указать индикатор, применимый при определении иодидов
| железоаммонийные квасцы | ||
Question21
К 25,00 мл раствора  прибавили 50,00 мл 0,l100 М
прибавили 50,00 мл 0,l100 М 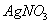 , разбавили водой до 100,0мл, отобрали на анализ 50,00 мл и оттитровали их 5,23 мл 0,09800 М
, разбавили водой до 100,0мл, отобрали на анализ 50,00 мл и оттитровали их 5,23 мл 0,09800 М 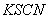 . Какая масса
. Какая масса  содержалась в 400,0 мл первоначального раствора?
содержалась в 400,0 мл первоначального раствора?
Ответ:4,18
Question22
Какие требования предъявляют к осадкам в методах осадительного титрования
| малое значение ПР, быстрое выпадение осадка | ||
Question23
|
|
|
 требуется для приготовления 250 мл раствора 0,05M концентрации.
требуется для приготовления 250 мл раствора 0,05M концентрации.
Ответ:0,73
Question24
Указать факторы, от которых зависит величина скачка на кривой титрования
| произведение растворимости осадка, исходные концентрации реагирующих вещества |
Question25
Какие требования предъявляют к реакциям в методах осадительного титрования
| осадок нерастворим и выпадает быстро, недопустимо соосаждение |
QuestionУказать фактор, на котором основано применение индикатора  при титровании хлоридов раствором нитрата серебра
при титровании хлоридов раствором нитрата серебра
различие в величинах ПР  и и 
|
Question27
Какая масса КС1 требуется для приготовления 250 мл раствора 0,05 M концентрации.
Ответ:
Конец формы
Кислотно-основные взаимодействия - Попытка 4
Начало формы
Question1
Какая из указанных солей может быть оттитрована стандартным раствором НСl методом прямого титрования

|
Question2
Укажите соответствие между основными установочными веществами для стандартизации растворов:
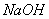
| Выбрать... тетраборат натрия тетраборат натрия щавелевая кислота перманганат калия | |

| Выбрать... тетраборат натрия тетраборат натрия щавелевая кислота перманганат калия | |
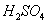
| Выбрать... тетраборат натрия тетраборат натрия щавелевая кислота перманганат калия | |
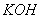
| Выбрать... тетраборат натрия тетраборат натрия щавелевая кислота перманганат калия |
Question3
По какой формуле рассчитывают титр стандартного раствора НСl по определяемому веществу NaOH
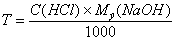
|
Question 4Какая посуда применяется для точного измерения объемов растворов в титриметрическом анализе?
| Мерные колбы, пипетки, бюретки | ||
Question5
Осаждение  - ионов в виде
- ионов в виде  дихроматом калия проводят в присутствии ацетатного буферного раствора, так как достигается
дихроматом калия проводят в присутствии ацетатного буферного раствора, так как достигается
полнота осаждения  и отделения и отделения  -ионов от -ионов от  и и 
|
Question7
| Масса соли, образовавшейся при нейтрализации 25 мл 0,5 н раствора едкого натра соляной кислотой, равна | 0,731 | |
| Масса гидроксида калия для приготовления 150 мл раствора с концентрацией 0,1 моль экв/л равна | Выбрать... 0,93 0,113 0,225 0,731 0,84 | |
| На нейтрализацию раствора серной кислоты пошло 20 мл раствора гидроксида натрия с титром 0,004616 г/мл. Масса серной кислоты в растворе равна | Выбрать... 0,93 0,113 0,225 0,731 0,84 | |
| Масса щавелевой кислоты безводной для приготовления 50 мл 0,1 н раствора равна | Выбрать... 0,93 0,113 0,225 0,731 0,84 |
Question8
|
|
|
1 л 0,3 М раствора  смешали с 1 л 0,4 М раствора HCl. Сколько молей и какого вещества осталось в избытке?
смешали с 1 л 0,4 М раствора HCl. Сколько молей и какого вещества осталось в избытке?
Ответ:0,2
Question9
Какое из указанных веществ является установочным веществом, применяемым для определения титра стандартного раствора NaOH

|
Question 10Сколько граммов безводной соды следует взять для приготовления 200 мл раствора, необходимого для установления титра 0,1 н раствора 
Ответ:1,06
Question11
Определите молярную концентрацию раствора, полученного при растворении сульфата натрия массой 42,6 г в воде массой 300 г, если плотность раствора 1,12 г/мл.
Ответ:
Question12
В каком из следующих растворов значение рН будет наибольшим

|
Question13
Сколько мг гидроксида бария содержится в растворе, если на нейтрализацию его идет 20,0 мл 0,1245 н. раствора соляной кислоты?
Ответ:
Question14
Какая масса сульфата меди содержится в 450 мл раствора с массовой долей 17%? (плотность раствора 1,05 г/мл)
Ответ:
Question15
Индикаторную гидроксильную погрешность рассчитывают по формуле:
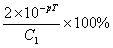
|
Question16 Сколько мл 0,15 н раствора гидроксида натрия пойдет на титрование 21 мл 0,1133 н раствора серной кислоты?
Ответ:
Question17
В 100 мл раствора содержится 19,615 г серной кислоты. Какова нормальность раствора?
Ответ:
Question18
Какой объем 0,1500 н. раствора гидроксида натрия пойдет на титрование 21,00 мл раствора соляной кислоты с Т = 0,003810 г/мл?
Ответ:14,61
Question19
Из раствора хлорида аммония испарилось 25 мл воды, в результате чего осталось 90 г раствора с массовой долей 31%. Рассчитайте массовую долю хлорида аммония в исходном растворе.
Ответ:
Question20
Индикаторную основную погрешность рассчитывают по формуле

|
Question21
Рассчитайте, какую навеску щавелевой кислоты ( O4×2
O4×2  O) необходимо взять для приготовления 250 мл 0,1 Н раствора?
O) необходимо взять для приготовления 250 мл 0,1 Н раствора?
Ответ:
Question22
Укажите соответствие между индикатором и интервалом перехода
| лакмус | Выбрать... 8-10 4,2-6,3 3,1-4,4 5,0-8,0 6,5-7,2 | |
| фенолфталеин | Выбрать... 8-10 4,2-6,3 3,1-4,4 5,0-8,0 6,5-7,2 | |
| метиловый красный | Выбрать... 8-10 4,2-6,3 3,1-4,4 5,0-8,0 6,5-7,2 | |
| метиловый оранжевый | Выбрать... 8-10 4,2-6,3 3,1-4,4 5,0-8,0 6,5-7,2 |
Question23
Для определения нерастворимых карбонатов  и
и  методом кислотно-основного титрования используется
методом кислотно-основного титрования используется
| обратное титрование |
Question24
|
|
|
Оксид кальция массой 2,27 г, загрязненный нерастворимыми примесями, растворен в 100 мл соляной кислоты (концентрация - 0,7740 моль/л). На нейтрализацию полученного кислого раствора затрачено 19,2 мл раствора гидроксида натрия (концентрация - 0,1250 моль/л). Рассчитайте массовую долю оксида кальция в образце.
Ответ:92,51
Question25
Индикаторную водородную погрешность рассчитывают по формуле
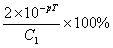
|
Question 26Как правильно выбрать индикатор по кривой кислотно-основного титрования?
Выберите один ответ.
| Верхний и нижний пределы интервала перехода окраски должен лежать внутри скачка титрования |
Question27 В титриметрических методах анализа точность получаемых результатов зависит от
| точности установления концентрации титранта, измерения объемов, выбранных индикаторов, точности установления концентрации титранта, определения точки эквивалентности |
Question 28Сколько граммов серной кислоты содержится в растворе, если на нейтрализацию его требуется 20,00 мл раствора NaOH c Т = 0,004614 г/мл?
Ответ:0,11
Question29
На титрование 25 мл 0,1 н раствора щавелевой кислоты пошло 27,5 мл гидроксида натрия. Определить титр (г/мл) раствора гидроксида натрия.
Ответ:0,0909
Question30
Укажите основные характеристики стандартных растворов
| Титр, нормальность, поправочный коэффициент | ||
Question31
При титровании раствора НСООН раствором NaOH в точке эквивалентности рассчитывают [  ] по формуле
] по формуле

|
Question 32При смешении равных объемов 0,1 М HCl + 0,1 М 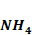 OH раствор будет иметь кислую реакцию
OH раствор будет иметь кислую реакцию
Question 33Сколько граммов КOH необходимо взять для приготовления 1,5 л 0,1 М раствора?
Ответ:8,4
Question34
Укажите формулу, по которой рассчитывают концентрацию  ионов водных растворов HCl:
ионов водных растворов HCl:
 
|
Question 35В выражении: НА +В =НВ++А, А - это
| сопряженное основание | ||
Question36
Сколько мл 0,1500 н. раствора NaOH пойдет на титрование 21 мл 0,1133 н. раствора серной кислоты?
Ответ:
Question37
В каком растворе степень диссоциации основания наибольшая

|
Question38
Сколько мл 0,1200 н. раствора соляной кислоты требуется для нейтрализации 0,2 г чистого карбоната натрия?
Ответ:31,45
Question39
В воде массой 400 г растворили сероводород объемом 12 мл (н.у.). Определите массовую долю сероводорода в растворе
Ответ:0,005
Question40
Какое из приведенных математических выражений соответствует закону действия масс:

|
Question42
Укажите соответствие между массовой долей и молярной концентрацией следующих растворов (точность до четвертого знака после запятой):
| 1.8%-ный раствор сульфата натрия с плотностью 1,0742 имеет молярную концентрацию | Выбрать... 0,2583 1,0178 1,1425 0,1362 1,9686 | |
| 10%-ный раствор хлорида аммония с плотностью 1,0532 имеет молярную концентрацию | Выбрать... 0,2583 1,0178 1,1425 0,1362 1,9686 | |
| 5.3%-ный раствор хлорида натрия с плотностью 1,1234 имеет молярную концентрацию | Выбрать... 0,2583 1,0178 1,1425 0,1362 1,9686 | |
| 2,5%-ный раствор карбоната натрия с плотностью 1,0952 имеет молярную концентрацию | Выбрать... 0,2583 1,0178 1,1425 0,1362 1,9686 |
Question43
Какие вещества могут быть использованы в качестве индикаторов в методе кислотно-основного титрования:
| органические соединения, изменения цвета которых происходит вследствие последовательного присоединения протонов или гидроксогрупп | ||
Question45
Индикаторную кислотную погрешность рассчитывают по формуле:
| . | 
|
Question 46На титрование 0,5520 г технического образца буры расходуется 18,0 мл раствора соляной кислоты (ТHCl/NaOH = 0,00400 г/мл). Определите массовую долю  10
10  O в образце.
O в образце.
Ответ:62,28
Question47
Укажите соответствие между условием задачи и рН раствора
| рН 0,02 моль/л раствора ацетата натрия, рК(уксусной кислоты)=4,75 | Выбрать... 2,58 5,27 2,95 3,71 8,23 | |
| рН 0,01 моль/л раствора азотистой кислоты, рК=3,16 | Выбрать... 2,58 5,27 2,95 3,71 8,23 | |
| рН 0,05 моль/л раствора хлорида аммония рК(аммиак)=4,76 | Выбрать... 2,58 5,27 2,95 3,71 8,23 | |
| рН 0,02 моль/л раствора бензойной кислоты, рК=4,2 | Выбрать... 2,58 5,27 2,95 3,71 8,23 |
Question48
Укажите соответствие между условием задачи титром (мг/мл):
| Титр 1 моль/л раствора щавелевой кислоты безводной | Выбрать... 20,2 30 90 4,44 75 | |
| Титр раствора в 100 мл которого содержится 0,4442 г гидроксида натрия равен моль | Выбрать... 20,2 30 90 4,44 75 | |
| Титр раствора, содержащий 1 моль уксусной кислоты в 2 л, равен | Выбрать... 20,2 30 90 4,44 75 | |
| Титр 0,1 моль раствора тетрабората натрия безводного | Выбрать... 20,2 30 90 4,44 75 |
Question49
Укажите соответствие между условием задачи и молярной концентрацией эквивалента (моль/л)
| На титрование 15 мл карбоната натрия с метилоранжем затрачено 18 мл соляной кислоты с титром 0,001132 г/мл. Молярная концентрация эквивалента титранта равна | Выбрать... 0,125 0,0294 0,0310 0,157 | |
| На титрование 20 мл серной кислоты затрачено 25 мл 0,1 М раствора гидрокида натрия. Молярная концентрация эквивалента раствора серной кислоты равна | Выбрать... 0,125 0,0294 0,0310 0,157 | |
| Титр раствора карбоната натрия 0,00156 г/мл. Молярная концентрация эквивалента этого раствора равна | Выбрать... 0,125 0,0294 0,0310 0,157 |
Question50
Укажите, первичные и вторичные стандарты
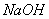
| вторичный | |

| Выбрать... не является стандартом вторичный вторичный первичный | |

| Выбрать... не является стандартом вторичный вторичный первичный | |

| Выбрать... не является стандартом вторичный вторичный первичный |
Question51
К кислотам Льюиса НЕ относятся

|
Question52
Точка эквивалентности соответствует рН 7 титрованию

|
Question54
Сколько фосфата натрия необходимо взять, чтобы приготовить 2,0 л 0,5 н. раствора по отношению к реакциям полного обмена? Какова молярность раствора?
Ответ:54,67
Question55
Укажите соответствие между условием задачи и массовой долей раствора (%) Точность приводить до десятых
| Плотность раствора серной кислоты с титром 0,01265 г/мл равна 1,2314. Массовая доля раствора равна | Выбрать... 0,6 1,0 9,1 3,5 4,0 | |
| В 150 мл воды растворили 15 г карбоната натрия. Массовая доля раствора равна | Выбрать... 0,6 1,0 9,1 3,5 4,0 | |
| Плотность 0,5 М раствора щавелевой кислоты безводной 1,1132. Массовая доля раствора равна | Выбрать... 0,6 1,0 9,1 3,5 4,0 | |
| В 250 мл раствора содержится 1.75 г буры. Плотность раствора 1,0954. Массовая доля раствора равна | Выбрать... 0,6 1,0 9,1 3,5 4,0 |
Question56
Определите массу воды, в которой необходимо растворить 50 г сульфата калия для получения раствора с массовой долей вещества 10%.
Ответ:450
Question57
Методом замещения определяют:

| ||
Question58
В общем виде содержание NH4Cl при его определении методом обратного титрования рассчитывают по формуле:

|
Question Определите массу карбоната кальция, если известно, что его навеску обработали 50 мл 0,2000 н. раствора соляной кислоты и на титрование избытка этой кислоты пошло 10 мл раствора гидроксида натрия. На титрование 25,0 мл соляной кислоты расходуется 24,0 мл гидроксида натрия.
Ответ:0,4
Question Для усиления гидролиза соли по катиону Kt++HOH ↔KtOH + H+ гидролизможноусилить
| добавлением ОН--ионов, связывающих избыточные Н+-ионов, разбавлением раствора водой и повышением температуры раствора |
Question При титровании водного раствора  раствором HCl [
раствором HCl [  ] в точке эквивалентности рассчитывают по формуле
] в точке эквивалентности рассчитывают по формуле

|
Question63
Указать соответствующее соединение, которое определяет рН в т.э. при титровании:
| Гидроксида натрия соляной кислотой, рН в т.э. определяет | Выбрать... Ацетат натрия Хлорид аммония Вода Уксусная кислота | |
| Гидроксида аммония соляной кислотой, рН в т.э. определяет | Выбрать... Ацетат натрия Хлорид аммония Вода Уксусная кислота | |
| Уксусной кислоты гидроксидом натрия, рН в т.э. определяет | Выбрать... Ацетат натрия Хлорид аммония Вода Уксусная кислота | |
| Соляной кислоты гидроксидом натрия, рН в т.э. определяет | Выбрать... Ацетат натрия Хлорид аммония Вода Уксусная кислота |
Question64
Вычислите массу 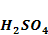 в растворе, если на нейтрализацию его пошло 20 мл раствора NaOH с титром 0,004616 г/мл.
в растворе, если на нейтрализацию его пошло 20 мл раствора NaOH с титром 0,004616 г/мл.
Ответ:0,11
Question По каким формулам рассчитывают концентрацию  - ионов водных растворов уксусной кислоты?
- ионов водных растворов уксусной кислоты?
 
|
Question В основе метода протолитометрии лежит реакция
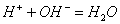
|
Question На титрование 25 мл 0,1 н. раствора щавелевой кислоты пошло 27,5 мл гидроксида калия. Определите нормальность раствора KOН.
Ответ:0,005091
Question Согласно теории Бренстеда-Лоури установите соответствие соединений кислотам, основаниям, амфолитам:

| Выбрать... Основание Кислота Амфолит | |

| Выбрать... Основание Кислота Амфолит | |

| Выбрать... Основание Кислота Амфолит |
Question Определить титр (г/мл) 0,5 М раствора 
Ответ:0,053
Question 25 мл 0,5 н. раствора едкого натра нейтрализовали соляной кислотой и раствор выпарили. Определите массу получившей соли.
Ответ:0,73
Question Определить молярную концентрацию раствора, полученного при растворении сульфата натрия массой 42,6 г в воде, массой 300 г, если плотность раствора 1,12 г/мл
Ответ:0,9807
Question Установить соответствие между реакцией среды и раствором соли
| Раствор хлорида меди, среда раствора | Выбрать... Нейтральная Щелочная Кислая | |
| Раствор хлорида аммония, среда раствора | Выбрать... Нейтральная Щелочная Кислая | |
| Раствор нитрита натрия, среда раствора | Выбрать... Нейтральная Щелочная Кислая | |
| Раствор ацетата аммония, среда раствора | Выбрать... Нейтральная Щелочная Кислая |
Question73
В ацидометрии используют стандартный раствор
| кислоты |
Question Какой прием титрования используется для определения следующих веществ методом кислотно-основного титрования
| нерастворимые карбонаты | Выбрать... косвенное титрование обратное титрование прямое титрование | |
| хлорид аммония | Выбрать... косвенное титрование обратное титрование прямое титрование | |
| кислота | Выбрать... косвенное титрование обратное титрование прямое титрование | |
| азот органического вещества | Выбрать... косвенное титрование обратное титрование прямое титрование | |
| щелочь | Выбрать... косвенное титрование обратное титрование прямое титрование |
Question75
В алкалиметрии используется стандартный раствор
| щелочи |
Question Какая масса соды ( ) необходима для уничтожения разлившейся серной кислоты объемом 5 л с концентрацией 6 моль/л? Соду следует взять на 50% больше от стехиометрического количества.
) необходима для уничтожения разлившейся серной кислоты объемом 5 л с концентрацией 6 моль/л? Соду следует взять на 50% больше от стехиометрического количества.
Ответ:4770
Question Сколько мг гидроксида бария содержится в растворе, если на нейтрализацию его идет 20 мл 0,1245 н раствора соляной кислоты?
Ответ:212,9
Question Точка нейтрализации (т.н.) совпадает с точкой эквивалентности (т.э.) кислотно-основного титрования при титрировании
| сильного основания сильной кислотой или сильной кислоты сильным основанием |
Question80
Какой из перечисленных электролитов необходимо прибавить к раствору для усиления гидролиза по аниону

|
Question В воде массой 600 г растворили 560 мл аммиака (н.у.). Определите массовую долю аммиака в полученном растворе.
Ответ:0,07
Question Найти соответствие рН, полученных смешением (точность до второго знака после запятой):
| 50 мл 0,01 М раствора уксусной кислоты и 25 мл 0,2 М ацетата натрия | Выбрать... 5,75 4,76 4,92 | |
| 100 мл 0,2 М ацетата натрия и 100 мл 0,1 М раствора соляной кислоты | Выбрать... 5,75 4,76 4,92 | |
| 100 мл 0,1 М уксусной кислоты и 100 мл 0,1 М ацетата натрия | Выбрать... 5,75 4,76 4,92 | |
| 100 мл 0,1 М уксусной кислоты и 100 мл 0,05М раствора гидроксида натрия | Выбрать... 5,75 4,76 4,92 |
Question83
Вычислите молярную концентрацию раствора сульфата калия, в 20 мл которого содержится 1,74 г растворенного вещества. Какова молярная концентрация раствора?
Ответ: 0,5
Question Какое из указанных веществ является установочным веществом, применяемым для определения титра стандартного раствора НСl
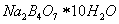
|
Question На величину скачка титрования оказывают влияние
| температура раствора, природа титруемых соединений, концентрация титруемого и стандартного растворов |
Question Для опрыскивания крыжовника и смородины против мучнистой росы применяется 0,5%-ный раствор кальцинированной соды ( ). Вычислите молярность этого раствора. (плотность раствора 1,01 г/
). Вычислите молярность этого раствора. (плотность раствора 1,01 г/  )
)
Ответ:0,0476
Question В каком из следующих растворов рН будет наименьшим
Выберите один ответ.
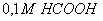
|
Question Какой объем (мл) раствора уксусной кислоты с концентрацией 0,1 моль экв/л необходим для приготовления 10 мл раствора с концентрацией в 10 раз меньшей:
Question Укажите соответствие между формулой расчета и условием:

| После т.э. | |

| До т.э | |

| Аммиак в т.э. | |

| Сильное сильным т.э. |
Question90
Сколько граммов  содержится в 1 мл 0,16 н. раствора, если его нормальность вычислена по реакции взаимодействия с кислотой и реакция идет до образования
содержится в 1 мл 0,16 н. раствора, если его нормальность вычислена по реакции взаимодействия с кислотой и реакция идет до образования  ?
?
Ответ:0,008
Question Кислотно-основное титрование точка нейтрализации совпадает с точкой эквивалентности при тетрировании:
| сильной кислоты сильным основанием |
Question Укажите уравнение химической реакции протекающей при титровании  стандартным раствором NaOH в присутствии индикатора фенолфталеина
стандартным раствором NaOH в присутствии индикатора фенолфталеина

|
Question93
Установить соответствие между раствором соли и окраской индикатора
| Карбонат натрия, фенолфталеин имеет окраску | Выбрать... Желтая Малиновая Оранжевая Розовая Синяя | |
| Ацетат натрия, лакмус имеет окраску | Выбрать... Желтая Малиновая Оранжевая Розовая Синяя | |
| Хлорид аммония, метилоранж имеет окраску | Выбрать... Желтая Малиновая Оранжевая Розовая Синяя | |
| Нитрит аммония, метилоранж имеет окраску | Выбрать... Желтая Малиновая Оранжевая Розовая Синяя |
Question94
Какую навеску безводной соды нужно взять, чтобы на ее титрование до 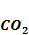 расходовалось бы 20,00 мл 0,1000 н. НСl?
расходовалось бы 20,00 мл 0,1000 н. НСl?
Ответ: 0,106
Question Сколько мл 0,1200 н раствора соляной кислоты требуется для нейтрализации 0,2 г чистого карбоната натрия?
Ответ:31,45
Question Навеску  0,5312 г растворили в мерной колбе на 100 мл. Чему равны титр и нормальность раствора?
0,5312 г растворили в мерной колбе на 100 мл. Чему равны титр и нормальность раствора?
Ответ:0,1
Question Какой объем (мл) 0,15 н раствора гидроксида натрия пойдет на титрование 21 мл раствора соляной кислоты с титром 0,003810 г/мл?
Ответ:14,61
Question Укажите соответствие между природой электролита и формулой, по которой рассчитывают [H+] его водных растворов

| Выбрать... Cильная кислота Сильное основание Слабое основание Слабая кислота | |

| Выбрать... Cильная кислота Сильное основание Слабое основание Слабая кислота | |
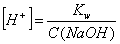
| Выбрать... Cильная кислота Сильное основание Слабое основание Слабая кислота | |

| Выбрать... Cильная кислота Сильное основание Слабое основание Слабая кислота |
Question99
Укажите, какая химическая посуда соответствует точной мерной посуде
| Цилиндр, коническая колба, мензурка | Выбрать... Не является мерной посудой Не точная Точная | |
| Колба Бунзена, воронка Бюхнера, груша | Выбрать... Не является мерной посудой Не точная Точная | |
| Химический стакан, круглодонная колба, цилиндр | Выбрать... Не является мерной посудой Не точная Точная | |
| Бюретка, пипетка, мерная колба | Выбрать... Не является мерной посудой Не точная Точная |
Question100
Укажите формулу для расчета соответствующей индикаторной ошибке:

| Выбрать... Водородная погрешность Кислотная погрешность Основная погрешность Гидроксильная погрешность | |
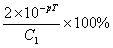
| Выбрать... Водородная погрешность Кислотная погрешность Основная погрешность Гидроксильная погрешность | |

| Выбрать... Водородная погрешность Кислотная погрешность Основная погрешность Гидроксильная погрешность | |

| Выбрать... Водородная погрешность Кислотная погрешность Основная погрешность Гидроксильная погрешность |
Question101
Определить массовую долю (%) раствора 0,1 н соляной кислоты (плотность=1,00 г/мл)
Ответ: 0,37Конец формы
|
|
|


