 |
При взаимодействии 6,3 г железа с серой выделилось 11,31 кДж теплоты. Вычислите теплоту образования сульфида железа ЕеS.
|
|
|
|
Что такое сродство к электрону? В каких единицах оно измеряется? Как изменяется окислительная активность неметаллов в периоде и в группе периодической системы с увеличением порядкового номера? Ответ мотивируйте строением атома соответствующего элемента.
Сродство к электрону – это энтальпия, поглощаемая 1 моль электронов для появления ионов данного элемента. Сродство к электрону измеряется в кДж/моль. Окислительная активность неметаллов (способность принимать электроны) в группе с увеличением по-рядкового номера элементов уменьшается, потому что с ростом заряда элемента растёт и радиус атома. Всё это приводит к уменьшению сродства к электрону у атомов элементов данной группы. Например, атомы фтора и хлора соответственно имеют следующие электронные конфигурации (Не)2s22p5 (r = 0,072нм) и (Ne)3s23p5 (r = 0,099нм). Атому фтора будет легче присоединять электрон, чем атому хлора.
В периодах окислительная активность неметаллов будет увеличиваться с увеличением порядкового номера элемента, так как будет уменьшаться радиус атомов с увеличением заряда ядра. Например, атом серы и хлора имеет следующие электронные конфигурации (Ne)3s23p4; (Ne)3s23p5. Имея семь электронов на внешнем энергетическом уровне, больше на один, чем атом серы и, соответственно больший радиус заряд ядра, чем у атома серы. Поэтому атом хлора будет иметь меньший размер атома (r = 0,099нм), чем атом серы (r = 0,104нм). Исходя из этого, атом хлора будет легче присоединять электроны, чем атом серы, т. е. хлор будет проявлять окислительные способности, чем сера.
При взаимодействии 6,3 г железа с серой выделилось 11,31 кДж теплоты. Вычислите теплоту образования сульфида железа ЕеS.
|
|
|
Решение:
Уравнение реакции имеет вид:
6,3х 11,31 кДж
Fe + S = FeS; ∆H0
55,845х х кДж
Вычислим теплоту образования сульфида железа EeS из пропорции:
6,3 г / (-11,31 кДж) = 55,845г / х;
х = (-11,31 * 55,845) / 6,3 = -100,26 кДж/моль.
Ответ: -100,26 кДж/моль.
58. Определите, при какой температуре начнется реакция восстановления Fe3O4, протекающая по уравнению:
Fe3 O4 (к) + СО (г) = ЗFеО (к) + СO2 (г); ∆Н = +34,55 кДж.
Решение:
Уравнение реакции имеет вид:
Fe3O4 (к) + СО (г) =ЗFеО (к) + СO2 (г); ∆Н = +34,55 кДж.
Значения ∆  находим из соотношений:
находим из соотношений:
∆  =
=  -
- 
Значения находим из специальных таблиц, получим:
∆  = 3S0 (FeО) + S0 (СО2) – [S0 (Fe3O4) + S0 (СО)];
= 3S0 (FeО) + S0 (СО2) – [S0 (Fe3O4) + S0 (СО)];
∆ 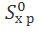 = [3(54,0) + (213,65) – (146,4 +197,91) = +31,34 Дж/моль . К.
= [3(54,0) + (213,65) – (146,4 +197,91) = +31,34 Дж/моль . К.
Найдём температуру, при которой ∆G = 0:
0 = ∆H0 - T ∆S0;
∆H0 = T ∆S0;
Т = ∆H0 / ∆S0 = 34,55 / 0,3134 = 1102,4 К.
Следовательно, при температуре 1102,4 K начнется реакция восстановления Fe3O4. Иногда эту температуру называют температурой начала реакции.
Ответ: 1102,4 К.
79. Почему при изменении давления смещается равновесие системы
N2 + 3Н2 ↔ 2NH3 и, не смещается равновесие системы N2 + O2D 2NO? Ответ мотивируйте на основании расчета скорости и обратной реакций в этих системах до и после изменения давления. Напишите выражения для констант равновесия каждой из данных систем.
Решение:
а) Уравнение реакции:
N2 + 3Н2 ↔ 2NH3.
Из уравнения реакции следует, что реакция протекает с уменьшением объёма в системе (из 4 моль газообразных веществ образуется 2 моль газообразного вещества). Поэтому при изменении давления в системе будут наблюдаться смещение равновесия. Если повысить давление в данной системе, то, согласно принципу Ле Шателье, равновесие сместится вправо, в сторону уменьшения объёма. При смещении равновесия в системе вправо скорость прямой реакции будет больше скорости обратной реакции:
 пр >
пр >  обр или
обр или  пр = k[N2] [H2]3 >
пр = k[N2] [H2]3 >  обр = k[NH3]2.
обр = k[NH3]2.
Если же давление в системе уменьшить, то равновесие системы сместится влево, в сторону увеличения объёма, то при смещении равновесия влево скорость прямой реакции будет меньше, чем скорость прямой:
|
|
|
νʹпр < νʹ обр или (νʹпр = k[N2] [H2]3)< (νʹобр = k[NH3]2).
б) Уравнение реакции:
N2 + O2 ↔ 2NO..
Из уравнения реакции следует, что при протекание реакции не сопровождается изменением объёма, реакция протекает без изменения числа молей газообразных веществ. Поэтому изменение давления в системе не приведёт к смещению равновесия, поэтому скорости прямой и обратной реакции будут равны:
νʹпр = νʹобр = или (νʹпр k[N2] [О2]) = (νʹобр = k[NО]2).
99. Из 700 г 60%-ной серной кислоты выпариванием удалили 200 г воды. Чему равна массовая доля оставшегося раствора?
Решение:
Находим массу серной кислоты в растворе:
m(H2SO4) = (700 . 60)/100 = 420 г.
Находим массу раствора после выпаривания:
m(ра-ра) = 700 – 200 = 500 г.
Находим массовую долю оставшегося раствора из формулы:
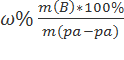 ;
;
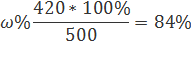
m(B) – масса растворённого вещества m(смеси); m(Ра-ра) – масса раствора, которая составляет сумму масс растворителя и растворённого вещества [m(ра-ра) = m(ра-ля) + m(В); - массовая доля растворённого вещества в процентах.
Ответ: 84%.
116. Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) Zn2+ + Н2S = ZnS↓ + 2H+
б) НСО3- + H+ = Н2O + СО2
в) Аg+ + Сl- = АgС1
Решение:
В левых частях данных ионно-молекулярных уравнений указаны свободные ионы, которые образуются при диссоциации растворимых сильных электролитов, следовательно, при составлении молекулярных уравнений следует исходить из соответствующих растворимых сильных электролитов. Например:
а) ZnCl2 + Н2S = ZnS + 2HCl;
б) KНСО3 + HCl = KCl + Н2O + СО2;
в) АgNO3 + NaСl = АgСl + NaNO3.
140. Могут ли происходить окислительно-восстановительные реакции между веществами: а) РН3 и НВг; б) K2Cr2O7 и Н3PO3; в) HNO3 и Н2S? Почему? На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме:
АsH3 + НNO3 ® Н3AsO4 + NO2 + Н2O
Решение:
а) Степень окисления в РH3 n(Р) = -3 (низшая), в HBr n(Br) = -1 (низшая). Так как и фосфор, и бром находятся в своей низшей степени окисления, то оба вещества проявляют только восстановительные свойства и взаимодействовать друг с другом не могут;
|
|
|
б) в K2Cr2O7 n (Сr) = +6 (высшая); в Н3PO3 n (Р) = +5 (высшая). Так как и хром, и фосфор находятся в своей высшей степени окисления, то оба вещества проявляют только окислительные свойства и взаимодействовать друг с другом не могут;
в) в HNO3 n (N) = +5 (высшая); в H2S n (S) = -2 (низшая). Следовательно, взаимодействие этих веществ возможно, причём HNO3 является окислителем, а H2S – восстановителем.
г) АsH3 + НNO3 ⇔ Н3AsO4 + NO2 + Н2O
Если в условии задачи даны как исходные вещества, так и продукты их взаимодействия, то написание уравнения реакции сводится, как правило, к нахождению и расстановке коэффициентов. Коэффициенты определяют методом электронного баланса с помощью электронных уравнений. Вычисляем, как изменяют степень окисления восстановитель и окислитель, и отражаем это в электронных уравнениях. Коэффициенты для восстановителя и окислителя идентичны для продуктов окисления и восстановления.. Коэффициент перед веществами, атомы которых не меняют свою степень окисления, находят подбором.
Уравнения электронного баланса:
| Восстановитель | 
| процесс окисления |
| Окислитель | 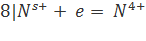
| процесс восстановления |
Ионно-молекулярное уравнение:
As3- + 8N5+ = As5+ + 8N4+
Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которые присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов восемь. Разделив это число на 1, получаем коэффициент 8 для окислителя и продукта его восстановления, а при делении 8 на 8 получаем коэффициент 1 для восстановителя и продукта его окисления. Молекулярное уравнение реакции:
АsH3 + 8НNO3 ⇔ Н3AsO4 + 8NO2 + 4Н2O
|
|
|


