 |
Определение лактозы молока
|
|
|
|
Охарактеризуйте электрохимические методы анализа биологических объектов
Электрохимические методы анализа -совокупность методов качественного и количественного анализа, основанных на электрохимических явлениях, происходящих в исследуемой среде или на границе раздела фаз и связанных с изменением структуры, химического состава или концентрации анализируемого вещества. Электрохимические методы анализа делятся на пять основных групп: потенциометрию, вольтамперометрию, кулонометрию, кондуктометрию и диэлектрометрию.
Потенциометрия объединяет методы, основанные на измерении эдс обратимых электрохимических цепей, когда потенциал рабочего электрода близок к равновесному значению (см. Электродный потенциал). Потенциометрия включает редоксметрию (см. Оксидиметрия), ионометрию и потенциометрическое титрование.
Вольтамперометрия основана на исследовании зависимости тока поляризации от напряжения, прикладываемого к электрохимической ячейке, когда потенциал рабочего электрода значительно отличается от равновесного значения (см. Поляризация электрохимическая). По разнообразию методов вольтамперометрия — самая многочисленная группа из всех электрохимических методов анализа, широко используемая для определения веществ в растворах и расплавах (например, полярография, амперометрия).
Кулонометрия объединяет методы анализа, основанные на измерении количества вещества, выделяющегося на электроде в процессе электрохимической реакции в соответствии с Фарадея законами. При кулонометрии потенциал рабочего электрода отличается от равновесного значения. Различают потенциостатическую и гальваностатическую кулонометрию, причём последняя включает прямой и инверсионный методы, электроанализ и кулонометрическое титрование.
|
|
|
К кондуктометрии относятся методы, в которых измеряют электропроводность электролитов (водных и неводных растворов, коллоидных систем, расплавов, твёрдых веществ). Кондуктометрический анализ основан на изменении концентрации вещества или химического состава среды в межэлектродном пространстве; он не связан с потенциалом электрода, который обычно близок к равновесному значению. Кондуктометрия включает прямые методы анализа (используемые, например, в солемерах) и косвенные (например, в газовом анализе) с применением постоянного или переменного тока (низкой и высокой частоты), а также хронокондуктометрию, низкочастотное и высокочастотное титрование.
Диэлектрометрия объединяет методы анализа, основанные на измерении диэлектрической проницаемости вещества, обусловленной ориентацией в электрическом поле частиц (молекул, ионов), обладающих дипольным моментом. Методы диэлектрометрии применяют для контроля чистоты диэлектриков, например для определения малых количеств влаги. Диэлектрометрическое титрование используют для анализа растворов.
Охарактеризуйте метод прямой потенциометрии
Методы прямой потенциометрии основаны на прямом применении уравнения Нернста (1) для нахождения активности или концентрации участника электродной реакции по экспериментально измеренной ЭДС цепи или потенциалу соответствующего электрода. Прямая потенциометрия применяется для непосредственного определения активности ионов (напр., Ag+ в растворе AgNO3) по значению электродного потенциала соответствующего индикаторного электрода (напр., серебряного); при этом электродный процесс должен быть обратимым.
У чому полягає метод потенціометричного титрування? Які біологічні об’єкти можна визначити за допомогою цього методу?
|
|
|
Потенциометрическое титрование основано на определении точки эквивалентности по результатам потенциометрических измерений. Вблизи точки эквивалентности происходит резкое изменение (скачок) потенциала индикаторного электрода. Это наблюдается, конечно, лишь тогда когда хотя бы один из участников реакции титрования является участником электродного процесса. Так, например, титрование по методу кислотно-основного взаимодействия может быть выполнено со стеклянным электродом. Определение хлорида - с хлорсеребряным и т.д. Так же, как и в других титриметрических методах, реакции потенциометрического титрования должны протекать строго стехиометрически, иметь высокую скорость и идти до конца. Для потенциометрического титрования собирают цепь из индикаторного электрода в анализируемом растворе и электрода сравнения. В качестве электродов сравнения чаще всего используют каломельный или хлорсеребряный электроды.
Определение лактозы молока
В основе метода лежит способность альдегидной группы лактозы в щелочной среде окисляться молекулярным йодом:
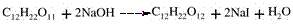
Избыточное количество йода, которое не вступило в реакцию, определяют титрованием тиосульфатом натрия, используя в качестве индикатора крахмал.
^ Материалы и реактивы: складчатые бумажные фильтры, молоко, 7 %-ный раствор сульфата меди, 2 %-ный раствор гидроксида натрия, 5 %-ный раствор фторида натрия, 0,05 моль/л раствор йода,
5 %-ный раствор соляной кислоты, 0,05 моль/л раствор тиосульфата натрия, 1 %-ный раствор крахмала.
Оборудование: стеклянные палочки, пипетки градуировочные, колбы мерные (объем 50 мл), колбы конические с притертой пробкой (объем 100 мл), воронки стеклянные, бюретки, капельницы, часы.
^ Ход работы. В две мерные колбы вносят по 5 мл раствора сульфата меди, по 5 мл раствора гидроксида натрия и по 2,5 мл раствора фторида натрия. В одну из них (проба) добавляют 5 мл молока, в другую (контроль) – 5 мл дистиллированной воды, перемешивают и доводят дистиллированной водой до объема 50 мл, через 30 мин фильтруют. Затем в конические колбы переносят по 20 мл фильтрата пробы и контроля, вливают по 20 мл раствора йода и, непрерывно перемешивая, по 10 мл раствора гидроксида натрия. Тщательно закрывают. Через 20 мин к содержимому колб добавляют по 10 мл раствора соляной кислоты, по три капли раствора крахмала и титруют раствором тиосульфата натрия до исчезновения окраски, образовавшейся при добавлении крахмала.
|
|
|
Массовую концентрацию лактозы в молоке (мг/мл) рассчитывают по формуле
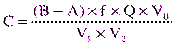 ,
,
где А и В – объемы раствора тиосульфата натрия, затраченные на титрование пробы и контроля;
f – коэффициент поправки на титр 0,05 моль/л раствора тиосульфата натрия;
Q – масса лактозы (18,01 мг), эквивалентная 1 мл 0,05 моль/л раствора тиосульфата натрия;
V0 – общий объем пробы;
V1 и V2 – объемы фильтрата и молока, соответственно, взятые для исследования.
^
|
|
|


