 |
Мессбауэровские параметры зюссита
|
|
|
|
Лабораторная работа № 3
Определение кристаллохимических формул магнитных материалов по данным
Мессбауэровской спектроскопии
I. Цель работы
Освоить расчет кристаллохимических формул магнитных материалов при различном числе обменных связей железа, за счет разупорядочения в структуре, изоморфных примесей и вакансий катионов.
II. Введение
Явление нарушения прямых и косвенных обменных магнитных взаимодействий за счет изоморфных замещений, вакансий и разупорядочения катионов в кристаллической структуре широко распространены как в техногенных магнитоупорядоченных материалах, так и в минералах. При этом возникают неэквивалентные положения ионов железа, которые могут отличаться как по изомерному сдвигу, квадрупольному расщеплению, так и магнитным полям на ядрах Fe57. Примерами могут служить ферриты различного состава, где за счет изоморфных замещений существенно меняются их магнитные характеристики, например в ферритах-шпинелях состава (Fe3-xMex), сплавы на основе железа и немагнитных элементов, например Fe1-xМех, Fe3-хМех, минералы сульфидов из группы пирротина Fe1-хS, в которых за счет различного числа и расположения вакансий рвутся обменные связи и возникают неэквивалентные положения ионов железа с магнитными полями на ядрах Fe57, зависимыми от числа вакансий во второй координационной сфере. Из-за этого определение состава таких соединений часто сопряжено со значительными трудностями. Определенную помощь в ряде случаев при расчете кристаллохимических формул может оказать мёссбауэровская спектроскопия. На примере ферромагнитного магнитного сплава сендаста ниже приведена технология таких расчетов.
|
|
|
III. Физическая сущность методика определения кристаллохимических формул
Известно [1, 2], что во многих случаях по мессбауэровским параметрам определяется координация ионов железа. С другой стороны, между координационными числами и формульными коэффициентами существуют обратные соотношения. Так, в структурах типа АВ к.ч.А = к.ч.В, в структурах АВ2 к.ч.А/к.ч.В =2:1, в общем случае АmВn к.ч.А/к.ч.В=n/m. Особенно успешно такие расчеты реализуются, когда вследствие изоморфных замещений или дефектов рвутся обменные магнитные связи и изменяется состав координационного окружения как в зюссите, или за счет вакансий как, например, у пирротина.
Эти два положения были рассмотрены нами и применены для расчета кристаллохимической формулы исследуемого твердого раствора Fe- Si.
Мёссбауэровский спектр образца природного аналога сендаста (Рис.1), снятый при комнатной температуре, имеет сложную сверхтонкую структуру с двумя наиболее ярко выраженными секстетами, соответствующими двум магнитным подрешеткам от ионов железа с различным числом атомов Fe (4 и 8) в первой координационной сфере [3].
Таблица 1
Химический состав природного аналога сендаста
| Природный аналог сендаста | Элементы | ∑ | ||||
| Fe | Si | Ti | V | Ni | ||
| Содержание, % | 86,34 | 13,52 | 0,002 | 0,23 | 0,09 | 100,10 |
| Кристаллохимическая формула рассчитанная по х/а | Fe3,04V0,1Si0,95 или (Fe, V)3,05Si0,95 |
Дополнительные секстеты, присутствующие в спектрах природного зюссита, обусловлены возникновением неэквивалентных положений атомов железа, имеющих различное число (2, 3, 5, 7) обменных связей Fe-Fe, образующихся за счет статистического распределения части атомов Fe и Si. Мёссбауэровские параметры зюссита приведены в таблице 2. Зависимость химического изомерного сдвига от числа связей (Рис. 2) линейна. Уменьшение изомерного сдвига с ростом числа связей Fe-Fe в структуре объясняется увеличением их ковалентности. Линейную зависимость от числа связей Fe-Fe имеют также магнитные поля на ядрах Fe57 (Рис. 3). С ростом числа связей величина магнитного поля увеличивается, что вполне закономерно.
|
|
|

Рис. 1. Мессбауэровский спктр зюссита (3-8 число обменных связей Fe-Fe).
Таблица 2
Мессбауэровские параметры зюссита
| №№ п.п. | Число связей между центральным ионом Fe полиэдра и лигандами | Изомерный химический сдвиг d, мм/c | Квадрупольный сдвиг D, мм/с | Магнитные поля на ядрах Fe57, кЭ | Ширина линии Г, мм/с | Площади секстипле- тов % отн. |
| 0,47 | 0,04 | 0,35 | 21,2 | |||
| 0,53 | 0,35 | 14,7 | ||||
| 0,56 | -0,05 | 0,35 | 10,8 | |||
| 0,63 | -0,10 | 0,35 | 3,6 | |||
| 0,70 | -0,05 | 0,35 | 39,9 | |||
| 0,73 | -0,01 | 0,35 | 9,8 |

|
|
При этом по величине магнитного поля на ядрах устанавливается число немагнитных атомов в окружении железа, а по площади соответствующей составляющей мёссбауэровского спектра формульные коэффициенты железа. Пользуясь соотношением между к.ч. и формульными коэффициентами, устанавливаются формульные коэффициенты немагнитных элементов, или вакансий [4,5]. Поскольку формулу сендаста можно представить в виде FeS1+ Х , по площадям секстетов можно определить долю неэквивалентных ионов железа каждого типа y, приходящихся на атом железа. Так как во второй координационной сфере у каждого атома железа в структуре сендаста имеется 8 соседей, то при одной оборванной связи на этот атом будет приходиться 0,125 единиц немагнитных атомов, а на у атомов 0,125 у единиц. Таким образом, находятся формульные коэффициенты х немагнитных атомов, приходящиеся на у неэквивалентных атомов железа. В общем случае кристаллохимическая формула таких соединений записывается как:
Fey1(0) Fey2(1) (Me)x2 Fey3(2) (Me)x3...Feyn(n-1) (Me,)xn, (1)
где верхним индексом в скобках указано число оборванных связей Fe-Fe за счет немагнитных атомов или вакансий в окружении атома железа. где: у - формульные коэффициенты неэквивалентных атомов железа; х - формульные коэффициенты приходящихся на них немагнитных атомов. При этом у1+ у2+ у3+... +уi = 1; х1+х2+ х3+...+хj = Х.
|
|
|
Для непосредственно изученного образца природного аналога сендаста формула запишется как:
Fe0,637(0)Fe0,441(1) (Si,V)0,055 Fe0,324(2) (Si,V)0,081Fe0,108(3) (Si,V)0,041 Fe1,196(4) (Si,V)0,598 Fe0,294(5) (Si,V)0,184 (2)
Приведенная к виду Fe3(Si,V)0,959, эта формула достаточно хорошо совпадает с рассчитанной формулой по данным химического анализа - Fe3,04,V0,01 Si 0,95 (табл.1).
Другим примером применения методики, является расчет, когда оборванные магнитные вязи возникают за счет вакансий катионов в структуре минерала, например в пирротинах различных модификаций [4]. На рис. 4. показаны возможные неэквивалентные положения ионов железа в модификациях пирротина 4С, 5С, 6С, 11С.

Рассчитанные значения вклада в магнитные поля на ядрах Fe57 от связи каждого типа позволили найти теоретические значения полей на ядрах атомов железа при любом числе и расположении вакансий в его катионном окружении. Это особенно важно при изучении гексагональных пирротинов, в которых вакансии могут быть как упорядочены, так и неупорядочены, вследствие чего их число в ближайшем катионном окружении атомов железа может быть различным. Расчет значений магнитных полей представлен в таблице 3.
Таблица 3
Магнитные поля на ядрах атомов железа при различном числе вакансий в их второй
координационной сфере
| № п/п | Число и расположение вакансий | Магнитные поля на ядрах Fe57, кэ | Модификация пирротина | ||
| Троилит | Моноклин-ный пирротин | Гексагональ-ный пирротин | |||
1 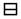
| |||||
2 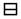
| 4с, 5c, 6c, 11c | ||||
3 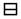
| |||||
1 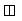
| 290,5 | 5c, 6c, 11c | |||
1 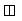 , 1 , 1 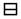
| 287,5 | ||||
1 
| 287,3 | ||||
1 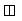 , 2 , 2 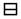
| 284,5 | ||||
1  , 1 , 1 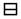
| 284,3 | ||||
1  , 2 , 2 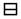
| 281,3 | ||||
2 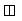
| |||||
2 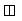 , 1 , 1 
| |||||
1  , 1 , 1 
| 269,8 | ||||
2  , 2 , 2 
| |||||
2 
| 266,5 | 5c, 6c, 11c | |||
2  , 1 , 1 
| 263,5 | ||||
2  , 2 , 2 
| 260,5 | ||||
2  , 1 , 1 
| 4c, 5c, 11c | ||||
3 
| 245,8 | ||||
3  , 1 , 1 
| 242,8 | ||||
3  , 1 , 1 
| 228,3 | ||||
4 
| 4c,5c, 11c |
Примечание:
|
|
|
 - вакансия находится с атомами железа в одной плоскости;
- вакансия находится с атомами железа в одной плоскости;
 - вакансия находится вдоль оси «c» в смежной плоскости;
- вакансия находится вдоль оси «c» в смежной плоскости;
 -вакансия находится в смежной плоскости с углом Fe-S - Fe 135°.
-вакансия находится в смежной плоскости с углом Fe-S - Fe 135°.
Расчет ограничен 4-мя вакансиями во второй координационной сфере атомов железа, поскольку в моноклинном пирротине это максимальное их число, и вероятность, что в неупорядоченном гексагональном пирротине в катионном окружении их может быть больше, мала, так как железистость гексагональных пирротинов больше по сравнению с моноклинным. Полученные данные позволяют установить состав пирротина любого типа.
Мёссбауэровские спектр пирротина представляют сумму секстетов, каждый из которых обусловлен ионами железа с определенным числом вакансий во второй координационной сфере. Неэквивалентные положения Fe характеризуются своими магнитными полями на ядрах. Разложив экспериментальный спектр с помощью компьютерной обработки на составляющие секстеты, по значению магнитных полей на ядрах неэквивалентных ионов железа по таблице 3 можно установить, сколько вакансий в их катионном окружении и как они расположены. Поскольку формулу каждого пирротина можно представить в виде FeS1+ Х , по площадям секстетов можно определить долю неэквивалентных ионов железа каждого типа y, приходящихся на атом железа. Так как во второй координационной сфере у каждого атома железа в структуре пирротина имеется 20 соседей, то при одной вакансии среди них на этот атом будет приходиться 0,05 вакансии, а на у атомов 0,05 у вакансий. Таким образом, находятся формульные коэффициенты вакансий х, приходящиеся на у неэквивалентных атомов железа. Формулу пирротина можно записать в виде:
Fe y1 (1 c ) c x1 Fe y2 (2 c ) c x2 … Fe yi (n c ) c xj, S1+X, (3)
где: у - формульные коэффициенты неэквивалентных атомов железа; х - формульные коэффициенты приходящихся на них вакансий. При этом у1+ у2+ у3+...+уi = 1; х1+х2+ х3+...+хj = Х.
Полученные кристаллохимические формулы позволяют определить состав пирротина в атомных % компонентов, а также дать распределение железа по неэквивалентным позициям.
Правильность методологического подхода определения состава показана на примере упорядоченного гексагонального пирротина Fe9 S10, спектр которого приведен на рисунке 5.
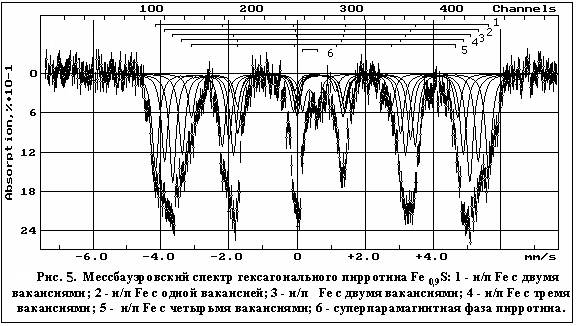
В гексагональном пирротине Fe9S10 (рис. 5) теоретическое отношении ионов Fe различного типа выражается отношением:
Fe(1 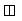 ) : Fe(2
) : Fe(2 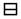 ): Fe(2
): Fe(2  ): Fe(2
): Fe(2  , 1
, 1 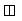 ): Fe(4
): Fe(4  ) = 0,5: 1,5: 1,5: 0,5: 0,5. (4)
) = 0,5: 1,5: 1,5: 0,5: 0,5. (4)
Выполнив расчеты формульных коэффициентов неэквивалентных ионов Fe и соответствующих им вакансий, получим формулу пирротина в виде:
|
|
|
Fe (1 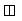 )0, 1(1) c 0,005(5) Fe(2
)0, 1(1) c 0,005(5) Fe(2 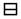 )0,3(3) c 0,003(3) Fe (2
)0,3(3) c 0,003(3) Fe (2  )0,3(3) c 0,03(3) Fe (2
)0,3(3) c 0,03(3) Fe (2  , 1
, 1 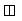 ) c 0,16(6)
) c 0,16(6)
Fe(4  )0,1(1) c 0,02 S1+X, а в кратком виде Fe S1,111, или Fe 0,9 S. (5)
)0,1(1) c 0,02 S1+X, а в кратком виде Fe S1,111, или Fe 0,9 S. (5)
Аналогично можно рассчитать теоретические соотношения концентраций неэквивалентных ионов Fe и соответствующие им соотношения в мёссбауэровском спектре, по которым по можно вывести формулы пирротинов модификаций Fe10 S11 и Fe11S12 [ 4-6].
Порядок проведения работы
1. Открыть мёссбауэроский спектр PrtM для математической обработки из папки «Примеры спектров», «Лабораторная работа №3».
2. Ввести калибровку.
3. Задать модель разложения спектра и запустить программу обработки.
3. Открыть последовательно окна «Результаты», «Таблица» и распечатать результат.
4. Записать в таблицу 4 значения площадей секстетов и магнитных полей.
5. Определить формульные коэффициенты неэквивалентных ионов железа, исходя из формулы пирротина FeS1+x.
6. Установить по полученным магнитным полям и таблицей 3 количество оборванных связей у ионов Fe.
7. Определить коэффициенты пересчета для определения формульных коэффициентов вакансий и записать в таблицу.
8. Определить формульные количества вакансий и записать в таблицу.
9. Выбрать интервал для корректировки модели и произвести обработку спектра
10. Записать расширенную формулу пирротина и сокращенную и записать в таблицу.
11. Сравнить полученную формулу с теоретической и сделать вывод.
12. Оформить лабораторную работу.
Таблица 4
Результаты поэтапного расчета кристаллохимической формулы пирротина по данным
мёссбауэровской спектроскопии
| №№ секстетов. | Площади секстетов % отн | Магнитные поля на ядрах Fe57 | Формульные коэффициенты неэквивалентных ионов Fe | Количество оборванных связей у ионов Fe | Коэффициенты пересчета для определения формульных коэффициентов вакансий | Формульные коэффициенты вакансий. |
| Расширенная кристаллохимическая формула пирротина | ||||||
| Сокращенная формула пирротина |
V. КОнтрольные вопросы
- В каких случаях применима методика определения кристаллохимических формул материалов?
- Чем отличается кристаллохимическая формула вещества от химической?
- Какие мёссбауэровские параметры используются при расчете кристаллохимических формул?
- Что такое координационное число катионов?
- Какова последовательность операций при определении кристаллохимических формул?
- Какую информацию можно получить из мёссбауэровских спектров?
ЛИТЕРАТУРА:
1. Menil F. Systematic trends of 57Fe Mössbauer isomer shifts in (FeOn) and (FeFn) polyhedra. Evidence of a new correlation between the isomer shift and the inductive effect of the competing bond T-X (- Fe) (where X is O or F and T element with a formal positive charge) // J. Phys. and Chem. Solids. 1985. Vol. 46. No 7. P. 763-789.
2. Бенкрофт Г., Меддок Р., Барнс Р. Применение эффекта Мессбауэра к минералогии силикатов. 1. Силикаты железа с известной структурой // Физика минералов, М., Мир, 1971, с. 179-204.
3. Первая находка зюссита на Земле / М.И. Новгородова, Р.Г. Юсупов, М.Т.Дмитриева, В.В.Коровушкин и др. // ДАН СССР, 1983, т. 271, № 6, с. 1480-1483.
4. Коровушкин В.В. Определение состава минералов группы пирротина с количественным распределением ионов железа по неэквивалентным позициям с помощью ЯГР-спектроскопии / Инструкция НСОММИ № 18 ЯГР, М., ВИМС, 1989, 19 с.
5. Коровушкин В.В., Якубовская Н.Ю., Шипко М.Н. Применение мессбауэровской спектроскопии для расчета кристаллохимических формул некоторых минералов и сплавов // Тезисы Всесоюзной конф. «Прикладная мессбауэровская спектроскопия», Казань, 1990, с.126.
6. Коровушкин В.В. ЯГР-спектроскопия в практике геолого-минералогических работ. (Лабораторные и технологические исследования минерального сырья: Обзор) / М., АО «Геоинформмарк». 1993, 39 с.
|
|
|


