 |
Химический элемент и простое вещество
|
|
|
|
Глава 2. МЕТОДИЧЕСКИЕ РАЗРАБОТКИ ПО ТЕМЕ «ВЕЩЕСТВО»
Оборудование. Мультимедийный проектор.
Домашнее задание к уроку. Представления об атомах и элементах у различных ученых (готовится в виде кратких сообщений, желательно с цитатами из работ авторов).
На предыдущем уроке при объяснении домашнего задания было показано несколько слайдов.
ХОД УРОКА
«Распространеннейшие в природе простые тела имеют малый атомный вес, а все элементы с малым атомным весом характеризуются резкостью свойств. Они поэтому суть типичные элементы».
Д.И.Менделеев
Учитель. Первые представления об элементах мы находим уже в греческой науке, но тогда под элементами подразумевались невесовые и невещественные категории. Аристотель рассматривал четыре элемента – землю, воздух, огонь и воду. В средние века алхимики прибавили к ним еще ртуть, серу и соль. Однако только немногие алхимики понимали термин «элемент» в философском смысле Аристотеля. Ошибка была в том, что понятие «элемент» смешивали с понятием «вещество» того же наименования. Подобное часто происходит и у начинающих изучать химию. Таким образом, сформировалась мысль о вещественности элементов, из комбинаций которых состоят разные вещества. Потом появилась мысль о возможности взаимного превращения веществ, например металлов в золото. Неудачи таких попыток постепенно привели алхимиков к мысли, что вещества, не разлагаемые физическими и химическими методами, являются действительно химическими элементами, из которых построены сложные вещества.
1-й ученик. Такую мысль в XVII в. высказывал Р.Бойль. Бойль стремился определить индивидуальность элементов, изучая специфические свойства тел, которые они образуют (реакции осаждения, цветные реакции).
|
|
|
2-й ученик. В XVIII в. эту мысль развил А.Лавуазье.
3-й ученик. Д.Дальтон считал, что все атомы одного химического элемента тождественны между собой. (Он ввел знаки химических элементов.) «Я, – писал Дальтон, – избрал слово атом для обозначения... первичных частиц... потому, что это слово кажется мне значительно более выразительным; оно включает в себя представление о неделимости, чего нет в других обозначениях». Иллюстрируя свое понимание атома, Дальтон приводил такой пример: «…я называю первичную частицу угольной кислоты сложным атомом. Однако, хотя этот атом и может быть разделен, но, распадаясь при таком делении на уголь и кислоту, он перестает уже быть угольной кислотой».
Учитель. Постепенно список «элементов» как результат многовекового опыта по разложению веществ увеличивался, но в этом списке наряду с вещественными сохранялись и невещественные «элементы» – кислород, азот, сера, едкий натр, светород, теплород.
4-й ученик. Первым методом открытия новых «элементов» был анализ минералов, причем критерием нового «элемента» было выделение вещества с новыми реакциями, а затем и самого простого вещества. Иногда промежуток времени между этими этапами составлял десятки лет. Так, фтор в виде соединений был открыт А.М.Ампером в 1810 г., но впервые выделен в виде простого вещества только в 1886 г. А.Муассаном. Это объяснялось также тем, что, с одной стороны, некоторые соединения долгое время принимали за «элементы» (оксиды щелочных металлов), с другой стороны, некоторые простые вещества считали оксидами неизвестных «элементов» (хлор – оксидом «мурия»). Большое количество элементов было открыто путем химического анализа. После введения в химическую практику новых физических методов с помощью электрического тока были выделены калий, натрий и кальций. При помощи спектрального анализа были открыты рубидий и цезий.
|
|
|
5-й ученик. Немецкий ученый Август Кекуле обратился к своему коллеге Карлу Венцелю с предложением организовать международный конгресс для достижения единства в химии и разрешения спорных проблем. Венцелю идея понравилась, и он взял на себя обязанности организатора и устроителя конгресса. К этому был привлечен также Адольф Вюрц, согласившийся вести заседания и быть секретарем. В марте 1860 г. они собрались в Париже и отпечатали обращение ко всем выдающимся химикам. 45 ученых подписали это обращение, среди них значатся известные русские химики Н.Н.Бекетов, Н.Н.Соколов и Н.Н.Зинин.
6-й ученик. Конгресс открылся 3 сентября 1860 г. в Карлсруэ, где Венцель преподавал в Политехническом институте. Участникам конгресса предстояло сделать выбор по тем вопросам, которые имели жизненно важное значение для развития химии в целом. В сущности, речь шла о том, быть ли химии на старых позициях или принять воззрения А.Авогадро и Ш.Ф.Жерара, открывавшие перед ней новые перспективы.
Сторонником первой точки зрения был французский академик, прославленный ученый Ж.Дюма. «Дюма… – писал Д.И.Менделеев, принимавший участие в конгрессе, – старался поставить пропасть между старым и новым, искусственно уладить дело об обозначениях, предлагая в неорганической химии оставить старое обозначение, а в органической – принять новые... При этом Дюма прекрасно характеризовал оба существующие направления. Одно, говорил он, представляет ясное последование за Лавуазье, Дальтоном и Берцелиусом. Исходная точка для ученых этого образа мыслей есть атом, неделимое простое тело; все прочее есть сумма атомов, величина, производная от первой. Другая партия идет по пути… Жерара; она берет готовые тела и сравнивает их; она берет частицы тела, отыскивает изменения и сличает их физические свойства. Первая партия все сделала для минеральной химии, в органической она до сих пор бессильна, потому что здесь химия еще немного может создать из элементов. Вторая партия, несомненно, сильно двинувшая органическую химию, ничего не сделала для минеральной». Дюма, свидетельствует далее Менделеев, призывал и тех и других идти своей дорогой.
|
|
|
7-й ученик. Сторонником другой точки зрения был Станислао Канниццаро. Его речь потрясла слушателей. «Я не могу… передать того воодушевления, той здравой энергии, вполне сложившегося убеждения, которые так могущественно действовали на слушателей», – отзывался о речи Канниццаро Менделеев. На конгрессе Канниццаро раздал оттиски своей книги «Краткое изложение курса химической философии». Читатели были поражены четкостью изложения, убедительностью, с которой устранялись разногласия, и открывавшимися в связи с этим перспективами развития экспериментальной науки. «Я читал книгу неоднократно и был поражен ясностью, с какой она освещала важнейшие спорные вопросы, – писал тогда известный химик Лотар Мейер. – С моих глаз как бы спала пелена, исчезли сомнения, и вместо них возникло чувство самой спокойной уверенности».
Гипотезу Авогадро Канниццаро назвал краеугольным камнем развития атомной теории Дальтона, которая, основываясь только на весовых и объемных соотношениях, становилась непригодной для экспериментальных исследований. Не надо удивляться, утверждал он, необходимости в гипотезе Авогадро для понимания законов. Именно неприятие идей Авогадро и привело к неудачам многих химиков и даже такого прославленного ученого, как Берцелиус.
Канниццаро c огромным воодушевлением произнес свою речь, и члены конгресса, несмотря на те несогласия, которые были между ними до этого, встретили ее почти единодушным одобрением. Когда предложили резолюцию, в которой характеризовалось различие понятий частицы (молекулы) и атома, то все проголосовали «за». Лишь одна чья-то рука робко поднялась при вопросе «кто против?», но и она тут же опустилась.
После конгресса в Карлсруэ отошли в прошлое разногласия, стоявшие на пути развития экспериментальных определений в химии, а атомный вес стал важнейшей характеристикой элемента.
8-й ученик. М.В.Ломоносов писал: «Элемент есть часть тела, не состоящая из каких-либо других меньших тел». Ломоносов более чем на сто лет опередил всех химиков Европы. В своей незавершенной работе «Элементы математической химии» он дал представление о строении вещества, подобное тому, что приняли химики лишь после конгресса в Карлсруэ. Он писал, что «корпускула (так он называл молекулу) – собрание элементов (т.е. атомов) в одну незначительную массу. Корпускулы однородны, если состоят из одинакового числа одних и тех же элементов, взаимосоединенных одинаковым образом. Корпускулы разнородны, когда элементы их различны и соединены разным образом или в различном числе; от этого зависит бесконечное разнообразие тел. Начало есть тело, состоящее из однородных корпускул».
|
|
|
Учитель. Именно потому, что научная истина не есть то, что принимается голосованием, положение в химии после конгресса не стало идиллическим. Борьба продолжалась. Одни были полностью «за» атомно-молекулярную теорию; другие принимали ее постольку, поскольку она казалась неплохим «инструментом» познания; третьи не признавали ее совсем. И так до тех пор, пока атом не стал для науки реальностью.
Съезд химиков явился толчком к дальнейшему движению, в частности к созданию периодического закона. Менделеев писал: «Главное понятие, с которым возможно приступить к объяснению периодической закономерности, состоит именно в коренном различии представлений об элементах и простых телах… Понятия и слова «простое тело» и «элемент» нередко смешивают между собою... Простое тело есть вещество, металл или металлоид, с рядом физических признаков и химических реакций... Под именем элемент должно подразумевать материальные составные части простых и сложных веществ…»
Этим понятием мы пользуемся и в настоящее время, хотя физический смысл его объясняем на основании современных представлений о строении атома.
Презентация элементов 1–3-го периодов
Выберите интересующий вас элемент.

Выбираем элемент углерод 6С.

На примере углерода учитель объясняет различие понятий «элемент» и «простое вещество».
Углерод – это элемент, который существует в природе либо в виде алмаза, известного всем драгоценного камня, либо в виде не менее известного графита. Углерод – один из немногочисленных элементов «без роду, без племени». История общения человека с этим веществом уводит во времена доисторические. Имя первооткрывателя углерода неизвестно, неизвестно и то, какая из форм элементарного углерода – алмаз или графит – была открыта раньше.
Люди не сразу пришли к пониманию того, что благороднейший алмаз и невзрачный уголь – близнецы. Между тем, установить это было совсем просто: в один прекрасный день с помощью линзы сконцентрировали солнечные лучи на кристаллике алмаза, помещенного под стеклянный колпак. Алмаз... сгорел, а под колпаком образовался углекислый газ – тот же самый, что образуется при горении угля.
|
|
|
И графит, и алмаз состоят из одинаковых углеродных атомов. Любой кристалл алмаза, даже огромный, шестисотграммовый «Куллинан», – это по существу одна молекула, состоящая из идеально упакованных атомов углерода.
Особенности молекулярного строения объясняют огромную разницу в свойствах графита и алмаза. Графит мягкий, легко расслаивается, алмаз – самое твердое вещество в природе.
Графит отлично проводит тепло и электричество, алмаз — изолятор.
Графит совершенно не пропускает света, алмаз прозрачен.
Существует более 6,5 млн веществ, называемых органическими. Что их объединяет? Представьте себе, во всех органических веществах обязательно есть элемент углерод!
Углерод – алмаз
Прозрачные кристаллы, после огранки превращаются в бриллианты.

Решетка кубическая, а = 3,5 нм.
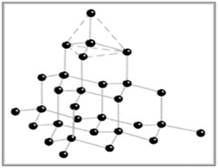
Углерод – графит
Вещество черного цвета с металлическим блеском.

Решетка гексагональная, а = 2,45 нм, с = 6,7 нм.

Проверка усвоения знаний
Натрий 11Na – элемент и вещество. Просмотрите презентацию и определите, где речь идет об элементе, а где о веществе.

Натрий по своей распространенности в природе занимает 6-е место среди элементов. Присутствует в атмосфере Солнца и в межзвездном пространстве. Содержание натрия в земной коре – 2,3%, в морской воде – 1,05%.
Натрий входит в состав человеческого организма, в крови содержится около 0,6% NаСl. Осмотическое давление крови поддерживается на необходимом уровне в основном за счет хлорида натрия.
Наибольшее количество натрия связано в соединении с хлором. Соль, или, как ее называют химики, хлорид натрия, образует мощные отложения. В год каждый человек с пищей потребляет от 8 до 10 кг соли. Недаром говорят: «Чтобы узнать человека, надо с ним пуд соли съесть». Оказывается, это не так уж много и по весу, и по времени: за год вдвоем и будет съеден пуд
(16 кг) соли.
Огромные количества соли содержат в себе воды морей и океанов. Солью, извлеченной из морских вод, можно было бы засыпать всю сушу земного шара слоем в 130 м. Так велико количество соли!
Интересный факт установили канадские ученые из медицинского университета в Торонто. У вспыльчивых, раздражительных людей натрий усваивается плохо и быстро выводится из организма, а у спокойных и доброжелательных постоянно испытывающих положительные эмоции, этот элемент усваивается хорошо.
Натрий – это легкоплавкий металл серебристо-белого цвета, на воздухе легко покрывается пленкой, состоящей из карбонатов, оксидов и гидроксидов.
Решетка кубическая, а = 4,28 нм.

Итоги урока формулируются и записываются в тетрадь в виде современных определений понятия «элемент» и «простое вещество».
Путешествие в мир веществ
Вступительное слово
Учитель. Вы пришли в необычный кабинет (подчеркнуть необычность кабинета, показать таблицы, химическую посуду, склянки с химическими реактивами и т.п.). В этом кабинете происходят таинственные вещи. Прежде чем показать вам интересные опыты, мы выясним, чем же занимаются в этом кабинете. Сначала ответьте на вопросы.
Как назвать одним словом все то, что нас окружает? Город? Страна? Земля? Вселенная? (Природа.)
Из чего состоит окружающая нас природа? (Парты, окошки, деревья – это тела.)
Из чего состоят тела? (Демонстрация предметов из стекла и дерева.) (Тела состоят из материала, вещества.)
Учитель пишет на доске: Природа – Тела – Вещества.
Учитель. Химия – наука о веществах. В этом кабинете изучают вещества. Веществ очень много, и все они разные. Одни твердые, другие жидкие, третьи газообразные. Одни вредные, другие полезные, третьи – опасные… (демонстрация рисунков). Словом, с веществами необходимо работать, соблюдая меры предосторожности. Существует очень много правил, называются они «Правила техники безопасности». Эти правила являются результатом многовекового общения человека с веществом. Неправильное обращение с веществами приводит к страшным последствиям.
Практическая часть
(Демонстрация и объяснение опытов)
1. «Дым без огня»
О б о р у д о в а н и е и р е а к т и в ы. Два стеклянных цилиндра (или стакана) с крышками, 25%-й водный раствор аммиака, концентрированная соляная кислота.
П р о в е д е н и е о п ы т а. В один чисто вымытый цилиндр налейте несколько капель концентрированной соляной кислоты, а в другой – раствор аммиака. Оба цилиндра закройте крышками и поставьте друг от друга на некотором расстоянии. Перед опытом следует показать, что цилиндры «пустые». Во время демонстрации цилиндр с соляной кислотой (на стенках) переверните вверх дном и поставьте на крышку цилиндра с аммиаком. Крышку уберите. Внутри цилиндра образуется белый дым – признак химической реакции.
2. «Химическое молоко»
О б о р у д о в а н и е и р е а к т и в ы. Два химических стакана, растворы хлорида бария и серной кислоты.
П р о в е д е н и е о п ы т а. Слить растворы хлорида бария и серной кислоты. Частицы образовавшегося белого осадка, не успев осесть, создают эффект молока.
3. «Химическая хирургия»
О б о р у д о в а н и е и р е а к т и в ы. Деревянная линейка, ватка, растворы хлорида железа(III) и роданида калия.
П р о в е д е н и е о п ы т а. Пригласить самого смелого. Смочить вату хлоридом железа(III) и протереть руку. Деревянную линейку смочить роданидом калия. При соприкосновении этих веществ образуется раствор кровавого цвета. Смыть раствор и показать ребятам отсутствие следов пореза.
4. «Цвет по волшебству»
О б о р у д о в а н и е и р е а к т и в ы. Химический стакан, растворы щелочи, фенолфталеина, серной кислоты, лакмуса.
П р о в е д е н и е о п ы т а. В раствор щелочи добавьте фенолфталеин, покажите малиновую окраску. Прилейте серную кислоту, покажите, что раствор в стакане снова стал бесцветным. Добавьте фиолетовый лакмус и получите снова красную окраску.
5. «Черный удав из стакана»
О б о р у д о в а н и е и р е а к т и в ы. Сахарная пудра, вода, концентрированная серная кислота (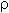 = 1,84 г/см3), два химических стакана на 100–150 мл, мензурка, стеклянная палочка, весы, разновесы.
= 1,84 г/см3), два химических стакана на 100–150 мл, мензурка, стеклянная палочка, весы, разновесы.
П р о в е д е н и е о п ы т а. Взвесьте на весах 30 г сахарной пудры и перенесите ее в химический стакан. Отмерьте мензуркой 12 мл концентрированной серной кислоты. Осторожно смешайте в стакане стеклянной палочкой сахар и кислоту в кашеобразную массу (стеклянную палочку тотчас выньте и поместите в стакан с водой). Через некоторое время смесь чернеет и разогревается, и вскоре из стакана начинает выползать пористая угольная масса*.
(Обугливание сахара и других углеводов серной кислотой объясняется окислительными свойствами концентрированной серной кислоты. Восстановителем является углевод, процесс экзотермический. Выделяющиеся газы и пары воды вспучивают угольную массу, которая поднимается в стакане.)
6. «Вулкан на столе»
О б о р у д о в а н и е и р е а к т и в ы. Коническая колба, фарфоровый тигель или чашка, лучинка, спички, дихромат аммония, спирт.
П р о в е д е н и е о п ы т а. В горло конической колбы вставьте тигелек или фарфоровую чашку. (Колбу можно покрыть пластилином, придав ей форму горы, или изготовить макет сопки.) Под колбу или макет положите большой лист бумаги для сбора оксида хрома(III). В тигелек насыпьте дихромат аммония, в центре холмика смочите его спиртом. Зажигается «вулкан» горящей лучинкой. Реакция экзотермическая, протекает бурно, вместе с азотом вылетают раскаленные частички оксида хрома(III). Если погасить свет, то создается впечатление извергающегося вулкана, из кратера которого выливаются раскаленные массы.
В завершение опытов подарить каждому полоску универсальной индикаторной бумажки, которая меняет свой цвет в зависимости от среды раствора, и предложить дома капнуть на нее водой из-под крана, соком лимона и раствором соды.
Напутственные слова
Учитель. Самое интересное в окружающем нас мире – это то, что он очень сложно устроен и к тому же постоянно изменяется. Каждую секунду в нем происходит неисчислимое множество химических реакций, в результате которых одни вещества превращаются в другие. Человек сделал вдох – и в организме начались реакции окисления органических веществ. Он сделал выдох – и в воздух попал углекислый газ, который затем поглотится растениями и в них превратится в углеводы. Некоторые реакции мы можем наблюдать непосредственно, например ржавление железных предметов, свертывание крови, сгорание автомобильного топлива. Однако подавляющее большинство химических процессов остаются невидимыми, но именно они зачастую определяют свойства окружающего мира. Чтобы управлять превращениями веществ, необходимо как следует разобраться в природе подобных реакций. Для этого и нужна химия.
Химия занимает особое место среди наук о природе. Она обладает фантастической созидательной силой. Часть веществ (кислород, вода, белки, углеводы, нефть, золото и др.) дана нам природой в готовом виде, другую часть (например, асфальт или искусственные волокна) человек получил сам из природных веществ. Но самую большую группу составляют вещества, которых раньше вообще не существовало, и человек синтезировал их самостоятельно. В этом и заключается уникальность химии: она не только изучает то, что дано природой, но и сама постоянно создает для себя все новые и новые объекты исследования. В этом отношении химии нет равных среди других наук.
Мир веществ разнообразный, причудливый и таинственный. Окунуться в богатство химического знания вы пока не можете. Но у вас все впереди.
Глава 3.ДИДАКТИЧЕСКИЕ КАРТОЧКИ ПО ТЕМЕ «ВЕЩЕСТВО»
вещество химический элемент
1. Химические явления – это
...............................................................................................................
...............................................................................................................
...............................................................................................................
2. Вещество – это
...............................................................................................................
...............................................................................................................
...............................................................................................................
3. Выпишите только химические явления из приведенного ниже списка: испарение воды, окисление меди, нагревание воды, горение топлива, плавление железа, гниение дров, ржавление железа.
...............................................................................................................
...............................................................................................................
...............................................................................................................
Знаки химических элементов
1. Напишите химические знаки следующих элементов:
водород, кальций, углерод, натрий, фосфор, калий, азот, магний, кислород, медь, хлор, железо, сера, алюминий, кремний, цинк, бром, марганец................................................................................................................
...............................................................................................................
...............................................................................................................
Подчеркните знаки химических элементов, молекулы которых двухатомны.
2. Запишите с помощью символов химических элементов, индексов и коэффициентов:
две молекулы азота ……………..; пять атомов хлора ……………..
Химические формулы
1. Что называется относительной молекулярной массой?
...............................................................................................................
...............................................................................................................
...............................................................................................................
2. Найдите относительную молекулярную массу следующих веществ: Н3РО4, Са(ОН)2, СuSO4.
...............................................................................................................
...............................................................................................................
...............................................................................................................
3. Определите массовую долю каждого элемента в соединении СuSО4.
...............................................................................................................
...............................................................................................................
...............................................................................................................
Строение атома
1. В чем заключается физический смысл номера периода?
...............................................................................................................
...............................................................................................................
...............................................................................................................
2. Составьте схему строения атома кремния, напишите электронную конфигурацию, определите число протонов, нейтронов и электронов.
...............................................................................................................
...............................................................................................................
...............................................................................................................
Химическая связь
1. Какая связь называется ковалентной?
...............................................................................................................
...............................................................................................................
...............................................................................................................
2. Укажите виды химической связи в следующих веществах:
Вr2 ……………………….; ZnO …………………………………..;
NH3 ………………………; Mg …………………………………....
Соединения химических элементов
1. Что называется степенью окисления?
...............................................................................................................
...............................................................................................................
...............................................................................................................
2. Определите степень окисления каждого элемента в сложных веществах из следующего списка:
ОF2, N2O3, Cl2, H2CO3, NaOH.
Выпишите формулы бинарных соединений и назовите эти соединения.
...............................................................................................................
...............................................................................................................
...............................................................................................................
Основные классы неорганических соединений
1. Дайте характеристику серной кислоты
...............................................................................................................
...............................................................................................................
...............................................................................................................
2. Какие оксиды соответствуют следующим кислотам:
угольная – ………………………; фосфорная –.
3. Из предложенного перечня веществ:
H2S, K2O, LiOH, MgSO4, HNO3
выпишите отдельно и назовите:
оксиды – …………………………………………………………….….;
кислоты – …………………………………………………………...….;
основания – ……………………………………………………………...
ЛИТЕРАТУРА
О. В. Байдалина. О прикладном аспекте химических знании // Химия в школе, 2005, № 5, с. 45-47.
Ахметов Н. С. Методика преподавания темы «Закономерности протекания химических реакций» // Химия в школе. 2002, № 3, с. 15 – 18.
Ахметов Н. С. Учебник для 8 класса общеобразовательных учреждений. М.: Просвещение, 1998 г.
Рудзитис Г. Е., Фельдман Р. Г. Учебник для 8 класса средней школы. М.: Просвещение, 1992.
Материалы сайта www.1september.ru
О. С. Габриелян, Н. П. Воскобойникова, А. В. Ящукова. Настольная книга учителя. Химия. 8 класс. М.: Дрофа, 2003 г.
Малинин К. М. Технология серной кислоты и серы. М., Л., 1994.
Васильев Б. Г., Отвагина М. И. Технология серной кислоты. М., 1985.
Отвагина М. И., Явор В. И., Сретенская Н. С., Шарифов М. Ю. Промышленность минеральных удобрений и серной кислоты. М., НИИТЭХИМ. 1972. Выпуск № 4.
Резницкий И. Г. Возможности использования нитрозного способа для переработки газов автогенных процессов на серную кислоту / Цветные металлы. 1991. № 4.
Березина Л. Т., Борисова С. И. Утилизация фосфогипсов - важнейшая экологическая проблема // Химическая промышленность. 1999 г. № 12.
Громов А. П. Экологические аспекты производства серной кислоты // Экология и промышленность России. 2001, № 12.
Лидин Р. А. Химия: Руководство к экзаменам / Р. А. Лидин, В. Б. Маргулис. – М.: ООО Издательство «АСТ»: ООО «Издательство Астрель», 2003. с. 64 – 70.
Единый государственный экзамен 2002: Контрольные измерительные материалы: Химия / А. А. Каверина, Д. Ю. Добротин, М. Г. Снастина и др.; М.: Просвещение, 2002. – с. 39 – 51.
Химия: Большой справочник для школьников и поступающих в вузы / Е. А. Алферова, Н. С. Ахметов, Н. В. Богомолова и др. М.: Дрофа, 1999. с. 430-438
Р. П. Суровцева, С. В. Сафронов. Задания для самостоятельной работы по химии. М.: Просвещение, 1993 г.
Размещено на
|
|
|


