 |
Физико-химические свойства
|
|
|
|
Фазовая диаграмма нитрида бора, равно как и диаграмма состояния системы B-N, не разработана. В литературе имеются сведения, что, кроме нитрида бора BN, в этой системе существуют и другие соединения бора с азотом: триазид бора B(N3) 3 и, возможно, низший нитрид бора B3N.
Химический Анализ кристаллов боразона показал, что они содержат 41,5% (вес.) бора и 50,1% (вес.) азота (теоретический состав BN: 43,6% бора и 50,4% азота). Анализ проводили, растворяя боразон в расплаве NaOH (с титрованием образующегося аммиака), поскольку на него не действуют ни одна из обычных кислот.
Кристаллы боразона не изменяются при нагреве в вакууме до температуры выше 2000 ˚С. При нагреве на воздухе медленное окисление боразона наблюдалось лишь при 2000 ˚С, тогда как алмаз сгорает на воздухе уже при 875 ˚С.
При нагреве боразона под давлением в 40000 атм. Наблюдался переход его в гексагональный нитрид бора при 2500 ˚С.
Боразон кристаллизуется в структуре цинковой обманки (сфалерита) с периодом решетки 3,615±0,001 Ả при 25 ˚С.
Кристаллы боразона, полученные при аллотропическом переходе
BN (гекс.) → BN (куб.) при высоких давлениях, имеют вид полиэдров, обычно тетраэдров или октаэдров. Они прозрачны, а их цвет зависит от наличия тех или иных примесей. Так, бор окрашивает кристаллы боразона, полученного из смесей, в коричневый или черный цвет, бериллий – в синий, сере – в желтый. Желтую окраски имеют также кристаллы боразона, полученного из смеси гексагонального нитрида бора с нитридом лития. Были получены также красные, белые и бесцветные кристаллы.
Плотность боразона составляет 3,45 г/см3 (ренгеновская плотность 3,47 г/см3). Твердость его при оценке по шкале Мооса оказалась соизмеримой с твердостью алмаза (10 баллов).
|
|
|
Данные о некоторых свойствах нитрида бора приводятся в табл. 1.
| Соединение | Т пл., ˚С | Теплота образования ккал/моль | Период решетки Ả | Удельный вес г/см3 | Микротвердость Кг/мм2 | Твердость по шкале Мооса | Ширина запрещенной зоны, эВ | Т.Э.Д.С. МкВ/гра. |
| BN(куб.) | ~3000 | - | 3,615 | 3,45 | - | 10 | ~5 (теор.) | - |
Таблица 1.
Электрические и оптические свойства
Измерение спектра отражения кубического нитрида бора (полученного с применением нитрида лития в качестве ’’катализатора’’), показали, что кристаллы обладают большим поглощением в интервалах от 7 до 9 эВ. Общий вид спектра поглощения похож на спектр поглощения алмаза, но характеризуется энергией, приблизительно на 2 эВ больше. Показатель преломления кубического нитрида бора составляет 2,22.
Зонная структура кубического нитрида бора рассчитана теоретически из зонной структуры алмаза методами теории возмущения (рис. 3). Максимум валентной зоны остается в точке  = 0, однако минимум валентной зоны проводимости оказывается смещенным по оси. В результате значение ΔЕ возрастает до ~10 эВ, вдвое превышая значение ΔЕ для алмаза.
= 0, однако минимум валентной зоны проводимости оказывается смещенным по оси. В результате значение ΔЕ возрастает до ~10 эВ, вдвое превышая значение ΔЕ для алмаза.
Исследуя влияние примесей на проводимость боразона показало, что присутствие в реакционной смеси металлического бериллия или его соли (от 0,01 до 1% (вес.)) способствует образованию кристаллов BN с проводимостью р – типа
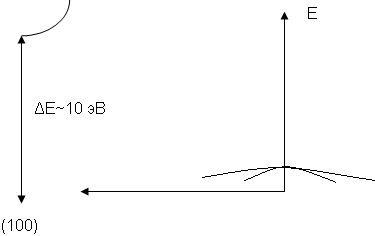
Рис. 3. Зонная структура кубического нитрида бора.
Такие кристаллы обладали сопротивлением 103 ом·см, хотя иногда наблюдались и такие низкие сопротивления, как 2·102 ом·см при комнатной температуре. Значение энергии активации проводимости колебалось в зависимости от индивидуальности измеряемого кристалла (а возможно также и за счёт влияния контактов). На основе опыта по легированию других соединений типа AIIIBV предполагается, что атомы бериллия могут замещать атомы бора или азота в решётке кубического нитрида бора.
|
|
|
Попытки создать в кристаллах боразона, полученных из системы B-N-Li, дырочную проводимость за счет добавки в реакционную смесь магния или цинка, не дали хороших результатов. Это, вероятно, связано с относительно большими размерами атомов указанных элементов и трудностью замещения ими атомов в структуре боразона.
Проводимость n-типа удавалось получить в кристаллах боразона при добавке в реакционную смесь избытка бора, а также серы, кремния и др.
Добавка бора придавала кристаллам тёмно-коричневую окраску. Такие кристаллы имели высокое удельное сопротивление.
Однако наиболее активное донорное действие проявила сера в количестве 0,3-3% оказалось возможным получить кристаллы, удельное сопротивление которых было 104 Ом ·см и иногда даже 103 Ом · см при 250С. Предполагают, что атомы серы замещают атомы азота в кубическом нитриде бора. Энергия ионизации примесных центров равнялась 0,05 эВ.
При добавке в реакционную смесь соединений, содержащих углерод и азот, удавалось получить кристаллы с проводимостью n-типа, имевшие сопротивление 105-107 Ом · см и энергию активации проводимости 0,28-0,41 эВ. Такие кристаллы имели жёлтую, коричневую или красно-коричневую окраску.
Наконец, электронная проводимость иногда наблюдалась на кристаллах боразона, полученных из реакционных смесей нитрид лития – нитрид бора или нитрид магния- нитрид бора без преднамеренно введенных легирующих добавок. Эти кристаллы обычно имели высокие сопротивления – порядка 106-109 Ом · см при комнатной температуре. Возможно, что причиной электронной проводимости в этом случае служил кислород, который было очень трудно исключить из реакционной смеси ввиду высокой активности нитридов, входивших в шихту. Указанное предположение согласуется с тем, что использование в качестве катализатора нитрида магния, являющегося более сильным раскислителем, чем нитрид лития, получились более высокоомные кристаллы боразона. Исследование выпрямляющих свойств кристаллов кубического нитрида бора производились на паре кристаллов n-и p-типа, находящихся в контакте. Через такую пару пропускался слабый постоянный ток (10-6а) при низком напряжении (5в) с помощью серебряных контактов.
|
|
|
Отношение прямого тока к обратному было довольно низким – от 2 до 20.
При 250 С самые большие токи пропускали так, что p-кристалл был положительным. Однако при температурах 300-4000 С направление выпрямления менялось для некоторых пар кристаллов. При охлаждении устанавливалось первоначальное направление выпрямления.
Дальнейший прогресс в изучении свойств кубического нитрида бора связан с получением крупных кристаллов подходящей формы, а также с разработкой технологии получения p-n-переходов.
Применение боразона.
Нитрид бора и материалы на его основе занимают заметное место в ряду важнейших инструментальных материалов и являются основой многих современных технологий Основанием для широкого применения нитрида бора в инструментах, послужила наибольшая твёрдость, приближающаяся к твёрдости алмаза. Термодинамические особенности полиморфизма нитрида бора обусловили появление большого количества материалов на основе его плотных модификаций и различных технологий его получения.
Во «ВНИИАЛМАЗ» разработана технология получения двухслойных пластин на основе кубического нитрида бора, обеспечивающая высокую твёрдость режущего слоя(28-30 ГПа), высокую термостойкость (более 12000) и стабильность качества. Разработанные и выпускаемые «ВНИИАЛМАЗ» режущие пластины на основе кубического нитрида бора рекомендуются для высокопроизводительного точения (гладкого и с ударом) закаленных сталей, серого, высокопрочного и отбеленного чугуна, для обработки стального и чугунного литья по литейной корке и других сверхтвёрдых материалов, а также фрезерования чугунов. Достоинством двухслойных пластин из кубического нитрида бора, производимых ВИИНИАЛМАЗом, является их высокая износостойкость, не уступающая зарубежным аналогам, и большой размер пластин (15 мм), позволяющий изготавливать резцы с большой режущей кромкой для обработки деталей из чугуна с глубиной резания, достигающей 6 мм на сторону при высоких скоростях резания 600м/мин. Это обеспечивает высокую производительность обработки, недостижимую для твёрдосплавных резцов.
|
|
|
Также нитрид бора нашёл широкое применение в реакциях промышленного органического синтеза и при крекинге нефти, в изделиях высокотемпературной техники, в производстве полупроводников, получении высокочистых металлов, газовых диэлектриков, как огнетушащее средство.
Нитрид бора входит в состав получения промышленной керамики.
Боразон предназначен для:
· изготовления изделий, применяемых в высокотемпературной технике (тигли, изоляторы, тигли для получения полупроводниковых кристаллов, детали электровакуумных приборов);
· производства полупроводниковых приборов и интегральных схем (твердотельные планарные источники примеси бора, диэлектрические прокладки конденсаторов);
· деталей электровакуумных приборов (окон выводов энергии, стержней теплоотводов).
РАСЧЁТНАЯ ЧАСТЬ
Таблица данных взятых из справочника:
| Δ H298, кДж/моль | Δ S298, Дж/моль | Δ G 298 , кДж/моль | Ср Дж/моль | |
| BN | 648 | 212 | 615 | 19.7 |
| PH 3 | -5 | 210.2 | - | 31 |
| NH 3 | -46.2 | 192.6 | - | 50.3 |
| BP | 455 | 202.1 | - | - |
Рассчитаем тепловой эффект, энтропию, изменение стандартной энергии Гиббса при Т=2980 К и стандартном давлении для следующей реакции по формулам, используя таблицу данных.
BP+NH3 → BN(k)+PH3
ΔH298=∑nΔH298прод.-∑nΔH298исх.
ΔH298=(648+(-5))-(455+(-46,2))=234,2 · 103 Дж/моль
ΔS298=∑n ΔS298прод.- ∑n ΔS298исх.
ΔS298=(212+210,2)-(202,1+192,6)=27,6 Дж/моль
ΔG298= ΔH298-T · ΔS298
ΔG298=234,2 · 103-298·27,6=151 кДж/моль
Теперь рассчитаем всё тоже самое, но только в интервале температур 2980±150К и построим график зависимости ΔG=f(T).
ΔHT= ΔH298+∫298ΔCp dT
ΔST= ΔS298+∫298ΔCp/T dT
ΔGT= ΔHT- TΔST
Расчет:
ΔH283=648+19.7(283-298) = 352.5 кДж/моль
ΔH288=648+19.7(288-298) = 451 кДж/моль
ΔH293= 648+19.7(293-298) =623, 3 кДж/моль
ΔH298=648+19.7(298-298) =648 кДж/моль
ΔH303=648+19.7(303-298) =746, 5 кДж/моль
ΔH308=648+19.7(308-298) =845 кДж/моль
ΔH 313=648+19.7(313-298) =943.5 кДж/моль
ΔH318=648+19.7(318-298) =985 кДж/моль
ΔS283=27,6+19.7(ln283- ln 298)=26.61 кДж/моль
ΔS288=27,6+19.7(ln 288- ln 298)=27.01 кДж/моль
ΔS293=27,6+19.7(ln 293- ln 298)=27.4 кДж/моль
ΔS298=27,6+19.7(ln 298- ln 298)=27.6 кДж/моль
ΔS303=27,6+19.7(ln 303- ln 298)=28.7 кДж/моль
ΔS308=27,6+19.7(ln 308- ln 298)=28.9 кДж/моль
ΔS313=27,6+19.7(ln 313- ln 298)=29.3 кДж/моль
ΔS318=27,6+19.7 (ln 318- ln 298)=29.6 кДж/моль
ΔG283=352.5*103-283*26.61=345 кДж/моль
ΔG288=451-288*27.01=443.3 кДж/моль
ΔG293=623, 3-293*27.4=615.2 кДж/моль
ΔG298=648-298*27.6=639.7 кДж/моль
ΔG303=746, 5 -303*28.7=737.3кДж/моль
ΔG308=845-308*28.9=835.6кДж/моль
ΔG313=943.5 -313*29.3=933.3кДж/моль
ΔG318=985-318*29.6=975.4кДж/моль
T, K
 |
 318
318
 283
283
 |
300 1000
ΔG, кДж/моль
Построили график зависимости ΔG=f(T), из него видно, что с увеличением температуры растет ΔG(в выбранном интервале).
|
|
|
ЗАКЛЮЧЕНИЕ:
На основе проделанной работы можно сделать вывод о том, боразон, как соединение типа AIIIBV на основе бора, обладает высокой химической стойкостью, большой шириной запрещённой зоны, малой энергией ионизации примесных центров. Получение боразона связано с технологическими трудностями (использование техники сверхвысоких давлений). Его свойства на данный момент не до конца изучены, но уже сейчас можно говорить о том, что он является удачным материалом для полупроводниковых приборов, предназначенных для работы в широком интервале температур.
ЛИТЕРАТУРА:
|
|
|


