 |
Получение альдегидов и применение альдегидов.
|
|
|
|
Тема 3.3. ««Кислородсодержащие органические соединения»
Карбонильные соединения. Альдегиды.
План.
- Карбонильные соединения: альдегиды, кетоны. Номенклатура, изомерия.
- Строение, физические и химические свойства альдегидов.
- Получение, применение альдегидов.
- Особенности свойств кетонов.

1. К карбонильным соединениям относятся соединения, содержащие карбонильную группу (карбонил, окси-группу).

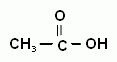
 Эти соединения, в зависимости от связанных с ней заместителей, делятся на две основные группы: альдегиды и кетоны. Альдегиды содержат карбонильную группу, которая связана с первичным атомом углерода, т.е. находится в начале углеродной цепи. Кетоны содержат карбонильную группу, которая связана со вторичным атомом углерода, т.е. находится в середине углеродной цепи. Карбоновые кислоты кроме карбонильной группы имеют еще и гидроксогруппу, причем обе функциональные группы связаны с одним (первичным) атомом углерода.
Эти соединения, в зависимости от связанных с ней заместителей, делятся на две основные группы: альдегиды и кетоны. Альдегиды содержат карбонильную группу, которая связана с первичным атомом углерода, т.е. находится в начале углеродной цепи. Кетоны содержат карбонильную группу, которая связана со вторичным атомом углерода, т.е. находится в середине углеродной цепи. Карбоновые кислоты кроме карбонильной группы имеют еще и гидроксогруппу, причем обе функциональные группы связаны с одним (первичным) атомом углерода.
В этой лекции мы рассматриваем альдегиды и кетоны. В зависимости от природы углеродного радикала различают алифатические и ароматические карбонильные соединения, а также предельные и непредельные.





Функциональная группа у альдегидов находится на конце углеродной цепи, у первичного атома углерода. Она является главной функциональной группой (других нет) и счет атомов идет от нее. Карбонильная группа в названии альдегида обозначается добавлением суффикса –аль. Цифра в названии не указывается, ведь это всегда первый атом углерода. Т.е. изомерии функциональной группы для альдегидов нет. Возможна только изомерия углеродного скелета и межклассовая изомерия с кетонами. У кетонов оксо-группа указывается добавлением суффикса –он. Кроме того, надо указать, где находится эта группа. Эта цифра должна быть как можно  меньше.
меньше.
|
|
|

 Например:
Например:
 Метаналь (формальдегид, муравьиный альдегид) Этаналь (ацетальдегид, уксусный альдегид)
Метаналь (формальдегид, муравьиный альдегид) Этаналь (ацетальдегид, уксусный альдегид)
 2-метилгексанон-3.
2-метилгексанон-3.
Пропаналь (пропионовый альдегид)
Пропанон

 Бутаналь (масляный альдегид)
Бутаналь (масляный альдегид)
Метилпропаналь
Физические свойства.
Карбонильные соединения не образуют водородных связей, поэтому температуры кипения у них ниже, чем у соответствующих спиртов. Метаналь – газ, все другие низшие альдегиды – жидкости, высшие – твердые вещества. Низшие альдегиды летучи и имеют характерный запах. Они растворимы в воде. Водный 40% раствор метаналя называют формалином. Этаналь летучая жидкость (температура кипения 210С), с неприятным удушливым запахом (в малых концентрациях он пахнет яблоками).
Особенности строения.  Атом углерода карбонильной группы находится в состоянии sp2 гибридизации и образует три
Атом углерода карбонильной группы находится в состоянии sp2 гибридизации и образует три  -связи, лежащие в одной плоскости под углом 1200 и одну
-связи, лежащие в одной плоскости под углом 1200 и одну  -связь с атомом кислорода, за счет негибридной р-орбитали. Причем связи между атомами углерода и кислорода сильно поляризованы. В результате на атоме углерода образуется частичный положительный заряд, и он становиться удобным объектом для атаки нуклеофила. Эта атака для альдегидов приводит к реакции присоединения (АN). В зависимости от природы радикала, связанного с карбонильной группой, величина заряда на атоме углерода может быть разной, т.е. альдегиды вступают в реакцию присоединения с разной активностью.
-связь с атомом кислорода, за счет негибридной р-орбитали. Причем связи между атомами углерода и кислорода сильно поляризованы. В результате на атоме углерода образуется частичный положительный заряд, и он становиться удобным объектом для атаки нуклеофила. Эта атака для альдегидов приводит к реакции присоединения (АN). В зависимости от природы радикала, связанного с карбонильной группой, величина заряда на атоме углерода может быть разной, т.е. альдегиды вступают в реакцию присоединения с разной активностью.
Химические свойства.
1) Итак, для альдегидов характерны реакции нуклеофильного присоединения. Такие реакции присоединения протекают для альдегидов с разными веществами.

Например,к реакциям присоединения (АN) относитсяреакция гидрирования (т.е. присоединения водорода).Эту реакцию можно рассматривать как реакцию восстановления альдегидов.
|
|
|
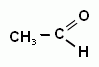
+ H2 → CH3-CH2-OH
Очень важной является реакция присоединения спиртов к альдегидам. При этом образуются полуацетали, а потом полуацетали при взаимодействии со спиртами превращаются в ацетали (но это уже реакция нуклеофильного замещения).

2) Характерной для альдегидов является реакция окисления. Альдегиды - это вообще один из наиболее легко окисляющихся классов органических соединений. При этом обычно образуются соответствующие карбоновые кислоты. А окисление в жестких условиях или очень сильным окислителем приведет к образованию углекислого газа.
Полное окисление:

+ О2 → СО2 + Н2О
Реакция «серебряного зеркала» (р. Толленса) – с аммиачным раствором нитрата серебра (обычно вместо формулы комплексного соединения серебра в уравнении пишут формулу оксида серебра). Образуется соответствующая карбоновая кислота и свободное серебро, которое выделяется в виде черного осадка или блестящей (зеркальной) пленки на поверхности сосуда.


+ Ag2O → + Ag↓
Реакция «медного зеркала» (р. Фелинга) – реакция окисления альдегидов комплексным соединением меди (II) (обычно вместо формулы комплексного соединения меди в уравнении пишут формулу гидроксида меди (II). Образуется соответствующая карбоновая кислота и оксид меди (I) оранжевого цвета. Эти реакции окисления (с оксидом серебра и с гидроксидом меди) используют как качественные на альдегиды. Можно использовать как качественную реакцию на альдегиды и реакцию с фуксинсернистой кислотой. В этом случае мы наблюдаем изменение окраски раствора в характерный розовый цвет.


+ Cu(OH)2↓ → + CuOH↓
Cu(OH)↓ → Cu2O↓ + H2O
Можно сделать вывод: карбонильные соединения легко окисляются и восстанавливаются. спирт ↔ альдегид ↔ карбоновая кислота
«ДОРОГА ОВР» Понятие степени окисления в органической химии несколько отличается от изученного нами в курсе неорганической химии. Каждый атом углерода в органической молекуле имеет свою степень окисления, которая может быть даже дробной. Пользоваться этим понятием в органике очень неудобно. Поэтому чаще говорят не о степени окисления, а о степени окисленности атома углерода.
Если данный атом углерода имеет связи только с атомами водорода или углерода, то его степень окисленности считают равной 0.
|
|
|
Например: в углеводородах СН3-СН3. Это неокисленная форма органических соединений.
Если атом углерода имеет одну связь с кислородом, то его степень окисленности считают равной 1.
Например: в спиртах CH3-CH2-OH
Если атом углерода имеет две связи с кислородом, то его степень окисленности считают равной 2.
 Например: в альдегидах и кетонах
Например: в альдегидах и кетонах
Если атом углерода имеет три связи с кислородом, то его степень окисленности считают равной 3.
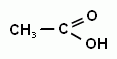 Например: в карбоновых кислотах
Например: в карбоновых кислотах
И максимально возможная степень окисленности появляется в молекуле СО2, т.к. здесь углерод все возможные для него четыре связи тратит на связь с кислородом.
Для написания ОВР в органической химии очень удобно пользоваться «дорогой ОВР», по которой в основном и протекают эти реакции. В процессе реакции обычно окисляется только углерод функциональной группы, а углеродная цепь не подвергается изменениям. Только при образовании карбоновых кислот (т.е. на третьей стадии окисления) цепь начинает разрываться, потому что углерод карбоксильной группы должен быть первичным. Окончательное разрушение углеродного скелета происходит только на последней стадии, при образовании углекислого газа.
Углеводород (0) ↔ спирт (1) ↔ альдегид (2) ↔ карб.кислота (3) ↔ СО2 (4)
Ш. Для карбонильной группы возможны реакции полимеризации с разрывом двойной связи. Их можно рассматривать как результат нуклеофильной атаки кислородным атомом одной молекулы карбонильного атома другой молекулы. Например, молекулы уксусного альдегида вступают в реакцию друг с другом, при этом углеродная цепочка становится длиннее (альдольная поликонденсация). Особенно характерна такая реакция для формальдегида. Например, при хранении формалина (40% раствор формальдегида) образуется белый осадок – параформ.

Кроме того, при длительном хранении формальдегид, даже в водных растворах, способен к реакции диспропорционирования (реакция Канниццаро).
|
|
|
2СН2О + Н2О → СН3ОН + НСООН, и раствор приобретает кислую реакцию.
Очень важной для современной промышленности является реакция поликонденсации формальдегида с фенолом. При этом образуется фенолформальдегидная смола.
Кетоны в целом менее активны, чем альдегиды. Окисление кетонов проходит аналогично окислению альдегидов, но в более жестких условиях и сопровождается разрывом углеродной цепи и образованием нескольких карбоновых кислот. При восстановлении кетонов образуются вторичные спирты. Простейшим кетоном является ацетон (диметилкетон, пропанон): бесцветная жидкость с характерным запахом, хорошо растворим в воде, сам хороший растворитель. Это исходное вещество для получения ряда лекарственных препаратов. Ацетон – один из продуктов метаболизма жирных кислот в организме человека. Его повышенная концентрация в крови и моче характерна при отравлении, тяжелых случаях диабета, при токсикозах и голодании. Повышение концентрации ацетона нарушает работу нервной системы.
Получение альдегидов и применение альдегидов.
Альдегиды получают:
1). окисление спиртов (одноатомных первичных);
2). гидратация ацетилена (реакция Кучерова, соли ртути в роли катализатора);
3). каталитическое окисление этилена (соли меди в роли катализатора);
4). каталитическое окисление метана (получение формальдегида) и т.д.
Метаналь используют:
- в медицине для получения лекарств (например: уротропин), для хранения биопрепаратов и дезинфекции помещений (формалин денатурирует белок);
- в сельском хозяйстве для протравливания семян;
- получения параформа, фенолформальдегидных смол (полимеров) и пластмасс.
Этаналь используют:
- для производства уксусной кислоты;
- производства лекарств (хлорал – трихлорацетальдегид, его гидрат применяется в качестве снотворного), полимеров и искусственных волокон (ацетатный шелк, целлофан, целлулоид…)
|
|
|


