 |
Термодинамический анализ выхода реакции от давления и температуры
|
|
|
|
Московский Государственный Институт
Стали и Сплавов
(технологический университет)
Кафедра Физической Химии
Домашнее задание № 1
Химическая термодинамика
Вариант № 54
Студент: Горечкина Анастасия
Группа: М2-11-3
Преподаватель:Апыхтина И.В.
Исходные данные:
Реакция: СS2 =C(s)+S2
Т1 = 1000 К
Т2 = 2000 К
Т3 = 1900 К
Р = 0,5 атм.
1. Расчет ΔН0298, ΔS0298, ΔCp (Δa, Δb, Δc) химической реакции по таблицам стандартных термодинамических величин
Рассчитаем тепловой эффект реакции в стандартных условиях.
По закону Гесса он равен разности между суммой стандартных теплот образования продуктов реакции и суммой стандартных теплот образования исходных веществ с учетом стехиометрических коэффициентов.
Для данной реакции:
ΔН0298 = ΔН0298(S2)-ΔН0298(CS2)
ΔН0298 = 128600-11630= 11900Дж
Рассчитаем изменение теплоемкости реакции при стандартных условиях.
Для этого найдем коэффициенты Δа, Δb, Δc для данной реакции:
Δа = а(S2)+а(C(s))- а(CS2)
Δа = 36.11+16.86-52.09= 0.88
Δb = b(S2)+b(C(s))- b(CS2)
Δb = 1.09+4.77-6.69 =-0.83*103
Δc = c(S2)+c(C(s))- c(CS2)
Δc = -3.51-8.54+7.53 =-4.52*105
ΔСр реакции рассчитывается в соответствии с уравнением:
ΔСр = Δа+Δb∙Т+Δс∙Т-2
ΔСр298 = 0.88-0.83*10-3T-4.52*105*T-2 = -4,457 Дж/К
Рассчитаем изменение энтропии и ∆G0298 при стандартных условиях.
Изменение энтропии при стандартных условиях равно разности между суммой энтропий продуктов и суммой энтропий исходных веществ при стандартных условиях с учетом стехиометрических коэффициентов.
Для данной реакции:
ΔS0298 = S0298(S2)+S0298(C(s))-S0298(CS2)
ΔS0298 = 228.06+5.74-237.77 =-3.97 Дж/моль*К
∆G0298=13083 Дж
2. Результаты приближенного расчета ΔН0Т, ΔS0T, ΔG0T и lnKр в интервале температур Т1÷Т2 при следующих приближениях:
|
|
|
а) ΔСр = 0
1) ΔН0Т = ΔН0298 + 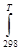 ΔСрdT = ΔН0298 +ΔСр∙dT = ΔН0298
ΔСрdT = ΔН0298 +ΔСр∙dT = ΔН0298
2) ΔS0T = ΔS0298 + 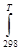 ΔСр/T dT = ΔS0298 + ΔСр dT/T = ΔS0298
ΔСр/T dT = ΔS0298 + ΔСр dT/T = ΔS0298
3) ΔG0T = ΔН0T – T∙ ΔS0T
4) lnKp = - ΔG0T/RT
| T,K | ∆H˚T,Дж | ∆S˚T, Дж/моль*К | ∆G˚T, Дж | ln Kp |
| -3,97 | -1,9097 | |||
| -3,97 | -1,7796 | |||
| -3,97 | -1,6711 | |||
| -3,97 | -1,5793 | |||
| -3,97 | -1,5006 | |||
| -3,97 | -1,4324 | |||
| -3,97 | -1,3727 | |||
| -3,97 | -1,3201 | |||
| -3,97 | -1,2733 | |||
| -3,97 | -1,2314 | |||
| -3,97 | -1,1937 | |||
б) ΔСр = ΔСр298=const
1) ΔН0Т = ΔН0298 +  ΔСрdT = ΔН0298 + ΔСр298∙(Т-298)
ΔСрdT = ΔН0298 + ΔСр298∙(Т-298)
2) ΔS0T = ΔS0298+  ΔСр/T dT= ΔS0298 + ΔСр· ln(T/298)
ΔСр/T dT= ΔS0298 + ΔСр· ln(T/298)
3) ΔG0T = ΔН0T – T∙ ΔS0T
4) lnKp = - ΔG0T/RT
| T,K | ∆H˚Т,Дж | ∆S˚Т, Дж/моль*К | ∆G˚Т, Дж | ln Kp | ∆Сp, Дж/К |
| 8771,2 | -9,37 | 18137,10561 | -2,1826 | -4,4572 | |
| 8325,5 | -9,79 | 19095,27479 | -2,089 | -4,4572 | |
| 7879,8 | -10,18 | 20094,01815 | -2,015 | -4,4572 | |
| 7434,1 | -10,54 | 21129,94628 | -1,9559 | -4,4572 | |
| 6988,4 | -10,87 | 22200,19291 | -1,9082 | -4,4572 | |
| 6542,7 | -11,17 | 23302,30239 | -1,8694 | -4,4572 | |
| -11,46 | 24434,14726 | -1,8377 | -4,4572 | ||
| 5651,3 | -11,73 | 25593,86653 | -1,8117 | -4,4572 | |
| 5205,6 | -11,99 | 26779,81859 | -1,7903 | -4,4572 | |
| 4759,9 | -12,27 | 27990,54452 | -1,7728 | -4,4572 | |
| 4314,1 | -12,46 | 29654,91401 | -1,7843 | -4,4572 |
в) ΔСр = ΔСр([298+T2]/2)=const
1) ΔН0Т= ΔН0298 +  ΔСрdT= ΔН0298 +ΔСр∙
ΔСрdT= ΔН0298 +ΔСр∙  dT= ΔН0298 + ΔСр∙(Т-298)
dT= ΔН0298 + ΔСр∙(Т-298)
2) ΔS0T= ΔS0298 +  ΔСр/T dT= ΔS0298 + ΔСр· ln(T/298)
ΔСр/T dT= ΔS0298 + ΔСр· ln(T/298)
3) ΔG0T = ΔН0T – T∙ ΔS0T
4) lnKp = - ΔG0T/RT
| Т, К | ∆Н0Т , Дж | ∆S0Т, Дж/моль*К | ∆G0Т, Дж | Ln Kp | ∆C0p, Дж/К |
| 11607,968 | -4,474 | -1,935 | -0,416 | ||
| 11566.368 | -4,513 | -1,808 | -0,416 | ||
| 11524.768 | -4,549 | -1,703 | -0,416 | ||
| 11483.168 | -4,583 | -1,615 | -0,416 | ||
| 11441.568 | -4,614 | -1,539 | -0,416 | ||
| 11399.968 | -4,642 | -1,473 | -0,416 | ||
| 11358.368 | -4,669 | -1,416 | -0,416 | ||
| 11316.768 | -4.694 | -1,366 | -0,416 | ||
| 11275.168 | -4,718 | -1,322 | -0,416 | ||
| 11233.568 | -4,741 | -1,282 | -0,416 | ||
| 11191.968 | -4,762 | -1,246 | -0,416 |
3. Результаты точного расчета функций ΔН0Т, ΔS0T, ΔG0T, lnKp в интервале температур Т1÷Т2:
|
|
|
1) ΔН0Т = ΔН0298 +ΔСрdT, где ΔСр = Δа + Δb∙T + Δc∙T-2
ΔН0Т = ΔН0298 + Δa∙(T-298) + Δb∙(T2-2982)/2 – Δc(1/T-1/298)
2) ΔS0T = ΔS0298 + ΔСр/T dT, где ΔСр = Δа + Δb∙T + Δc∙T-2
ΔS0T= ΔS0298 + Δa∙ln(T/298) + Δb∙(T-298)/2 – Δc(1/T2-1/2982)
3) ΔG0T = ΔН0T – T∙ ΔS0T
4) lnKp = - ΔG0T/RT
| T,К | ∆Н0Т, Дж | ∆S0Т, Дж/моль*К | ∆G0Т, Дж | Ln Kp | ∆C0p, Дж/К | Кр |
| -5,806 | -2,0304 | -0,402 | 0,131 | |||
| -5,845 | -1,9097 | -0,407 | 0,148 | |||
| -5,881 | -1,8092 | -0,430 | 0,164 | |||
| -5,917 | -1,7246 | -0,466 | 0,178 | |||
| -5,953 | -1,6524 | -0,513 | 0,192 | |||
| -5,990 | -1,5901 | 0,566 | 0,204 | |||
| -6,028 | -1,5359 | -0,625 | 0,215 | |||
| -6,068 | -1,4883 | -0,687 | 0,226 | |||
| -6,109 | -1,4463 | -0,754 | 0,235 | |||
| -6,152 | -1,4091 | -0,822 | 0,244 | |||
| -6,196 | -1,3758 | -0,893 | 0,253 |
4. Графики температурной зависимости термодинамических функций ΔСр, ΔН0Т, ΔS0T, ΔG0T, lnKp для всех вариантов расчета
График зависимости ΔН0Т от Т

График зависимости Ln Kp от Т

График зависимости ∆ Ср от Т

График зависимости ∆ Gºт от Т

График зависимости ∆ Sºт от Т

5. Результаты расчета равновесных составов: числа молей, мольные доли и массовые проценты, при заданных Т3 и Р для случаев, когда реагируют стехиометрические смеси
а) исходных веществ;
Б) всех веществ.
а) CS2 = C(s) +S2
Исходные 1 0 0
числа молей
Равновесные 1-z z z ∑ = 1+z
числа молей
1. Запишем выражение для Кр реакции:
Кр = РS2/PCS2 = XS2 /XCS2
2. Допустим, что к моменту равновесия прореагировало z молей СО2. Запишем выражения для равновесных мольных долей:
Xcs2 = 1-z/1+z
Xs2 = z/1+z
Xc(s) = z/1+z
3. Запишем Кр как функцию от z.
Кр = z/(1-z)
4. Подставим значения Кр и Р
Кр = 0.244
Р = 0.5 атм.
По расчетам: z = 0,1961≈0,2
5. Результат
Xcs2 = 1-z/1=0.8 CS2 = 80 % n(cs2 ) = 0.8 моля
Xs2 = z/1 =0.2 S2 = 20 % n(s2 )= 0.2 моля
Массовый процент:

Wcs2 =82,6% Ws2 = 17,4%
б) СS2 = C(S) + S2
Исходные 1 1 1
числа молей
Равновесные 1-z 1+z 1+z ∑ = 3+z
числа молей
1. Запишем выражение для Кр реакции:
Кр = РS2/PCS2 = XS2 /XCS2
2. Допустим, что к моменту равновесия прореагировало z молей СО2. Запишем выражения для равновесных мольных долей:
Xs2 = 1+z/3+z
Xcs2 = 1-z/3+z
Xc(s) = z+1/3+z
|
|
|
3. Запишем Кр как функцию от z.
Kp = (1+z)/ (1-z)
4. Подставим значения Кр и Р
Кр = 0.244
Р = 0.5 атм.
По расчетам: z = -0.61
5. Результат
Xs2 = 1+z/2 =0.195 S2 – 19.5% ns2 = 1,61 моля
Xсs2 = 1-z/2 = 0.805 CS2 – 80.5% ncs2 = 0.39 моля
Массовый процент:

Ws2 = 17% Wcs2=83 %
6. Исследование вопроса о направлении реакции при температуре Т3 и Р, если в исходный момент взято по одному молю каждого исходного вещества и по два моля продукта реакции
CS2 =C(S) +S2
Исходные 1 2 ∑=3
числа молей
1/3 2/3
Кр = 0.244
Р = 0.5атм.
Т = 1900 К
Для того, чтобы определить, в каком направлении идет реакция, необходимо знать знак ΔG. Из уравнения изотермы Вант-Гоффа:
ΔG = ΔG0T + RT∙ln(Рs2/Pcs2) =
ΔG = 22259+8.31·1900ln2 = 33 203Дж > 0
Значит,реакция идет в обратном направлении
Термодинамический анализ выхода реакции от давления и температуры
А) График точных значений стандартных энтальпий реакции ∆Нº(Т) полностью лежит выше оси абцисс,т.е. ∆Нº(Т)>0,т.е. наша реакция эндотермическая.
(∂ln(Kp)/ ∂T)p = ∆HT/(R*T2) –Уравнение Вант-Гоффа
Если Т↑ то lnKp увеличивается→Кр увеличивается→выход газообразных продуктов увеличивается. Для эндотермической реакции увеличение выхода достигается увеличение Т.
Б) Кр=F(Т)=Кр=const
При увеличении давления выход газообразных продуктов в реакции уменьшится. При уменьшении давления выход реакции газообразных продуктов реакции увеличится
|
|
|


