 |
Биологический азот претерпевает в почвах циклические превращения (из нитратов и нитритов- в аммиак и аминокислоты и обратно), в процессе которых он меняет свои валентности.
|
|
|
|
Круговорот азота является одним из самых сложных круговоротов в природе. Охватывает всю биосферу, а также атмосферу, литосферу, гидросферу. Очень важную роль в круговороте азота играют микроорганизмы. В круговороте азота выделяют следующие этапы:
1-й этап (фиксация азота): а) азотфиксирующие бактерии связывают (фиксируют) газообразный азот с образованием аммонийной формы (NH и солей аммония) – это биологическая фиксация; б) вследствие грозовых разрядов и фотохимического окисления образуются оксиды азота, при взаимодействии с водой они образуют азотную кислоту, в почве она превращается в нитратный азот.
2-й этап – превращение в растительный белок. Обе формы (аммонийная и нитратная) фиксированного азота усваиваются растениями и превращаются в сложные белковые соединения.
3-й этап – превращение в животный белок. Животные поедают растения, в их организме растительные белки превращаются в животные.
4-й этап – разложение белка, гниение. Продукты метаболизма растений и животных, а также ткани отмерших организмов под воздействием микроорганизмов разлагаются с образованием аммония (процесс аммонификации).
5-й этап – процесс нитрификации. Аммонийный азот окисляется до нитритного и нитратного азота.
6-й этап – процесс денитрификации. Нитратный азот под воздействием денитрифицирующих бактерий восстанавливается до молекулярного азота, который поступает в атмосферу. Круг замыкается.
Антропогенное воздействие на круговорот азота заключается в следующем:
1 Промышленное использование азота для получения аммиака примерно на 10% повышает общее количество азота, фиксированного естественным путем.
2 Широкое использование азотных удобрений, превышающее потребности растений, приводит к загрязнению окружающей среды, при этом часть избыточного азота смывается в водоемы, вызывая опасное явление «эвтрофирования»(загрязнение водоемов водорослями). Оно вызывает вторичное загрязнение водоемов, нарушение круговорота веществ, изменение их трофического статуса.
|
|
|
Нитрификация
Азот в форме аммиака и соединений аммония, получающийся в процессах биогенной азотфиксации, быстро окисляется до нитратов и нитритов. Этот процесс носит название нитрификации, он осуществляется нитрифицирующими бактериями. Однако нет такой бактерии, которая бы прямо превращала аммиак в нитрат. В его окислении всегда участвуют две группы бактерий: одни окисляют аммиак, образуя нитрит, а другие окисляют нитрит в нитрат. Наиболее известные виды нитрифицирующих бактерий- это Nitrosomonas и Nitrobacter. Nitrosomonas окисляет аммиак:
NH3 + 1½ O2 = (NO2-) + 2H+ + H2O
Nitrobacter окисляют нитрит:
(NO2-) + ½ O2 = NO3-
Все живые организмы поставляют азот в окружающую среду. С одной стороны, все они выделяют в ходе жизнедеятельности продукты азотистого обмена: аммиак, мочевину и мочевую кислоту. Последние два соединения разлагаются в почве с образованием аммиака (который при растворении в воде дает ионы аммония).
Аммонификация
Мочевая кислота, выделяемая птицами и рептилиями, также быстро минерализуется особыми группами микроорганизмов с образованием NH3 и СО2. С другой стороны, азот, включённый в состав живых существ, после их гибели подвергается аммонификации (разложение содержащих азот сложных соединений с выделением аммиака и ионов аммония(NH4+)) и нитрификации.
Денитрификация
Продукты нитрификации — NO3- и (NO2-) в дальнейшем подвергаются денитрификации. Этот процесс целиком происходят благодаря деятельности денитрифицирующих бактерий, которые обладают способностью восстанавливать нитрат через нитрит до газообразной закиси азота (N2O) и азота (N2). Эти газы свободно переходят в атмосферу.
|
|
|
10 [ H ] + 2 H+ +2NO3- = N2 + 6 H2O
В отсутствие кислорода нитрат служит конечным акцептором водорода. Способность получать энергию путем использования нитрата как конечного акцептора водорода с образованием молекулы азота широко распространена у бактерий. Временные потери азота на ограниченных участках почвы, несомненно, связаны с деятельностью денитрифицирующих бактерий. Таким образом, круговорот азота невозможен без участия почвенной микрофлоры.

КАК УСТРОЕНА БИОЛОГИЧЕСКАЯ ОЧИСТКА ВОДЫ?
Помимо этого, будут успешно развиваться токсичные микроорганизмы в водоемах, чего допустить нельзя – именно поэтому соединения азота и фосфора нужно нещадно удалять из сточных вод.
Для удаления применяются соответствующие физико-химические способы очистки сточных вод, а именно нитрификация и денитрификация сточных вод. По сути, процессы эти - окисление аммиака до азотной кислоты, при котором осуществляется ассимиляция углекислоты нитрита до газообразного азота.

Иными словами, денитрификация призвана очистить стоки от соединений азота, а также избавить массу канализационных жидкостей от биологических окисляемых соединений органического типа.
Рекомендуемый уровень кислотности в этом процессе ― 7-7,5 Ph. Если уровень кислотности будет ниже или выше рекомендуемого уровня, то процесс будет затормаживаться. Роль органических веществ, при проведении денитрификации могут сыграть практически любые виды биологически окисляемых органических соединений (углеводы, спирты, продукты распада белков и, конечно, органические кислоты).
Большой цикл Азота.
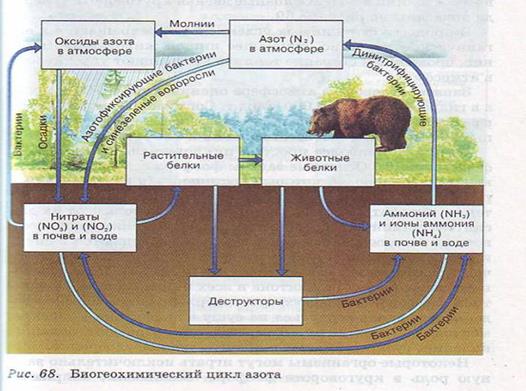
КРУГОВОРОТ АЗОТА
Азот входит в состав земной атмосферы в несвязанном виде в форме двухатомных молекул. Приблизительно 78% всего объема атмосферы приходится на долю азота. Кроме того, азот входит в состав растений и животных организмов в форме белков. Растения синтезируют белки, используя нитраты из почвы. Нитраты образуются там из атмосферного азота и аммонийных соединений, имеющихся в почве. Процесс превращения атмосферного азота в форму, усвояемую растениями и животными, называется связыванием (или фиксацией) азота.
|
|
|
При гниении органических веществ значительная часть содержащегося в них азота превращается в аммиак, который под влиянием живущих в почве нитрифицирующих бактерий окисляется затем в азотную кислоту. Последняя, вступая в реакцию с находящимися в почве карбонатами, например с карбонатом кальция СаСОз, образует нитраты:
2HN0з + СаСОз = Са(NОз)2 + СОС + Н0Н
Некоторая же часть азота всегда выделяется при гниении в свободном виде в атмосферу. Свободный азот выделяется также при горении органических веществ, при сжигании дров, каменного угля, торфа. Кроме того, существуют бактерии, которые при недостаточном доступе воздуха могут отнимать кислород от нитратов, разрушая их с выделением свободного азота. Деятельность этих денитрифицирующих бактерий приводит к тому, что часть азота из доступной для зеленых растений формы (нитраты) переходит в недоступную (свободный азот). Таким образом, далеко не весь азот, входивший в состав погибших растений, возвращается обратно в почву; часть его постепенно выделяется в свободном виде.
Непрерывная убыль минеральных азотных соединений давно должна была бы привести к полному прекращению жизни на Земле, если бы в природе не существовали процессы, возмещающие потери азота. К таким процессам относятся, прежде всего, происходящие в атмосфере электрические разряды, при которых всегда образуется некоторое количество оксидов азота; последние с водой дают азотную кислоту, превращающуюся в почве в нитраты. Другим источником пополнения азотных соединений почвы является жизнедеятельность так называемых азотобактерий, способных усваивать атмосферный азот. Некоторые из этих бактерий поселяются на корнях растений из семейства бобовых, вызывая образование характерных вздутий — «клубеньков», почему они и получили название клубеньковых бактерий. Усваивая атмосферный азот, клубеньковые бактерии перерабатывают его в азотные соединения, а растения, в свою очередь, превращают последние в белки и другие сложные вещества.
|
|
|
Таким образом, в природе совершается непрерывный круговорот азота. Однако ежегодно с урожаем с полей убираются наиболее богатые белками части растений, например зерно. Поэтому в почву необходимо вносить удобрения, возмещающие убыль в ней важнейших элементов питания растений. В основном используются нитрат кальция Ca(NO3)2, нитрат аммония NH4NO3, нитрат натрия NANO3, и нитрат калия KNO3. Например, в Таиланде используются листья лейкаены как органическое удобрение. Лейкаена принадлежит к бобовым растениям и, как и все они, содержит очень много азота. Поэтому ее можно использовать вместо химического удобрения.
В последнее время наблюдается повышения содержания нитратов в питьевой воде, главным образом за счет усилившегося использования искусственных азотных удобрений в сельском хозяйстве. Хотя сами нитраты не так уж опасны для взрослых людей, в организме человека они могут превращаться в нитриты. Кроме того, нитраты и нитриты используются для обработки и консервирования многих пищевых продуктов, в том числе ветчины, бекона, солонины, а также некоторых сортов сыра и рыбы. Отдельные ученые полагают, что в организме человека нитраты могут превращаться в нитрозамины:
Известно, что нитрозамины способны вызывать онкологические заболевания у животных. Большинство из нас уже подвержено воздействию нитрозаминов, которые в небольшом количестве находятся в загрязненном воздухе, сигаретном дыму и некоторых пестицидах. Полагают, что нитрозамины могут быть причиной 70-90% случаев онкологических заболеваний, возникновение которых приписывают действию факторов окружающей среды.
Соединения азота - содержится в природных водах в виде неорганических соединений: аммонийных, нитратных, нитритных ионов, в белках организма и в продуктах их жизнедеятельности. Неорганические соединения азота необходимы для жизнедеятельности организмов, особенно автотрофов.
Малый цикл серы.
Важное значение в формировании геохимических и гидрогеохимических условий имеют сульфофикация, т.е. окисление элементарной и восстановленной форм серы до SO42- — тионовыми, пурпурными и серобактериями (аэробными и анаэробными), и
сульфатредукция — восстановление элементарной и окисленной форм серы до H2S бактериями рода Desulfovebrio и др. Эти процессы представляют собой важнейшие этапы круговорота серы в природе. Процесс сульфофикации серобактериями характерен для аэробных условий. Он происходит по схеме:
2H2S + О2 →2Н2О + S2 + 65 ккал,
S2 + 3О2 + 2 Н2О → 2H2SО4 + 283 ккал.
Образующаяся на промежуточном этапе сера накапливается в клетках серобактерий и затем окисляется до серной кислоты. При наличии в системе кальция возможно продуцирование гипса.
|
|
|
Процесс сульфатредукции возможен лишь в анаэробных условиях и заключается в восстановлении окисленных форм серы (SO42-) до H2S анаэробными сульфатредуцирующими бактериями. Известно, что чисто химическое разложение сульфатов под влиянием температуры и давления в пределах доступной изучению части
разреза литосферы из-за очень высокой энергии связи кислорода и серы в ионе SO42- может происходить лишь в высокотемпературных условиях (большие глубины, районы современного вулканизма).
Сульфатредукция обусловливает сразу несколько гидрогеохимических следствий: генерируются значительные количества (от миллиграммов до 1—4 г/л) сероводорода
(S2- + 2Н2О = H2S + 2ОН-) — одного из важнейших потенциал задающих веществ. При этом создаются восстановительные условия (Eh 300 мВ и менее) и выпадают в осадок в виде сульфидов Fe, Си, РЬ и др. Повышение рН среды приводит к смещению карбонатных равновесий в сторону СО32-, следствием чего является осаждение СаСО3.
При автотрофной сульфатредукции выделяется значительное,
вплоть до пересыщения, количество углекислоты, которая при
наличии в водах Са2+ и Mg2+ стимулирует осаждение карбонатов
этих элементов. За счет редукции сульфатов и осаждения карбонатов кальция и магния могут происходить существенное снижение минерализации подземных вод и смена доминирующих ионов.
6. Большой цикл серы. Круговорот серы.
Сера входит в состав ряда аминокислот и белков. Соединения серы поступают в круговорот в основном в виде сульфидов из продуктов выветривания пород суши и морского дна. Ряд микроорганизмов (например, хемосинтезирующие бактерии) способны переводить сульфиды в доступную для растений форму — сульфаты. Растения и животные отмирают, минерализация их остатков редуцентами возвращает соединения серы в почву. Так, серобактерии окисляют до сульфатов образующийся при разложении белков сероводород. Сульфаты способствуют переводу труднорастворимых соединений фосфора в растворимые. Количество минеральных соединений, доступных растениям, возрастает, улучшаются условия для их питания.
Ресурсы серосодержащих полезных ископаемых весьма значительны, а избыток этого элемента в атмосфере, приводящий к кислотным дождям и нарушающий процессы фотосинтеза вблизи промышленных предприятий, уже беспокоит ученых. Количество серы в атмосфере существенно увеличивается при сжигании природного топлива.

Цикл серы сопрягается с циклом органического углерода в реакциях сульфидогенеза, катализируемых только прокариотами, сульфат- и сероредуцирующими организмами. В биогеохимическом цикле серы участвуют следующие формы соединений серы, создающие значительные резервуары: 1) сульфаты, преимущественно сульфаты моря; 2) сульфиды в виде растворенного H2S и нерастворимых сульфидов металлов, частично эндогенного (вулканического) и в основном экзогенного (биогенного) происхождения; 3) сера, в значительной части эндогенного происхождения. Разнообразные промежуточные соединения неполного окисления серы, как тиосульфат или SO2, появляются в транзитных формах и незначительной концентрации, не образуя резервуары. Подобно тому как конечным результатом сопряженных циклов углекислоты, органического углерода, кислорода оказывается накопление кислорода атмосферы, конечным продуктом серного цикла оказываются сульфаты океана.
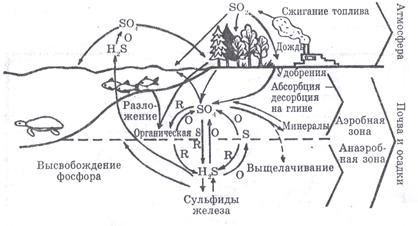
Рис. Круговорот серы (по Ю.Одуму, 1975). «Кольцо» в центре схемы иллюстрирует процесс окисления (О) и восстановление (R), благодаря которым происходит обмен серы между фондом доступного сульфата (S04) и фондом сульфидов железа, находящихся глубоко в почве и в осадках
7. Классификация Вернадского.
Подразделение химических элементов по характеру их поведения в процессах миграции.
1. Благородные газы – He, Ne, Ar, Kr, Xe. Соединения с другими атомами образуют исключительно редко, поэтому в природных химических процессах значительного участия не принимают.
2. Благородные металлы – Ru, Rh, Pd, Os, Ir, Pt, Au. Соединения редки. Преимущественно присутствуют в форме сплавов, и образуются в основном в глубинных процессах (магматических, гидротермальных).
3. Циклические элементы – H, B, C, N, O, F, Na, Mg, Al, Si, P, S, Cl, K, Ca, Ti, V, Mn, Fe, Co, Ni, Cu, Zn, As, Se, Sr, Mo, Ag, Cd, Ba, (Be, Cr, Ge, Zr, Sn, Sb, Te, Hf, W, Re, Hg, Tl, Pb, Bi). Наиболее многочисленная группа и преобладающая по массе. Для каждого элемента характерен определённый круг химических соединений, возникающих и распадающихся в ходе природных процессов. Таким образом, каждый элемент проходит цепочку превращений, в конечном счёте возвращаясь к исходной форме нахождения – и далее. Циклы не являются полностью обратимыми, так как часть элементов постоянно выходит из круговорота (и часть так же снова в него вовлекается).
4. Рассеянные элементы – Li, Sc, Ga, Br, Rb, Y, Nb, In, J, Cs, Ta. Безусловно, господствуют рассеянные атомы, не образующие химических соединений. Незначительная доля может участвовать в образовании самостоятельных минеральных соединений (большинство – в глубинных процессах, а J и Br – в гипергенных).
5. Редкоземельные элементы – La, Ce, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tu, Yb, Lu. Тяготеют к рассеянным. Основная черта – совместная миграция.
6. Радиоактивные элементы - Po, Rn, Ra, Ac, Th, Pa, U. Основная специфика в том, что в геохимическом процессе происходит постоянное превращение одних элементов в другие, что делает процессы их химической миграции наиболее сложными.
Элементы условности данной классификации:
· наличие химических элементов, занимающих промежуточное положение между группами, т.е. способных вести себя в миграционных процессах двояко; в этих случаях для отнесения такого элемента к одной из двух возможных групп «решающим аргументом будет история главной по весу части атомов или наиболее яркие черты их геохимической истории» (наличие доли субъективизма в таком критерии очевидно).
· выделение в особую группу радиоактивных элементов не учитывает разной устойчивости изотопов; у ряда элементов существенной является доля как стабильных, так и нестабильных изотопов, и, естественно, геохимическая история соответствующих долей общего числа атомов данного элемента будет различной (K, Rb, Sm, Re и др.). Сейчас, в связи с процессами радиогенного загрязнения, необходимо учитывать и миграцию искусственных радиоактивных изотопов.
|
|
|


