 |
Физические основы термодинамики
|
|
|
|
ОСНОВНЫЕ ФОРМУЛЫ И ЗАКОНЫ
МОЛЕКУЛЯРНОЙ ФИЗИКИ И ТЕРМОДИНАМИКИ
Молекулярная физика
Количество молей (вещества) газа:  ,
,
где m – масса газа, M – молярная масса газа, N – количество молекул газа,
 – постоянная Авогадро.
– постоянная Авогадро.
Если система представляет собой смесь нескольких газов, то количество молей (вещества) этой системы:
 ,
,
где  - количества молей,
- количества молей,  - количества молекул,
- количества молекул,  - массы и
- массы и  - молярные массы газов,
- молярные массы газов,  - число компонентов смеси.
- число компонентов смеси.
Уравнение Менделеева - Клапейрона (уравнение состояния идеального газа):
 ,
,
где  - давление,
- давление,  - объем,
- объем,  - термодинамическая температура,
- термодинамическая температура,  - масса и
- масса и  - молярная масса газа,
- молярная масса газа,  - универсальная газовая постоянная.
- универсальная газовая постоянная.
Закон Бойля-Мариотта (изотермический процесс:  ,
,  ,
,  ) для двух состояний газа:
) для двух состояний газа:  .
.
Закон Гей-Люссака (изобарный процесс:  ,
,  ,
,  ) для двух состояний газа:
) для двух состояний газа:  .
.
Закон Шарля (изохорный процесс:  ,
,  ,
,  ) для двух состояний газа:
) для двух состояний газа:  .
.
Объединенный газовый закон ( ,
,  ) для двух
) для двух
состояний газа:  .
.
Закон Дальтона определяет давление смеси газов:
 ,
,
где  - парциальные давления компонентов смеси;
- парциальные давления компонентов смеси;  - число компонентов смеси.
- число компонентов смеси.
Молярная масса смеси газов:  ,
,
где  - количества молей,
- количества молей,  - массы газов,
- массы газов,  - число компонентов смеси.
- число компонентов смеси.
Концентрация молекул газа:  ,
,
где  - количество молекул,
- количество молекул,  - объем,
- объем,  – постоянная Авогадро,
– постоянная Авогадро,  - молярная масса и
- молярная масса и  - плотность газа.
- плотность газа.
Средняя кинетическая энергия поступательного движения молекулы:
 ,
,
где  - постоянная Больцмана,
- постоянная Больцмана,  - термодинамическая температура.
- термодинамическая температура.
Основное уравнение молекулярно-кинетической теории идеальных газов:
 ,
,
где  - давление,
- давление,  - концентрация молекул газа.
- концентрация молекул газа.
Зависимость давления газа от концентрации молекул и термодинамической температуры:
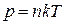 .
.
Из основного уравнения молекулярно-кинетической теории идеальных газов следует, что
|
|
|
 ,
,
где  - суммарная кинетическая энергия поступательного движения
- суммарная кинетическая энергия поступательного движения  молекул газа.
молекул газа.
Средняя полная механическая энергия одной молекулы:  ,
,
где  - сумма числа поступательных, числа вращательных и удвоенного числа колебательных степеней свободы молекулы:
- сумма числа поступательных, числа вращательных и удвоенного числа колебательных степеней свободы молекулы:
 .
.
Скорости молекул газа:
среднеквадратичная -  ;
;
среднеарифметическая -  ;
;
наиболее вероятная -  ,
,
где  - масса одной молекулы,
- масса одной молекулы,  - молярная масса газа.
- молярная масса газа.
Среднее число соударений, испытываемых одной молекулой газа в единицу времени:
 ,
,
где  – эффективный диаметр молекулы;
– эффективный диаметр молекулы;  – концентрация молекул;
– концентрация молекул;
 – среднеарифметическая скорость молекул.
– среднеарифметическая скорость молекул.
Средняя длина свободного пробега молекул газа:
 .
.
Физические основы термодинамики
Первое начало термодинамики:  ,
,
где  - количество теплоты, переданное газу;
- количество теплоты, переданное газу;  - изменение внутренней энергии газа и
- изменение внутренней энергии газа и  - элементарная работа, совершаемая газом против внешних сил.
- элементарная работа, совершаемая газом против внешних сил.
Элементарная работа, совершаемая газом против внешних сил:
 ,
,
где  - давление,
- давление,  - изменение объема газа.
- изменение объема газа.
Работа, совершаемая газом при изменении его объема от  до
до  :
:
 .
.
Работа, совершаемая газом в изобарном процессе:
 ,
,
где  и
и  - начальная и конечная термодинамические температуры газа.
- начальная и конечная термодинамические температуры газа.
Работа, совершаемая газом в изотермическом процессе:
 .
.
где  и
и  - начальное и конечное давления газа.
- начальное и конечное давления газа.
Связь между молярной  и удельной
и удельной  теплоемкостями вещества:
теплоемкостями вещества:
 , где
, где  - молярная масса вещества.
- молярная масса вещества.
Молярные теплоемкости газа при постоянном объеме  и постоянном давлении
и постоянном давлении  :
:
 и
и 
 ,
,
где  - сумма числа поступательных, числа вращательных и удвоенного числа колебательных степеней свободы молекулы.
- сумма числа поступательных, числа вращательных и удвоенного числа колебательных степеней свободы молекулы.
Уравнение Майера:  ,
,
где  и
и  - молярные теплоемкости газа при постоянном давлении и постоянном объеме,
- молярные теплоемкости газа при постоянном давлении и постоянном объеме,  - универсальная газовая постоянная.
- универсальная газовая постоянная.
Внутренняя энергия идеального газа:  ,
,
где  - молярная теплоемкость газа при постоянном объеме.
- молярная теплоемкость газа при постоянном объеме.
Уравнения Пуассона, связывающие термодинамические параметры идеального газа в адиабатном процессе:
|
|
|
 ;
;  ;
;  ,
,
где  - показатель адиабаты.
- показатель адиабаты.
Работа, совершаемая газом в адиабатическом процессе:
 ,
,
где  .
.
Коэффициент полезного действия (К.П.Д.) тепловой машины:
 ,
,
где  - полезная работа, совершаемая тепловой машиной за один цикл;
- полезная работа, совершаемая тепловой машиной за один цикл;
 - количество теплоты, полученное рабочим телом от нагревателя, и
- количество теплоты, полученное рабочим телом от нагревателя, и
 - количество теплоты, отданное рабочим телом холодильнику за один цикл.
- количество теплоты, отданное рабочим телом холодильнику за один цикл.
Термический К.П.Д. цикла Карно:  ,
,
где  и
и  - термодинамические температуры нагревателя и холодильника.
- термодинамические температуры нагревателя и холодильника.
Изменение энтропии системы:
 ,
,
где  и
и  – пределы интегрирования, соответствующие начальному и конечному состояниям системы. Так как процесс равновесный, то интегрирование не зависит от формы пути системы, совершающей переход из одного состояния в другое.
– пределы интегрирования, соответствующие начальному и конечному состояниям системы. Так как процесс равновесный, то интегрирование не зависит от формы пути системы, совершающей переход из одного состояния в другое.
Формула Больцмана:
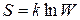 ,
,
где  – энтропия системы;
– энтропия системы;  – термодинамическая вероятность ее состояния;
– термодинамическая вероятность ее состояния;  –постоянная Больцмана.
–постоянная Больцмана.
Контрольное задание №2
Вариант 1
1. В сосуде при давлении 105 Па и температуре 270С находится смесь азота, кислорода и гелия, массы которых равны. Найти плотность смеси газов.
2. Найти формулу некоторого соединения углерода с водородом, если известно, что это вещество массой 0,66 г в газообразном состоянии при температуре 270С в объеме 1 дм3 создает давление 105 Па.
3. Подсчитать число молекул, содержащихся в углекислом газе массой 100 г. Найти массу молекулы и концентрацию молекул при нормальных условиях. Плотность газа при нормальных условиях равна 1,94 кг/м3 .
4. Плотность газа в баллоне газонаполненной электрической лампы равна 0,9 кг/м3. При горении лампы давление в ней возросло с 80 кПа до 110 кПа. Насколько увеличилась при этом среднеквадратичная скорость молекул газа?
5. Определить, во сколько раз среднеквадратичная скорость пылинки массой 1,75·10-12 кг, взвешенной в воздухе, меньше среднеквадратичной скорости движения молекул воздуха.
6. В закрытом сосуде находится 3 моля гелия при температуре 270 С. На сколько процентов увеличится давление в сосуде, если газу сообщить 3 кДж теплоты?
7. Одноатомный идеальный газ находятся в баллоне объемом 10 л при давлении 105 Па. Какова внутренняя энергия газа?
8. Для нагревания газа массой 1 кг на 1К при постоянном давлении требуется 912 Дж теплоты, а при постоянном объеме – 649 Дж теплоты. Какой это газ?
|
|
|
9. В вертикальном цилиндре под тяжелым поршнем находится кислород массой 2 кг. Для повышения температуры кислорода на 5 К ему было сообщено 9160 Дж теплоты. Найти удельную теплоемкость кислорода ср, работу, совершаемую им при расширении и увеличении его внутренней энергии. Молярная масса кислорода 0,032 кг/моль.
Вариант 2
1. Два сосуда, наполненных воздухом при давлениях соответственно Р1=0,8 МПа и Р2 =0,6 МПа, имеют объемы V1 =3л и V2 =5л. Сосуды соединяют трубкой, объемом которой можно пренебречь по сравнению с объемами сосудов. Найти установившееся давление в сосудах. Температуру считать постоянной.
2. При давлении 2×106 Па идеальный газ занимает объем 5 литров. В результате изотермического расширения его объем увеличился на 1 л, а концентрация молекул стала равной n=3,62×1026 м-3. При какой температуре протекал этот процесс?
3. Средняя энергия молекулы одноатомного идеального газа равна 0,038 эВ (1эВ =1,6×10-19 Дж). Давление газа равно 0,2 МПа. Найти число молекул в одном кубическом метре газа.
4. Определить наиболее вероятную скорость молекул газа, плотность которого при давлении p = 40 кПа составляет r = 0,37 кг/м3.
5. Во сколько раз изменится средняя квадратичная скорость молекул идеального газа при увеличении его объема в 2 раза? Давление газа при этом увеличится в 3 раза, масса неизменна.
6. В цилиндре объемом V1 =190 см3 под поршнем находится газ при температуре Т1=323 К. Найти работу расширения газа при нагревании его на ∆Т=100 К. Масса поршня m = 120 кг, его площадь S = 50 см 2. Атмосферное давление р0=0,1 МПа.
7. Некоторая масса газа, занимающего объем V1 = 0,01 м 3, находится при давлении р1=0,1 МПа и температуре Т1 = 300 К. Газ нагревается вначале при постоянном объеме до температуры Т2 = 320 К, а затем при постоянном давлении до температуры Т3= 350 К. Найти работу, совершаемую газом, при переходе из состояния 1 в состояние 3.
8. Удельная теплоемкость газа при постоянном давлении равна 912 Дж/кг×К, а при постоянном объеме 649 Дж/кг×К. Определить молекулярный вес газа и число степеней свободы его молекул.
|
|
|
9. Коэффициент полезного действия цикла Карно равен 0,3. При изотермическом расширении газ получил от нагревателя 200 Дж энергии. Определить работу, совершаемую при изотермическом сжатии.
Вариант 3
1. Определить плотность смеси газов, находящихся при давлении 1 МПа и температуре 270С. Смесь состоит из 5 киломолей азота, 1,5 киломолей кислорода и 0,5 киломоля углекислого газа.
2. Какова температура Т газа, находящегося под давлением р = 0,5 МПа, если в сосуде объемом V =1,5 л содержится N = 1,8×1024 молекул?
3. Какое давление на стенки сосуда производят молекулы газа, если масса газа 3 г, объем 50 л, а средняя скорость молекул 500 м/с?
4. Плотность неизвестного газа равна r = 0,09 кг/м3 . При этом в объеме V = 0,1 м3 содержится N = 2,7×1024 молекул. Какой это газ?
5. В воздухе взвешена пылинка массой m=1,242×10-20 кг. Температура воздуха Т=300 К. Подсчитать среднеквадратичную скорость пылинки и ее кинетическую энергию.
6. Какую работу совершает кислород массой m = 0,32 кг при изобарном нагревании на ∆Т=20 К?
7. Один киломоль газа при изобарическом расширении совершает работу А=831 кДж. В исходном состоянии объем газа V1 =3 м3 , а температура Т1=300 К. Каковы параметры р2,V2,T2 после расширения?
8. Кислород массой m = 2 кг занимает объем V1 = 1 м3 и находится под давлением p1 = 0,2 МПа. При нагревании газ расширяют в условиях постоянного давления до объема V2 = 3 м3, а затем его давление увеличивают до p3 = 0,5 МПа при неизменном объеме. Найти изменение внутренней энергии DU газа, совершенную им работу A и теплоту Q, переданную газу. Построить график процесса.
9. Температура нагревателя 2270 С. Определите КПД идеального двигателя и температуру холодильника, если за счет каждого килоджоуля теплоты, полученного от нагревателя, двигатель совершает 350 Дж механической работы.
Вариант 4
1. В сосуде при температуре 1000С и давлении 4×105 Па находится 2 м3 смеси кислорода и сернистого газа. Определить парциальное давление компонентов, если масса сернистого газа 8 кг.
2. Плотность неизвестного газа равна 0,09кг/м3 . При этом в объеме 0,1 м3 содержится 2,7×1024 молекул. Какой это газ? Определите его молярную массу.
3. Найти среднюю длину пробега молекулы азота при 00С и давлении 10-3 мм рт.ст.
4. Во сколько раз изменится среднеквадратичная скорость молекул идеального газа при увеличении его объема в 2 раза? Давление газа при этом увеличится в 3 раза, масса неизменна.
5. Молекула кислорода, ударившись о стенку сосуда, передала ей импульс ∆р=5,06×10-23 кг×м/с. Найти температуру газа в сосуде, если скорость данной молекулы была направлена под углом a = 300 к стенке и равнялась удвоенной среднеквадратичной скорости.
|
|
|
6. Какова удельная теплоемкость при постоянном объеме некоторого двухатомного газа, если плотность этого газа при нормальных условиях равна 6,3 кг/м3?
7. В закрытом сосуде находится смесь азота массой 56 г и кислорода массой 64 г. Определить изменение внутренней энергии этой смеси, если ее охладили на 200 С.
8. Водород массой 40 г, имевший температуру 300 К, адиабатически расширяется; при этом объем газа возрастает втрое. Затем при изотермическом сжатии объем газа уменьшается в 2 раза. Определить полную работу, совершенную газом, и конечную температуру газа. Построить график процесса.
9. Газ совершает цикл Карно: 2/3 теплоты, полученной от нагревателя, отдается охладителю. Температура охладителя 280 К. Определить температуру нагревателя.
Вариант 5
1. Некоторая масса водорода находится при температуре Т1 =200 К и давлении р1 =0,4кПа. Газ нагревают до температуры Т2 =10000 К, при которой молекулы водорода практически полностью распадаются на атомы. Найти давление р2 газа, если его объем и масса остались без изменения.
2. Сосуд разделен пополам полупроницаемой перегородкой. Объем каждой части – 1 л. В левую половину введены водород массой 2 г и азот массой 28 г. Справа от перегородки – вакуум. Какое давление установится в обеих частях сосуда, если перегородка пропускает только водород, а температура остается постоянной и равной 373 К?
3. Какое давление на стенки сосуда оказывает кислород, если средняя квадратичная скорость его молекул равна 400 м/с, а в объеме V = 1 см3 содержится N = 2,7·1019 молекул?
4. Найти концентрацию молекул кислорода, если его давление равно p = 0,2 МПа, а средняя квадратичная скорость его молекул <vкв> = 700 м/с.
5. Плотность газа в баллоне газонаполненной электрической лампы равна r = 0,9 кг/м3. При горении лампы давление в ней возросло с p1 = 80 кПа до p2 = 110 кПа. Насколько увеличилась при этом средняя квадратичная скорость молекул газа?
6. В закрытом воздухе объемом 61 л находятся равные массы аргона и азота при нормальных условиях. Какое количество теплоты нужно сообщить этой газовой смеси, чтобы нагреть ее на 600С?
7. В теплоизолированном цилиндре с поршнем находится азот массой m=0,2 кг при температуре t1=200 C. Азот, расширяясь, совершает работу А= 4,47 кДж. Найти изменение внутренней энергии азота ΔU и его температуру t2 после расширения. Удельная теплоемкость азота при постоянном объеме – Сv=745 Дж/кг×К.
8. Объем газа при адиабатическом сжатии уменьшился в 10 раз, а давление увеличилось в 21,4 раза. Определить соотношение удельной теплоемкости при постоянном давлении и удельной теплоемкости при постоянном объеме.
9. Газ совершает цикл Карно. Температура охладителя 170 С. Как изменится КПД цикла, если температура нагревателя повысилась от 127 до 4470 С?
Вариант 6
1. В баллоне емкостью 10 л содержится окисел азота (NO) под давлением 8 атм. Определить массу газа и массу его молекулы. Температура 15°С.
2. Из баллона со сжатым газом вследствие неисправности вентиля вытекал газ. Какая часть газа осталась в баллоне, если первоначально при температуре 27°С манометр показывал давление 60 атм, а через некоторое время при температуре 12°С – 19 атм?
3. Определить среднюю кинетическую энергию поступательного движения молекул газа, находящегося под давлением 0,3 Па. Концентрация молекул равна 1013 см-3.
4. Найти среднюю длину свободного пробега молекул азота при 0°С и давлении 10-3 мм рт. ст. Диаметр молекулы принять равным 0,3 мм.
5. 2,18 кг двухатомного газа находится под давлением 7,8·105 Па и имеет плотность 6,28 кг/м3. Найти энергию теплового движения молекул газа при этих условиях.
6. При изотермическом расширении водорода массой 1 г объем увеличился в 2 раза. Определить работу расширения и количество тепла, переданного телу. Температура водорода 300 К.
7. Удельная теплоемкость газа при постоянном давлении равна 912 Дж/кг×К, а при постоянном объеме 649 Дж/кг×К. Определить молекулярный вес газа и число степеней свободы его молекул.
8. Кислород массой 2 кг занимает объем 1 м3 и находится под давлением 0,2 МПа. Газ был нагрет сначала при постоянном давлении до объема 3 м3, а затем при постоянном объеме до давления 0,5 МПа. Найти изменение внутренней энергии газа, совершаемую им работу и теплоту, переданную газу. Построить график процесса.
9. Двигатель работает как машина Карно и за цикл получает от нагревателя 3 кДж тепла. Температура нагревателя 600 К, температура холодильника 300 К. Найти совершившуюся за цикл работу и количество теплоты, отдаваемое при этом холодильнику.
Вариант 7
1. Баллон объемом 0,015 м3 содержит 7·10-3 кг азота и 4,5·10-3 кг водорода при температуре 27°С. Определить давление смеси.
2. В баллоне, объем которого равен 10 л, находится гелий под давлением 105 Па и при температуре 27°С. После того как из баллона была взята проба массой 10 г, давление в баллоне понизилось до 0,9·105 Па. Определить температуру гелия, оставшегося в баллоне.
3. В сосуде, объем которого 1 л, содержится 5 г идеального газа под давлением 500 гПа. Определить среднеквадратичную скорость молекул газа.
4. Найти концентрацию молекул кислорода, если его давление равно 0,2 МПа, а средняя квадратичная скорость молекул 700 м/с.
5. Средняя квадратичная скорость молекул некоторого газа равна 480 м/с при температуре 296 К. Сколько молекул содержится в 10-ти г этого газа?
6. Одноатомный идеальный газ изотермически расширился из состояния с давлением 106 Па и объемом 1 л вдвое. Найти внутреннюю энергию газа в конечном состоянии.
7. Одному молю двухатомного газа сообщили 20 Дж тепла, в результате чего газ нагрелся на несколько градусов при постоянном объеме. Какое количество тепла нужно сообщить метану массой 30 г, чтобы нагреть его на такое же число градусов при постоянном давлении?
8. При изобарическом нагревании от температуры 20°С до температуры 50°С газ совершает работу в 2,5 кДж. Определить число молекул, участвующих в этом процессе.
9. Некоторая масса газа, занимающего объем V1 = 0,01 м 3, находится при давлении р1 = 0,1 МПа и температуре Т1 = 300 К. Газ нагревается вначале при постоянном объеме до температуры Т2 = 320 К, а затем при постоянном давлении до температуры Т3 = 350 К. Найти работу, совершаемую газом, при переходе из состояния 1 в состояние 3.
Вариант 8
1. В сосуде объемом 10 л находится 2·1023 молекул газа. Какова температура газа, если давление в сосуде равно 0,12 МПа?
2. В баллоне находится газ массой 10 кг при давлении 10 МПа. Какую массу взяли из баллона, если давление стало равным 2,5 МПа? Температуру газа считать постоянной.
3. На сколько процентов увеличится среднеквадратичная скорость молекул водяного пара при повышении его температуры от 370С до 400С?
4. Кинетическая энергия поступательного движения молекул азота, находящегося в баллоне объемом 6,68 м3, равна 7,9·104 Дж, а среднеквадратичная скорость его молекул составляет 7·103 м/с. Найти массу азота в баллоне.
5. При некоторой температуре молекулы кислорода имеют среднеквадратичную скорость 460 м/с. Какова при этой температуре среднеквадратичная скорость молекул азота?
6. Вычислить величину отношений удельных теплоемкостей для газовой смеси, состоящей из 5-ти киломолей кислорода и 6-ти киломолей углекислого газа. Газы считать идеальными.
7. Кислород, взятый при температуре 270 С, изобарически сжали до объема, в 5 раз меньшего первоначального. Определить работу внешней силы при сжатии, если масса газа равна 160 г.
8. Водород массой 2 кг при температуре 300 К охлаждают изохорически так, что его давление падает в 3 раза. Затем водород изобарически расширяют. Найти работу газа, если его конечная температура равна начальной.
9. Кислород массой 2 кг занимает объем 1 м3 и находится под давлением 0,2 МПа. При нагревании газ расширяют в условиях постоянного давления до объема 3 м3, а затем его давление увеличивают до 0,5 МПа при неизменном объеме. Найти изменение внутренней энергии газа, совершенную им работу и теплоту, переданную газу. Построить график процесса.
Вариант 9
1. В баллоне, объем которого 719 м3, находится газ, состоящий из смеси углекислого газа и паров воды. Температура газа 513°С. Число молекул углекислого газа 8,35·1022, число молекул паров воды 5,87·1022. Вычислить давление газовой смеси.
2. Тонкий резиновый шар радиуса 2 см заполнен воздухом при температуре 200С и давлении 0,1 МПа. Каков будет радиус шара, если его опустить в воду с температурой 40С на глубину 20 м?
3. Подсчитать число молекул, содержащихся в углекислом газе массой m = 100 г. Найти массу молекулы и концентрацию молекул при нормальных условиях. Плотность газа при нормальных условиях равна r = 1,94 кг/м3.
4. Гелий находится при температуре 270 С. Кинетическая энергия теплового движения всех молекул газа Ек=10 Дж. Определить число молекул.
5. При температуре 300 К плотность газа равна 1,2 кг/м3, а среднеквадратичная скорость молекул составляет 500 м/с. Найти концентрацию молекул газа.
6. Азот массой 10 г расширяется изотермически при температуре -200С, при этом давление меняется от 202 до 101 кПа. Определить работу расширения, изменение внутренней энергии азота и количество сообщенной ему теплоты.
7. Удельная теплоемкость газа при постоянном давлении равна 912 Дж/кг×К, а при постоянном объеме 649 Дж/кг×К. Определить молекулярный вес газа и число степеней свободы его молекул.
8. Азот, находившийся при температуре 400 К, подвергли адиабатическому расширению, в результате которого его объем увеличился в 5 раз, а внутренняя энергия уменьшилась на 4 кДж. Определить массу азота.
9. Температура нагревателя идеальной тепловой машины t1=1170C, а холодильника –t2 =270C. Количество теплоты, получаемое машиной от нагревателя за 1 с, равно Q = 60 кДж. Вычислить КПД машины, количество теплоты, отдаваемое холодильнику за 1 с, и мощность машины.
Вариант 10
1. При какой температуре кислород, находясь под давлением 0,2 МПа, имеет плотность 1,2 кг/м3? Какова при этом концентрация молекул кислорода?
2. Каково давление смеси газов в колбе, если в каждом кубическом сантиметре находится 1020 молекул кислорода и 3∙1020 молекул азота. Температура смеси 1500 С.
3. Определить наиболее вероятную скорость молекул газа, плотность которого при давлении 40 кПа составляет 0,37 кг/м3.
4. Среднеквадратичная скорость молекул некоторого газа равна 851 м/с. Давление газа составляет 7,4∙105 Па. Найти плотность газа при этих условиях.
5. В сосуде, объем которого 3 л, находится кислород массой 3 г при температуре 130 С. Определить внутреннюю энергию газа и давление газа на стенки сосуда.
6. Найти удельную теплоемкость при постоянном объеме для газовой смеси, масса киломоля которой равна 22 кг, а отношение удельных теплоемкостей равно 1,395.
7. Работа расширения некоторого двухатомного идеального газа составляет 2 кДж. Определить количество подведенной к газу теплоты, если процесс протекает изобарно.
8. Один моль идеального двухатомного газа, находящийся под давлением в 1 атм при температуре 270 С, нагревается при постоянном объеме до давления в 2 атм. После этого газ изотермически расширяется до начального давления и затем изобарически сжимается до начального объема. Начертить график цикла. Определить температуры газа для характерных точек цикла.
9. Газ, совершающий цикл Карно, получает от нагревателя 42 кДж теплоты. Какую работу совершает газ, если абсолютная температура нагревателя в 3 раза выше, чем температура холодильника?
|
|
|


