 |
Тема: Кинетика химических и биохимических реакций. Химическое равновесие
|
|
|
|
Тема: Тепловые эффекты химических реакций. Термодинамические характеристики химических и биохимических процессов
3.Контроль усвоения темы ( тесты для самоконтроля уровня текущих знаний).
Образец теста
1. Система, которая не может обмениваться веществом с окружающей средой, но может обмениваться с ней энергией и работой называется _____ системой.
1) изолированной
2) закрытой
3) равновесной
4) открытой
2. Окружающая среда, как и система, обладает соответствующими свойствами, т.е. параметрами. Из внешних параметров обычно учитывают только _____.
1) давление и температуру
2) плотность и концентрацию
3) концентрацию и давление
4) химический потенциал и давление
3.  , применяемая в медицинской практике в качестве антисептика, а также антидота при отравлении марганцовокислым калием, неустойчивое соединение, медленно разлагающееся под действием света. В этой связи термодинамической функцией, которая служит критерием данного процесса при постоянной температуре и объеме является _____.
, применяемая в медицинской практике в качестве антисептика, а также антидота при отравлении марганцовокислым калием, неустойчивое соединение, медленно разлагающееся под действием света. В этой связи термодинамической функцией, которая служит критерием данного процесса при постоянной температуре и объеме является _____.
1) энтальпия
2) энергия Гиббса
3) энергия Гельмгольца
4) внутренняя энергия
4. Внутренней энергией системы называется ______.
1) кинетическая энергия движения молекул
2) суммарный запас всех видов энергии
3) потенциальная энергия системы
4) энергия притяжения электронов к ядру
5. Если в ходе процесса при постоянном давлении системой совершается только работа расширения, то для внутренней энергии справедливо выражение _____.
1) 
2) 
3) 
4) 
6. Химическая реакция обязательно сопровождается выделением или поглощением энергии, поскольку _____.
1) для ее протекания необходима энергия, равная энергии активации
2) её протекание требует столкновения реагирующих частиц
|
|
|
3) её протекание заключается в разрыве одних, и образовании других химических связей
4) при её протекании количество атомов до и после реакции остается постоянным
7. Энергия, освобождающаяся при окислении питательных веществ в процессе _____ не используется.
1) синтеза АТФ
2) теплопродукции
3) гидролиза концевой фосфоангидридной связи АТФ
4) сокращения мышц
8. В молекуле АТФ макроэргической связью является- _____.
1) гликозидная
2) фосфоэфирная
3) фосфоангидридная
4) водордная
9. На синтез одной молекулы глюкозы в реакции темновой фазы фотосинтеза затрачено АТФ ______.
1) 3
2) 6
3) 18
4) 12
10. В ходе циклического фотофосфорилирования происходит _____.
1) восстановление НАДФН
2) восстановление НАДН
3) синтез АТФ
4) фотоокисление воды
11. Конечными продуктами обмена веществ являются: _____.
1) мочевина,  ,
, 
2) пируват, мочевина, АТФ
3) ацетил-КоА,  , пируват
, пируват
4)  ,
,  , ацетил-КоА
, ацетил-КоА
12. Часть энергии системы, которую можно использовать для совершения работы при постоянной температуре и давлении, называется _____.
1) энтальпией
2) связанной энергией
3) свободной энергией
4) энтропией
13. Для замыкания гликозидной связи при синтезе сахарозы необходимо свободной энергии _____ кДж.
1) 5-10
2) 10-15
3) 20-30
4) 45-50
14. Все биохимические процессы в организме человека протекают при постоянном давлении и температуры, тип такого процесса называется _____.
1) изотермическим
2) изохорным
3) изобарно- изотермическим
4) адиабатическим
15. В реальных системах термодинамический процесс может сопровождаться как увеличением, так и уменьшением энтропии, поэтому данная характеристика уменьшается, как правило, при _____.
1) плавлении
2) испарении
3) полимеризации
4) диссоциации
16. Первый закон термодинамики является отображением всеобщего принципа сохранения и превращения энергии, поэтому математическое выражение этого закона имеет вид: _____.
|
|
|
1) 
2) 
3) 
4) 
17. Максимальная калорийность пищевых продуктов вычисляется на основании методов термохимии путем определения теплоты сгорания продуктов с помощью прибора - _____.
1) осмометра
2) вискозиметра
3) калориметрической бомбы
4) калориметра
18. Закон Гесса позволяет рассчитывать тепловые эффекты реакций (процесс образования продуктов), протекающих в животных и растительных организмах, поэтому данным условиям удовлетворяет уравнение: _____.
1) 
2) 
3) 
4) 
19. Для следующих нижеуказанных систем –______ применим второй закон термодинамики, который отражает факторы, определяющие направление и глубину протекания химических реакций.
1) изолированных, гетерогенных
2) закрытых, гомогенных
3) открытых, гетерогенных
4) закрытых гетерогенных
20. Необратимые процессы старения организма связаны с изменением энтропии, поэтому тип данной энергии в биологии расценивают, как _____.
1) связанный
2) внутренний
3) полной энергией системы
4) рассеянной
21. Изменение свободной энергии Гиббса /  / – это максимальная работа, которую организм выполняет за определенное время, для расчета который справедливо выражение _____.
/ – это максимальная работа, которую организм выполняет за определенное время, для расчета который справедливо выражение _____.
1) 
2) 
3) 
4) 
22. В биоэнергетике при изучении биохимических реакций принято пользоваться значениями  при рН = 7. При этом процессы дыхания и усвоения пищи, протекающие при
при рН = 7. При этом процессы дыхания и усвоения пищи, протекающие при  в системе, называются ______.
в системе, называются ______.
1) эндэргоническими
2 эндотермическими
3) экзэргоническими
Тема: Кинетика химических и биохимических реакций. Химическое равновесие
3. Контроль усвоения темы ( тесты для самоконтроля уровня текущих знаний).
Образец теста
1. «При увеличении температуры на 10 градусов скорость большинства химических реакций увеличивается в 2-4 раза» – это формулировка _____.
1) закона действующих масс
2) закон Генри
3) правила Вант-Гоффа
4) закона Гесса
2. Отношение произведения равновесных активностей продуктов реакции, взятых в степенях, равных их стехиометрическим коэффициентам, к такому же произведению активностей исходных веществ при данной температуре есть величина постоянная, называемая _____.
1) константой химического равновесия
2) степенью диссоциации
3) свободной энергией Гиббса
4) константой скорости реакции
3. Если температурный коэффициент скорости равен 3, то при увеличении температуры от  до
до  скорость химической реакции _____ раз.
скорость химической реакции _____ раз.
|
|
|
1) увеличится в 27 раз
2) уменьшится в 27 раз
3) увеличится в 81 раз
4)уменьшится в 81 раз
4. Количественное влияние температуры на скорость химической реакции выражается уравнением _____.
1) Вант-Гоффа
2) Аррениуса
3) Фарадея
4) Рауля
5. Реакция окисления этанола в организме человека идет по уравнению:  . При повышении концентрации исходных веществ в 5 раз скорость данной реакции _____раз.
. При повышении концентрации исходных веществ в 5 раз скорость данной реакции _____раз.
1) уменьшится в 25 раз
2) увеличится в 25 раз
3) уменьшится в 5 раз
4) увеличится в 5 раз
6. В организме человека тростниковый сахар (сахароза) под влиянием ферментов превращается в глюкозу и фруктозу. Если увеличить температуру на  при
при  =3, то скорость этой реакции _____ раз (а).
=3, то скорость этой реакции _____ раз (а).
1) уменьшится в 3 раз
2) увеличится в 9 раз
3) уменьшится в 9 раз
4) увеличится в 27 раз
7. Величина  (константа равновесия) зависит от _____ и рекомендуют ёё использовать для характеристики смещения равновесия биохимических процессов.
(константа равновесия) зависит от _____ и рекомендуют ёё использовать для характеристики смещения равновесия биохимических процессов.
1) концентрации реагирующих веществ
2) катализатора
3) давления
4) природы реагирующих веществ и температуры
8. Реакция окисления глюкозы в организме человека протекает по уравнению:  . Кинетическое уравнение скорости этой реакции имеет вид: _____.
. Кинетическое уравнение скорости этой реакции имеет вид: _____.
1) 
2) 
3) 
4) 
9. В растениях в процессе фотосинтеза с участием природного катализатора пигмента (хлорофилла) за счет солнечной энергии образуется глюкоза по схеме:  , Кинетическое уравнение скорости этой реакции имеет вид: _____.
, Кинетическое уравнение скорости этой реакции имеет вид: _____.
1) 
2) 
3) 
4) 
10. Порядок реакции для указанной реакции:  имеет вид: _____.
имеет вид: _____.
1) 0
2) 1
3) 2
4) 3
11. При повышении давления в 4 раза скорость химической реакции:  увеличивается в _____ раз (а).
увеличивается в _____ раз (а).
1) 64
2) 124
3) 924
4) 1024
12. Бикарбонат натрия, применяющийся в медицине при отравлении циклическими антидепрессантами, подвергается гидролизу по реакции:  . Уравнение константы равновесия этой реакции имеет вид: _____.
. Уравнение константы равновесия этой реакции имеет вид: _____.
1) 
2) 
3) 
4) 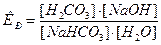
13. Температурный оптимум действия ферментов в живом организме в градусах составляет_____  .
.
1) 35-40
2) 65-70
3) 15-20
4) 0-10
1. с.
|
|
|


