 |
Техническая характеристика ВСН – 3.
|
|
|
|
Техническая характеристика ВСН – 3.
Предел измерения касательных напряжений сдвига (предельного статического
напряжения сдвига) в Па для пружин: №1……………………………... …. 0 – 45
№2…………………………………0 – 90
Предел измерения динамической вязкости ньютоновских жидкостей при 200
об/мин гильзы в Па∙ с для пружин: №1…………………………….. 0, 001 – 0, 2
№2……………………………... 0, 001 – 0, 4
Частота вращения гильзы, об/мин… ………………... ……. 0, 2; 200; 300; 400; 600
Основная приведенная погрешность измерения, %, не более:
касательных напряжений сдвига…………………………………….. 4
динамической вязкости……………………………………………….. 5
Погрешность отсчета угла поворота измерительного элемента, градус……... …… 
Ток переменный напряжением, В……………………………………….. ………… 
Предел термостатирования,  …………………………………………………….. 20 – 60
…………………………………………………….. 20 – 60
При измерениях с помощью трансмиссии и редуктора прибора ВСН – 3 гильза 11 может вращаться с частотой 0, 2 (для определения статического напряжения сдвига), 200, 300, 400 и 600 мин-1 (для определения реологических параметров).
Для проведения измерений испытуемый раствор заливается в стакан 13 до риски на внутренней его поверхности. С помощью телескопического стола 14 этот стакан фиксируется в верхнем положении. При этом промывочная жидкость находиться в зазоре между гильзой 11 и цилиндром 12. При вращении гильза крутящий момент передается жидкости в зазоре. Скорость вращательного движения концентрических слоев жидкости в зазоре уменьшается по направлению от вращающегося цилиндра к измерительному. Между слоями жидкости возникают касательные напряжения сдвига, и чем они больше, тем выше касательные напряжения в жидкости и крутящий момент, передающийся измерительному цилиндру. Об этом свидетельствует увеличение угла поворота этого цилиндра.
|
|
|
Используя различные скорости вращения наружного цилиндра, измеряют угол поворота измерительного цилиндра 12 по шкале 8 пропорциональный величине касательного напряжения в жидкости.
После проведения измерений на приборе ВСН – 3 строится реограмма в координатах n (частота вращения, мин-1) и φ (угол закручивания пружины прибора, град. ), образец которой приведен на рис. 4. 8.
n, мин-1
 |
n2
α
n1
 φ, град
φ, град
φ О φ 1 φ 2
Рис. 6. 8. Образец реограммы, получаемой при измерениях на приборе ВСН-3.
На этой реограмме обычно выделяется прямолинейный участок с углом наклона α. Обработка этой реограммы позволяет получить основные реологические параметры:
- пластическая вязкость:
 , (6. 3)
, (6. 3)
Если учесть свойства пружины и геометрические размеры подвесной системы коэффициентом К1 и помня, что  (угол закручивания пружины при частоте 300 мин-1), а
(угол закручивания пружины при частоте 300 мин-1), а  (тоже при частоте 600 мин-1), то выражение (4. 3) запишется в виде:
(тоже при частоте 600 мин-1), то выражение (4. 3) запишется в виде:
 , Па∙ с (6. 4)
, Па∙ с (6. 4)
- динамическое напряжение сдвига:
находится через величину отрезка  по абсциссе:
по абсциссе:
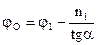 , (6. 4)
, (6. 4)
Величину  можно уподобить динамическому напряжению сдвига
можно уподобить динамическому напряжению сдвига  , если учесть константы прибора К1 и К2, и что
, если учесть константы прибора К1 и К2, и что  (угол закручивания пружины при частоте 300 мин-1), тогда:
(угол закручивания пружины при частоте 300 мин-1), тогда:
|
|
|
 , Па (6. 5)
, Па (6. 5)
- эффективная (кажущаяся) вязкость:
находится из соотношения:
 , (6. 6)
, (6. 6)
где: m = 32, 2 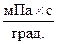 - константа пружины №2;
- константа пружины №2;
ω – угловая частота,  ;
;
φ 600 – угол закручивания при частоте n-1.
Приняв n = 600 мин-1 и определив φ 600 можно получить:
 , мПа∙ с (6. 7)
, мПа∙ с (6. 7)
Для пружины №2:
К1 = 10-3; К2 = 0, 3; К3 = 103.
6. 3. Материалы и реагенты. Глины
Глина является основным структуро- и коркообразователем. Отличительной особенностью глин является их способность адсорбировать молекулы воды при получении водного раствора (суспензии). Глинистые минералы, в состав которых входят окиси кремния (SiО2), обычно в природных условиях содержат гидратационную воду, поэтому по химическому составу они являются гидросиликатами. В зависимости от преобладающих окислов в составе гидросиликатов их подразделяют на глиноземистые, содержащие Al2О3 (каолинит, монтмориллонит и др. ), железистые – Fе2О3 (гидрослюды) и магнезиальные – MgО (сепиолит палыгорскитовые).
Каолинит – глинообразующий минериал, состав которого отвечает формуле Al2O3·2H2O·2SiO2, имеет цвет от белого до светло серого. В состав каолинитовой глины также входят минералы галлуазит, диккит, аноксит, энделлит.
Основной особенностью минералов этой группы является то, что глинистые частицы толщиной 0, 05÷ 0, 2 мкм имеют шестиугольную форму поперечным размером 0, 3÷ 4, 0 мкм. Кристаллическая решетка таких минералов не имеет свободных зарядов на поверхности за счет замещений в пределах этой решетки. Поэтому такие глинистые частицы имеют между собой жесткую связь, молекулы воды плохо взаимодействуют с поверхностью глинистых частиц, что обусловливает неспособность глины набухать, гидратироваться из-за неэффективного проникновения молекул воды в их межслоевое пространство.
Монтмориллонитовая глина отвечает формуле Al2O3·4SiO2·H2O, имеет цвет от светло-серого до серо-зеленого цвета. Глинообразующими этой группы минералов являются также сапонит, вергликулит, нотронит, бейделит и др.
|
|
|
Характерной для монтмориллонитовых глин является форма частиц в виде чешуек поперечным размером 0, 01÷ 0, 4 мкм, что в десятки, сотни раз превышает их толщину. Основные свойства таких глин:
- в разрезе частица глины образует две параллельные плоскости;
- краевые части глинистых частиц представляют собой обломки кристаллов с наличием нескомпенсированных зарядов;
- поверхность глинистых частиц несет на себе отрицательные заряды, а также обменные катионы Nа+ если глина образовалась в морском, и Са++ - в пресноводном бассейне;
- для кристаллической решетки монтмориллонита характерны изоморфные замещения в пределах кристаллической решетки, что обусловливает ее электрическую несбалансированность и присутствие обменных катионов Nа+ или Са++ на плоскостях и краях глинистых частиц;
- в межполосное пространство глинистых частиц эффективно проникают молекулы воды, приводя к их гидратации, набуханию и диспергированию.
Указанные выше свойства обусловливают то, что монтмориллонитовые глины являются наиболее технологичными при получении глинистых растворов. Стабильные суспензии глин в воде получаются при их невысокой концентрации.
Основным недостатком растворов, приготовленных из монтмориллонитовых глин, является ухудшение свойств в случае агрессии катионов Са++, Mg++ и др. из пластовых отложений, что усложняет процесс приготовления и регулирования свойств таких растворов.
Гидрослюдистые глинообразующие минералы имеют формулу
(ОН)4Ку(Si(8-у)·Alу)(Al4·Fe4·Mg4·Mg6)O20. Для разновидностей гидрослюд: гидромусковита у=2, иллита у=1, 0÷ 1, 5. Минералы этой группы имеют рыжевато-бурый цвет. Основной особенностью их является наличие в межслоевом пространстве остаточных катионов К+, что обусловливает затруднение в проникновении молекул воды, и уменьшение их адсорбции на плоскостях и гранях глинистых частиц.
|
|
|
Такие глинистые минералы являются комплексом переходных продуктов при генезисе крайних минералов: каолинита-монтмориллонита.
Палыгорскитовые минералы – это волокнистые минералы, магнезиальные водные силикаты с формулой 2MgO·3SiO2·4 Н2О. Они имеют красноватый цвет. Частицы сепилолит-палыгорскита имеют игольчатую форму. Взаимодействие между ними происходит за счет механического сцепления, т. к. заряды на их поверхности отсутствуют. Поэтому палыгорскитовые глины используются как эффективные структурообразователи в условиях высокой минерализации. Такие глины не могут обеспечит низкие значения показателя фильтрации. Эта проблема решается за счет введения в раствор монтмориллонитовой глины, дающей в составе раствора коллоидную фракцию.
Природные глины обычно состоят из нескольких глинообразующих минералов, название которым дается по названию преобладающего по содержанию минерала. Кроме того, в глинах присутствуют и другие минералы: кварц, полевой шпат, кальцит и др.
Сырье зависит от преобладающего глинообразующего минерала, бывает следующих видов:
- бентониты (монтмориллонитовая глина);
- палыгорскиты;
- каолинит-гидрослюдистые глины;
- местные некондиционные (комовые глины).
Наиболее технологичные в применении глинопорошки, которые выпускаются в соответствии с ТУ 39-0147007-105-93, в зависимости от минерального состава глин следующих типов:
- бентонитовые (Б);
- полыгорскитовые (П);
- каолинит-гидрослюдистые (КГ).
Такие глинопорошки бывают модифицированные (М) и немодифицированные.
В качестве модифицирующих добавок используют: кальцинированную соду, полимеры и органические реагенты.
Срок хранения немодифицированных и модифицированных неорганическими реагентами не ограничен, а модифицированных органическими реагентами – 8 месяцев.
В зависимости от выхода раствора выделяют 6 групп глинопорошков: А, Б, В, Г, Д и Н.
Выход раствора – это количество м3 глинистого раствора со стандартной эффективной вязкостью mэ=20 мПа∙ с, которое можно получить из 1 т глинопорошка.
В табл. 6. 1 приведены сведения об основных типах глинопорошков.
Таблица 6. 1. Типы выпускаемых глинопорошков
| Тип глинопорошка | Марки глинопорошков | |||||
| Выход раствора с µэ=20 мПа·с из 1 т глинопорошка, м3 | ||||||
| 5(4) | Менее 5(4) | |||||
| Бентонитовый | --- | х)ПББ | ПБВ | ПБГ | ПБД | ПБН |
| Бентонитовый модифицированный | ПБМА | ПБМБ ПБМБэ ПБМБп | ПБМВ | ПБМГ | --- | --- |
| Палыгорскитовый | --- | ППБ | ППВ | ППГ | ППД | ППН |
| Палыгорскитовый модифицированный | --- | ППМБ | ППМВ | ППМГ | --- | --- |
| Каолинит-гидрослюдистый | --- | --- | --- | --- | ПКГД | ПКГН |
Х) П – первое в марке, порошок;
|
|
|
Э – для экспорта;
П – с добавкой палыгорскита.
Основные параметры, которые характеризуют качество глин:
1. Объемная концентрация глины в растворе.
Уравнение баланса масс для глинистого раствора:
mр=mв+mг, (6. 8)
или
Vр∙ ρ р= Vр∙ ρ в(1-Кг)+ Vр∙ ρ г∙ Кг, (6. 9)
где: mр, mв, mг – масса раствора, воды и глины соответственно;
Vр – объем раствора;
Кг – объемная концентрация глины в растворе;
ρ р, ρ в, ρ г – плотность раствора, воды и глины соответственно.
Преобразовав (6. 9) и решив относительно Кг, получим:
Кг=  , % (6. 10)
, % (6. 10)
2. Выход раствора.
Объем, занимаемый глиной при объемной концентрации Кг в растворе с выходом Вр:
Vг=Вр∙ Кг (6. 11)
Подставив в (6. 11) Vг=  , и Кг по формуле (6. 10), получили:
, и Кг по формуле (6. 10), получили:
 , м3 (6. 12)
, м3 (6. 12)
Выход раствора рассчитывается при mг=1 т стандартных значениях условий вязкости mэ=20 мПа∙ с и соответствующей плотности раствора ρ р.
3. Масса глины, необходимая для приготовления 1 м3 глинистого раствора. Используя уравнение (6. 12) и решив его относительно mг получили формулу для определения массы определенной марки глинопорошка для 1 м3 глинистого раствора со стандартной эффективной вязкостью mэ=20 мПа∙ с в виде и плотностью ρ ст.
 , т (6. 13)
, т (6. 13)
где: ρ ст – плотность стандартного раствора при mэ=20 мПа∙ с.
По формуле (6. 13) величина  находится при Вр=1 м3.
находится при Вр=1 м3.
4. Обменная емкость глины.
Атомы кремния и алюминия, входящие в кристаллическую решетку глинистых минералов могут быть замещены катионами из растворов, т. е. может происходить катионный обмен между структурными элементами кристаллической решетки и заряженными частицами, находящимися в растворе. Причем, этот катионный объем может проходить между заряженными частицами, имеющими неодинаковый заряд с атомами решетки. В этом случае для компенсации ненасыщенных валентностей поверхность глинистых частиц адсорбирует катионы из водных растворов. Каждый вид глин обладает определенным количеством обменных катионов, что определяется строением их кристаллической решетки, условиями формирования глинистых минералов, структурными замещениями в пределах кристаллической решетки конкретного вида глинообразующих минералов. Исходя из этого, каждый вид глины обладает определенной обменной емкостью – количеством г-ион обменных катионов, содержащихся в 1 кг сухой глины. Для различных видов глин обменная емкость (г-ион) имеет следующие значения:
монтмориллонитовая 0, 8 – 1, 5
гидрослюдистая 0, 1 – 0, 4
палыгорскитовая 0, 2 – 0, 3
каолинитовая 0, 03 – 0, 15
В глинистых минералах обменными катионами являются в основном Na+ (натриевые глины), Ca++ (кальциевые глины), а также Mg++, K+, H+, NH4+.
Гидрофильные свойства глин увеличиваются при увеличении значения обменной емкости. Однако все глины в той ли иной степени являются гидрофильными, что важно при получении глинистых растворов на водной основе.
В случае замещений на поверхности глины с помощью аммоний – катиона NH4+, происходит изменение свойств глин, и тогда она приобретает органофильные свойства, что необходимо для получения глинистых растворов на углеводородной основе. Для этих целей чаще всего используется модифицированный бентонит или аммонит – бентонит.
Дисперсионная среда промывочных жидкостей на водной основе
Вода является дисперсионной средой для таких промывочных жидкостей. Молекулы воды обычно диссоциируют на ионы H+ и OH-. произведение ионов водорода и гидроксила является постоянным [H+] [OH-] = 1·10-14 (при t = 22ОС) и называется ионным числом воды. Концентрация ионов водорода под действием определенных природных условий может меняться, но ионное число воды остается постоянным. Поскольку концентрация ионов водорода мала и выражается числом с отрицательной степенью, то ее удобно выражать десятичным логарифмом с знаком минус. Это число называют водородным показателем pH. Если вода является нейтральной, когда [H+] = 10-7 и [OH-] = 10-7, то в данном случае pH = 7. Для щелочных вод pH> 7, для кислых вод pH< 7. Величина pH оказывает большое влияние на пептизацию глинистых частиц, на поведение химических реагентов при химической обработке растворов.
В воде могут присутствовать соли карбонатов и бикарбонатов Ca++ и Mg++ или других солей этих катионов (CaSO4, CaCl2, MgSO4, MgCl2), которые придают воде жесткость. По величине жесткости воду делят на мягкую(1, 5 – 3, 0 ммоль/кг), умеренно жесткую (3, 0 – 5, 5 ммоль/кг), жесткую (5, 5 - 9) и очень жесткую (более 9, 0 – 10, 0 ммоль/кг).
Жесткость воды ухудшает свойства глинистых растворов и затрудняет их регулирование.
В воде могут присутствовать и другие соли, общее содержание которых может колебаться в различных пределах. По содержанию NaCl воды подразделяются на пресные (до 0, 1 %), минерализованные (0, 1 – 5 %) и рассолы (более 5 %).
В зависимости от качества воды выбирается вид глины и химреагентов. Пресная вода обеспечивает лучшие качества глинистых растворов и наибольший его выход. При большом содержании солей (более 5 %) бентонит ухудшает свою способность к образованию коллоидной системы воды. В этом случае лучше использовать палыгорскитовые глины.
|
|
|


