 |
Тема: Смеси идеальных газов.
|
|
|
|
I. Понятие об идеальном газе. Состояние системы.
Предыдущая лекция была посвящена вопросам методов исследования свойств тел на основе молекулярно-кинетической теории.
Используя выводы рассмотренных вопросов, разберем основные законы для газов.
Все газы делятся на два основных вида:
 |
Идеальным газом называется газ, удовлетворяющий следующим условиям:
1) размеры молекул пренебрежительно малы
2) соударения молекул происходят как соударения упругих шариков
3) между молекулами не проявляются силы взаимодействия
Пример идеального газа – сильно разряженные газы (не превышающие атмосферное в 100 раз) при не очень низких температурах.
Реальным газом называется газ, между молекулами которого существуют заметные силы межмолекулярного взаимодействия, и учитывается размер молекул.
Понятие об идеальном газе является практически удобной абстракцией. Такое понятие дало возможность построить молекулярно-кинетическую теорию, рассмотреть вопросы о вычислении теплоемкостей, явления переноса и др. В определенных границах выводы этой теории хорошо подтверждаются экспериментами.
Введем некоторые понятия, необходимые для рассмотрения вопросов лекции.
Термодинамическая система – совокупность макроскопических объектов, обменивающихся энергией в форме работы и в форме теплоты как друг с другом, так и с внешней средой. Макроскопические объекты – компоненты (число от 1 до ¥).

Состояние системы определяется, как уже говорилось совокупностью её термодинамических параметров (параметров состояния).
 |
Время перехода системы из неравновесного состояния в равновесное называется временем релаксации.
|
|
|
Термодинамическим процессом (процессом) называется всякое изменение состояния системы.
II. Процессы.
 
| 1) Равновесный, при котором система проходит непрерывный ряд равновесных состояний: Этот процесс бесконечно медленный |
| 2) Обратимый, при котором возможно осуществить обратный переход через те же промежуточные состояния так, чтобы не осталось никаких изменений в окружающих телах. Пример: колебания тяжелого маятника. Необратимый, при котором в теле или в окружающих телах есть изменения. Примеры: передача тепла от более нагретого тела к менее нагретому; любой процесс с трением. | |

| 3) Круговой (цикл), в результате совершения которого система возвращается в исходное состояние. |
4) Адиабатный, осуществляемый системой без теплообмена с внешней средой.
5) Политропный, при котором идеальная теплоемкость газа постоянна (общий процесс, его частными случаями являются адиабатный и все изопроцессы).
 6) Изопроцессы, протекающие при неизменном значении какого-либо параметра состояния при m = const.
6) Изопроцессы, протекающие при неизменном значении какого-либо параметра состояния при m = const.
III. Основные газовые законы.
Из основного уравнения кинетической теории газов можно вывести все газовые законы, ранее установленные экспериментально. Для вывода каждого закона используем конкретную формулу основного уравнения.
| а) Закон Бойля-Мариотта (изотермический процесс) | |

|  , т.к. , т.к.  , получим основное уравнение: , получим основное уравнение:
 , (из уравнения (8) лекции 7),
где N – число молекул в единице объема
m – масса газа , (из уравнения (8) лекции 7),
где N – число молекул в единице объема
m – масса газа
 – средняя квадратичная скорость молекул – средняя квадратичная скорость молекул
 при t = const и m = const, следовательно, правая часть const, т.е.
PV = const (1) при t = const и m = const, следовательно, правая часть const, т.е.
PV = const (1)
|
| б) закон Гей-Люссака (изобарический процесс) | |

|  (*) (*)
 (**)
поделив (*) на (**), получим: (**)
поделив (*) на (**), получим:  (2)
или Vt = V0(1+ αt0), где
Vt – температура при t0C;
V0 – температура при 00С; (2)
или Vt = V0(1+ αt0), где
Vt – температура при t0C;
V0 – температура при 00С;
 – температурный коэффициент – температурный коэффициент
|
в) Закон Шарля (изохорический процесс)
Получается аналогичным рассуждением:
 (3)
(3)
или Pt = Р0(1 + αt0)
|
|
|
г) Объединенный газовый закон


 (4)
(4)
Во всех выше рассмотренных законах масса газа считается постоянной.
Для примера приведем графики различных процессов в разных системах координат:
 |
IV. Уравнение состояния идеальных газов и газовая постоянная.
Уравнением состояния газа называется уравнение, связывающее основные параметры, характеризующие состояние газа.
Согласно объединенному газовому закону
 ,
,
где С – газовая постоянная.
С зависит от массы, химического состава и выбора единиц измерения P, V, T.
 – называется удельная газовая постоянная.
– называется удельная газовая постоянная.
Получим уравнение, выведенное Клапейроном в 1834г. для произвольной массы газа:
PV=mBT (5)
B для системы СИ:  ,
,
где ρ – плотность газа.
Однако гораздо удобнее пользоваться уравнением состояния в универсальном виде, что и было сделано Менделеевым в 1874г.

 – уравнение Менделеева-Клапейрона, (6)
– уравнение Менделеева-Клапейрона, (6)
где μ – масса киломоля газа;
R – универсальная газовая постоянная.
R = 8,32∙103 Дж/Кмоль∙К
или R = 8,32 ДЖ/моль∙К
 – число молей.
– число молей.

| Выясним физический смысл универсальной газовой постоянной. В цилиндре заключен 1 моль газа. Нагреваем газ на 10 при Р = const. Вычислим работу расширения газа. A = F(ℓ1– ℓ) = ps(ℓ1– ℓ)= pV1–pV = R(T + 1) – RT = R A = R (7) |
Физический смысл R: R численно равна работе при изобарическом расширении 1 моля газа при нагревании его на 1 градус.
Уравнение Менделеева-Клапейрона широко используется для решения многих практических задач (вплоть до давлений, немного превышающих атмосферное и не очень низких температурах).
V. Смесь газов. Закон Дальтона.
Все зависимости, полученные выше для идеальных газов, справедливы и для их смесей, если в них подставлять газовую постоянную, молекулярную массу и теплоемкость смеси.
Закон Дальтона. В инженерной практике часто приходится иметь дело с газообразными веществами, близкими по свойствам к идеальным газам и представляющими собой механическую смесь отдельных компонентов различных газов, химически не реагирующих между собой. Это так называемые газовые смеси. В качестве примера можно назвать продукты сгорания топлива в двигателях внутреннего сгорания, топках печей и паровых котлов, влажный воздух в сушильных установках и т. п.
|
|
|
Основным законом, определяющим поведение газовой смеси, является закон Дальтона: полное давление смеси идеальных газов равно сумме парциальных давлений всех входящих в нее компонентов:

Парциальное давление pi — давление, которое имел бы газ, если бы он один при той же температуре занимал весь объем смеси.
Способы задания смеси. Состав газовой смеси может быть задан массовыми, объемными или мольными долями.
Массовой долей называется отношение массы отдельного компонента Мi, к массе смеси М:
 .
.
Очевидно, что 
 и
и  .
.
Массовые доли часто задаются в процентах. Например, для сухого воздуха  ;
;  .
.
Объемная доля представляет собой отношение приведенного объема газа V, к полному объему смеси V:  .
.
Приведенным называется объем, который занимал бы компонент газа, если бы его давление и температура равнялись давлению и температуре смеси.
Для вычисления приведенного объема запишем два уравнения состояния i -го компонента:
 ; (2.1)
; (2.1)
 .
.
Первое уравнение относится к состоянию компонента газа в Смеси, когда он имеет парциальное давление pi и занимает полный объем смеси, а второе уравнение — к приведенному состоянию, когда давление и температура компонента равны, как и для смеси, р и Т. Из уравнений следует, что
 . (2.2)
. (2.2)
Просуммировав соотношение (2.2) для всех компонентов смеси, получим с учетом закона Дальтона  ,откуда
,откуда  . Объемные доли также часто задаются в процентах. Для воздуха
. Объемные доли также часто задаются в процентах. Для воздуха  ,
,  .
.
Иногда бывает удобнее задать состав смеси мольными долями. Мольной долей называется отношение количества молей Ni рассматриваемого компонента к общему количеству молей смеси N.
Пусть газовая смесь состоит из N1 молей первого компонента, N2 молей второго компонента и т. д. Число молей смеси  , а мольная доля компонента будет равна
, а мольная доля компонента будет равна  .
.
В соответствии с законом Авогадро объемы моля любого газа при одинаковых р и Т, в частности при температуре и давлении смеси, в идеально газовом состоянии одинаковы. Поэтому приведенный объем любого компонента может быть вычислен как произведение объема моля  на число молей этого компонента, т. е.
на число молей этого компонента, т. е.  а объем смеси — по формуле
а объем смеси — по формуле  . Тогда
. Тогда  , и, следовательно, задание смесильных газов мольными долями равно заданию ее объемными долями.
, и, следовательно, задание смесильных газов мольными долями равно заданию ее объемными долями.
|
|
|
Газовая постоянная смеси газов. Просуммировавуравнения (2.1) для всех компонентов смеси, получим  . Учитывая
. Учитывая  , можно записать
, можно записать
 , (2.3)
, (2.3)
где
 . (2.4)
. (2.4)
Из уравнения (2.3) следует, что смесь идеальных газов также подчиняется уравнению Клапейрона. Поскольку  то из (2.4) следует, что газовая постоянная смеси [Дж/(кг-К)] имеет вид
то из (2.4) следует, что газовая постоянная смеси [Дж/(кг-К)] имеет вид
 (2.5)
(2.5)
Кажущаяся молекулярная масса смеси. Выразим формально газовую постоянную смеси R, введя кажущуюся окулярную массу смеси  :
:  (2.6)
(2.6)
Сравнивая правые части соотношений (2.5) и (2.6), найдем
 .
.
Изопределения массовых долей следует, что
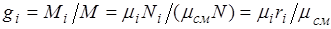
Просуммировав это соотношение для всех компонентов и учитывая, что  , получим выражение для кажущейся молекулярной и массы смеси, заданной объемными долями:
, получим выражение для кажущейся молекулярной и массы смеси, заданной объемными долями:
 . (2.7)
. (2.7)
Соотношение между объемными и массовыми долями. Учитывая (2.7), получаем  .
.
Поскольку  , то
, то

Разделив числитель и знаменатель этой формулы на массу смеси М, получим
 .
.
Аналитическое выражение первого закона термодинамики
Первый закон термодинамики представляет собой частный случай всеобщего закона сохранения и превращения энергии применительно к тепловым явлениям. В соответствии с уравнением Эйнштейна  надо рассматривать единый закон сохранения и превращения массы и энергии. Однако в технической термодинамике мы имеем дело со столь малыми скоростями объекта, что дефект массы равен нулю, и поэтому закон сохранения энергии можно рассматривать независимо.
надо рассматривать единый закон сохранения и превращения массы и энергии. Однако в технической термодинамике мы имеем дело со столь малыми скоростями объекта, что дефект массы равен нулю, и поэтому закон сохранения энергии можно рассматривать независимо.
Закон сохранения и превращения энергии является фундаментальным законом природы, который получен на основе обобщения огромного количества экспериментальных данных и применим ко всем явлениям природы. Он утверждает, что энергия не исчезает и не возникает вновь, она лишь переходит из одной формы в другую, причем убыль энергии одного вида дает эквивалентное количество энергии другого вида.
В числе первых ученых, утверждавших принцип сохранения материи и энергии, был наш соотечественник М. В. Ломоносов (1711 — 1765 гг.).
Пусть некоторому рабочему телу с объемом V и массой М, имеющему температуру Т и давление р, сообщается извне бесконечно малое количество теплоты  . В результате подвода теплоты тело нагревается на dT и увеличивается в объеме на dV.
. В результате подвода теплоты тело нагревается на dT и увеличивается в объеме на dV.
Повышение температуры тела свидетельствует об увеличении кинетической энергии его частиц. Увеличение объема тела приводит к изменению потенциальной энергии частиц. В результате внутренняя энергия тела увеличивается на dU. Поскольку рабочее тело окружено средой, которая оказывает на него давление, то при расширении оно производит механическую работу  против сил внешнего давления. Так как никаких других изменений в системе не происходит, то по закону сохранения энергии
против сил внешнего давления. Так как никаких других изменений в системе не происходит, то по закону сохранения энергии
|
|
|
 (2.8)
(2.8)
т. е. теплота, сообщаемая системе, идет на приращение ее внутренней энергии и на совершение внешней работы.
Полученное уравнение является математическим выражением первого закона термодинамики. Каждый из трех членов этого соотношения может быть положительным, отрицательным или равным нулю. Рассмотрим некоторые частные случаи.
1.  — теплообмен системы с окружающей средой отсутствует, т. е. теплота к системе не подводится и от нее не отводится. Процесс без теплообмена называется адиабатным. Для него уравнение (2.8) принимает вид:
— теплообмен системы с окружающей средой отсутствует, т. е. теплота к системе не подводится и от нее не отводится. Процесс без теплообмена называется адиабатным. Для него уравнение (2.8) принимает вид:
 .
.
Следовательно, работа расширения, совершаемая системой в адиабатном процессе, равна уменьшению внутренней энергии данной системы. При адиабатном сжатии рабочего тела затрачиваемая извне работа целиком идет на увеличение внутренней энергии системы.
2.  — при этом объем тела не изменяется, dV =0. Такой процесс называется изохорным, для него
— при этом объем тела не изменяется, dV =0. Такой процесс называется изохорным, для него
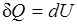 ,
,
т. е. количество теплоты, подведенное к системе при постоянном объеме, равно увеличению внутренней энергии данной системы.
3. dU=0 – внутренняя энергия системы не изменяется и
 ,
,
т.е. сообщаемая системе теплота превращается в эквивалентную ей внешнюю работу.
Для системы, содержащей 1 кг рабочего тела
 . (2.9)
. (2.9)
Проинтегрировав уравнения (2.8) и (2.9) для некоторого процесса, получим выражение первого закона термодинамики в интегральной форме:
 ;
;  .
.
|
|
|


