 |
Расчет дозы препарата железа
|
|
|
|
В России лечение ЖДА определяется протоколом, утвержденным Минздравсоцразвития России 22 октября 2004 г., – «Протокол ведения больных. Железодефицитная анемия» [1]. Создание этого протокола группой ведущих специалистов нашей страны явилось значительным движением вперед, поскольку «вооружило» врачей единым пониманием проблемы дефицита железа, критериями его диагностики, принципами лечения и наблюдения больных ЖДА, оценки качества их жизни.
С точки зрения врача-педиатра лечение ЖДА у детей имеет некоторые особенности, которые следует учитывать в лечебном протоколе. Прежде всего, применение у детей в возрасте до 3 лет солевых препаратов двухвалентного железа в дозе 5–8 мг/кг массы тела в сутки, как это рекомендовано в «Протоколе», вызывает проявления токсичности у многих больных и не оправдано с терапевтической точки зрения.
При расчете доз солевых препаратов железа следует использовать рекомендации ВОЗ [2, 3] (табл. 3). Аналогичная доза солевых препаратов железа (3 мг/кг массы тела в сутки) для детей в возрасте до 3 лет указана и в пособии для врачей, утвержденном Департаментом здравоохранения Москвы в 2004 г. [4].
Таблица 3. Возрастные дозы пероральных солевых препаратов железа для лечения ЖДА (рекомендации ВОЗ, 1998; цит. по [2])
| Возраст | Суточная доза элементарного железа |
| До 3 лет | 3 мг/кг |
| Старше 3 лет | 45–60 мг |
| Подростки | До 120 мг |
Различный возраст детей (от периода новорожденности до старшего подросткового возраста) и, соответственно, различная масса тела (3,2–70 кг и более), делают необходимым индивидуальный расчет дозы препарата железа для каждого ребенка.
В «Протоколе» дозу препарата на основе гидроксид полимальтозного комплекса (ГПК) трехвалентного железа рекомендуют рассчитывать, ориентируясь на возраст детей, а не на массу их тела. Мы считаем, что в детской практике доза препаратов железа (III) на основе ГПК должна составлять 5 мг/кг массы тела в сутки независимо от возраста, именно эта доза рекомендована в упомянутом выше пособии для врачей [4].
|
|
|
Литература
1. Протокол ведения больных. Железодефицитная анемия. – М.: Ньюдиамед, 2005. – 76 с.
2. WHO, UNICEF, UNU. IDA: prevention, assessment and control: report of joint WHO/UNICEF/UNU consultation. Geneva, WHO; 1998.
3. UNICEF, United Nations University, WHO. Iron deficiency anemia: assessment, prevention and control. A guide for programme managers. – Geneva: World Health Organization, 2001 (WHO/NHD/01.3). – 114 p. – Режим доступа: http://www.who.int/nutrition/publications/micronutrients/anaemia_iron_deficiency/WHO_NHD_01.3/en.
4. Румянцев А.Г., Коровина Н.А., Чернов В.М. и др. Диагностика и лечение железодефицитной анемии у детей: Метод. пособие для врачей. – М., 2004. – 45 c.
5.2. Терапевтический план лечения ЖДА у детей
В российской педиатрической практике многие годы был принят так называемый «трапециевидный» терапевтический план лечения ЖДА у детей. В соответствии с этим планом в первые 3–5 дней дозу солевых препаратов железа постепенно повышали, чтобы не вызвать у больного раздражения слизистой оболочки ЖКТ. Полную (100%) дозу солевого препарата железа применяли в течение 1,5–3 мес. в зависимости от степени тяжести анемии с последующим ее снижением до 50% к окончанию лечения. Этот план, как и большинство других, был разработан эмпирическим путем, и его эффективность никогда не была подтверждена рандомизированными исследованиями.
Появление препаратов железа (III) на основе ГПК заставило пересмотреть план лечения ЖДА.
Под руководством сотрудников Федерального научно-клинического центра детской гематологии, онкологии и иммунологии (ФНКЦ ДГОИ) Минздрава России было проведено рандомизированное исследование по сравнению эффективности двух планов лечения ЖДА различной степени тяжести у детей и подростков: традиционного «трапециевидного» и нового, предусматривающего прием 100% дозы препарата железа (III) на основе ГПК в течение всего периода лечения. Во время исследования оценивали переносимость препарата на основе ГПК и эффективность терапии в ранние (ретикулоцитарная реакция, прирост концентрации Hb) и поздние сроки (нормализация концентрации Hb, СЖ и СФ). Была доказана эффективность терапии у детей и подростков с ЖДА препаратом железа (III) на основе ГПК. После завершения курса лечения нормализация концентрации Hb была достигнута у 96,9% пациентов, СЖ – у 73,4%, СФ – у 60,9% пациентов. Незначительное количество (6,3%) нежелательных явлений (запор в течение 1-го месяца лечения) и 100% приверженность пациентов к лечению позволили заключить, что препарат железа (III) на основе ГПК является оптимальным препаратом для терапии ЖДА у детей и подростков [1‒3].
|
|
|
Также было доказано преимущество использования 100% дозы препарата железа (III) на основе ГПК в течение всего курса лечения: нормализация концентрации СЖ была зафиксирована у 90,6%, СФ – у 75% детей и подростков. При использовании традиционного «трапециевидного» плана лечения аналогичные показатели составили 56,3 и 46,9% соответственно [1‒3].
Литература
1. Ожегов Е.А., Тарасова И.С., Ожегов А.М. и др. Сравнительная эффективность двух терапевтических планов лечения железодефицитной анемии у детей и подростков. Вопросы гематологии/онкологии и иммунопатологии в педиатрии 2005; 4(1): 14–9.
2. Ожегов Е.А. Оптимизация лечения железодефицитной анемии у детей и подростков. Автореф. дис. … канд. мед. наук. – М., 2005. – 23 с.
3. Тарасова И.С., Чернов В.М. Факторы, определяющие эффективность лечения детей с железодефицитной анемией. Вопросы практической педиатрии 2011; 3(6): 49–52.
Препараты для лечения ЖДА
Препараты железа для лечения ЖДА могут быть условно разделены на ионные солевые (преимущественно двухвалентные) и препараты железа (III) на основе ГПК. Рандомизированные исследования последних лет доказали, что эффективность солевых препаратов железа и препаратов железа (III) на основе ГПК в лечении ЖДА одинакова [1].
В процессе лечения ЖДА солевыми препаратами железа могут возникать следующие проблемы:
|
|
|
· передозировка и даже отравление вследствие неконтролируемого организмом всасывания;
· взаимодействие с другими лекарственными препаратами и пищей;
· выраженный металлический привкус;
· окрашивание эмали зубов и десен, иногда стойкое;
· частый отказ пациентов от лечения (до 30–35% приступивших к лечению), т.е. низкая комплаентность.
Большинства перечисленных проблем можно избежать при использовании препаратов железа на основе ГПК железа (III), имеющего следующие свойства и преимущества:
· высокая безопасность, отсутствие риска передозировки, интоксикации и отравлений;
· отсутствие потемнения десен и зубов;
· приятный вкус;
· отличная переносимость;
· высокая комплаентность лечения;
· отсутствие взаимодействия с другими лекарственными средствами и продуктами питания;
· наличие антиоксидантных свойств.
Применение солевых препаратов железа может сопровождаться токсичностью и развитием таких нежелательных явлений таких, как боли в эпигастральной области, запор, понос, тошнота, рвота. Это приводит к низкой комплаентности лечения ЖДА солевыми препаратами железа. Возможны передозировка и даже отравления солевыми препаратами железа из-за пассивного неконтролируемого всасывания. Современные препараты железа на основе ГПК железа (III) не вызывают таких осложнений и прекрасно переносятся.
Основные пероральные препараты железа, применяемые в лечении ЖДА, и содержание в них элементарного железа приведены в табл. 4.
Таблица 4. Основные пероральные препараты, применяемые для лечения ЖДА, и содержание в них элементарного железа
| Препарат | Состав препарата (в 1 драже, 1 таблетке, в 1 мл капель или сиропа) | Форма выпуска | Содержание элементарного железа |
| Актиферрин | Сульфат железа 113,85 мг, D, L-серин 129 мг в 1 капсуле | Капсулы, в блистере 10 капсул, по 2 и 5 блистеров упаковке | Fe2+: 34,5 мг в 1 капсуле |
| Актиферрин | Сульфат железа 47,2 мг, D, L-серин 35,6 мг, глюкоза и фруктоза 151,8 мг, калия сорбат 1 мг в 1 мл капель | Капли для приема внутрь, 30 мл во флаконе | Fe2+: 9,48 мг в 1 мл |
| Актиферрин | Сульфат железа 171 мг, D, L-серин 129 мг, глюкоза, фруктоза в 5 мл сиропа | Сироп, 100 мл во флаконе | Fe2+: 34 мг в 5 мл |
| Сорбифер Дурулес | Сульфат железа 320 мг, аскорбиновая кислота 60 мг | Таблетки, покрытые оболочкой, по 30 и 50 таблеток во флаконе | Fe2+: 100 мг в 1 таблетке |
| Мальтофер | ГПК | Капли, 10 или 30 мл во флаконе | Fe3+: 50 мг в 1 мл раствора (20 капель, 1 капля – 2,5 мг железа) |
| Мальтофер-Фол | ГПК, фолиевая кислота 0,35 мг в 1 таблетке | Жевательные таблетки, 10 таблеток в блистере, по 3 блистера в упаковке | Fe3+: 100 мг в 1 таблетке |
| Мальтофер | ГПК | Жевательные таблетки, в блистере 10 таблеток, по 3 и 50 блистеров в упаковке | Fe3+: 100 мг в 1 таблетке |
| Мальтофер | ГПК | Сироп, 150 мл во флаконе | Fe3+: 10 мг в 1 мл |
| Тардиферон | Сульфат железа 256,3 мг, мукопротеоза 80 мг, аскорбиновая кислота 30 мг | Таблетки, покрытые оболочкой, 10 таблеток в блистере, 3 блистера в упаковке | Fe2+: 80 мг |
| Тотема | В 10 мл раствора содержится: 50 мг глюконата железа, 1,33 мг глюконата марганца, 0,7 мг глюконата меди, глицерол, глюкоза, сахароза, лимонная кислота, цитрат натрия и др. | Раствор для приема внутрь, ампулы по 10 мл, по 20 шт. в упаковке | Fe2+: 5 мг в 1 мл |
| Ферретаб комп. | Фумарат железа 154 мг, фолиевая кислота 0,5 мг | Капсулы, 10 капсул в блистере, 3 блистера в упаковке | Fe2+: 50 мг в 1 капсуле |
| Ферроплекс | Сульфат железа 50 мг, аскорбиновая кислота 30 мг | Драже, в упаковке 100 шт. | Fe2+: 10 мг в 1 драже |
| Ферронал | Глюконат железа 300 мг в 1 таблетке | Таблетки, покрытые оболочкой, в блистере 10 таблеток, 1 блистер в упаковке | Fe2+: 30 мг в таблетке |
| Ферлатум | Протеин сукцинилат железа 800 мг в 15 мл | Раствор для приема внутрь, 15 мл во флаконе, 10 флаконов в упаковке | Fe2+: 40 мг в 15 мл |
| Фенюльс | Сульфат железа 150 мг, аскорбиновая кислота 50 мг, рибофлавин 2 мг, тиамин 2 мг, никотинамид 15 мг, пиридоксин гидрохлорид 1 мг, пантотеновая кислота 2,5 мг | Капсулы, 10 капсул в блистере, 1 блистер в упаковке | Fe2+: 45 мг в 1 капсуле |
| Феррум Лек | ГПК | Жевательные таблетки, 10 таблеток в стрипе, 3 стрипа в упаковке | Fe3+: 100 мг в 1 таблетке |
| Феррум Лек | ГПК | Сироп, 100 мл во флаконе | Fe3+: 10 мг в 1 мл |
| Хеферол | Фумарат железа 350 мг в 1 капсуле | Капсулы, во флаконе 30 шт. | Fe2+: 115 мг в капсуле |
Парентеральные (внутривенные и внутримышечные) препараты железа (табл. 5) показаны в тех случаях, когда есть противопоказания к применению пероральных препаратов или они неэффективны. Парентеральные препараты железа в лечении ЖДА показаны при:
|
|
|
· тяжелой форме ЖДА (в настоящее время встречается довольно редко, менее чем в 3% случаев);
· непереносимости пероральных препаратов железа;
· резистентности к лечению пероральными препаратами железа;
· наличии язвенной болезни желудка или двенадцатиперстной кишки или операций на ЖКТ, даже в анамнезе;
|
|
|
· анемии, ассоциированной с хроническими болезнями кишечника (язвенный колит, болезнь Крона);
· хронической болезни почек для лечения и профилактики анемии в преддиализный и диализный периоды;
· наличии противопоказаний к переливанию эритроцитной массы, в том числе по религиозным убеждениям (например, свидетели Иеговы);
· необходимости быстрого насыщения организма железом.
Внутримышечные или внутривенные инъекции препарата железа обычно проводят 1–3 раза в неделю. При использовании парентеральных препаратов железа не рекомендуется превышать общий дефицит железа, который предварительно рассчитывают по формуле:
| Общий дефицит железа, мг |
| Масса тела больного, кг кг |
| = |
| ´ |
| Hb Hb (норма), больного, г/л г/л |
| Депо железа, мг (1) мг |
| 0,24 + |
| ´ |
Коэффициент 0,24 = 0,0034 ´ 0,07 ´ 1000:
‒ содержание железа в Hb ‒ приблизительно 0,34%;
‒ объем крови ‒ 7% массы тела;
‒ 1000 ― перевод граммов в миллиграммы.
Депо железа у пациентов с массой тела:
‒ менее 35 кг‒ 15 мг/кг, целевая концентрация Hb ‒ 130 г/л;
‒ более 35 кг‒ 500 мг, целевая концентрация Hb ‒ 150 г/л.
Особенностью данной формулы является учет железа в депо, составляющего значимую (более 30%) часть общего количества железа. Снижение запасов железа в депо может быть доказано по снижению концентрации СФ.
Зная общий дефицит железа в организме (в мг) и количество железа в 1 ампуле препарата (например, 100 мг), можно рассчитать необходимое количество ампул на курс лечения по формуле:
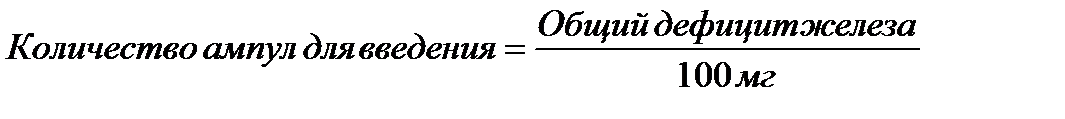 (2)
(2)
Возможны нежелательные явления при использовании парентеральных препаратов железа. Оба способа введения (внутривенный и внутримышечный) могут вызвать различные нежелательные явления – местные (покраснение, жжение, зуд) и общие (аллергические, анафилактоидные). Последние характерны для парентеральных препаратов железа, содержащих декстран. Это требует наблюдения больного, применения тест-дозы перед началом лечения, точного расчета количества железа, которое следует ввести во избежание повреждающего действия его повышенной концентрации в циркуляции. Необходимо иметь в виду возможность возникновения нежелательных явлений, обусловленных гиперчувствительностью пациента к препаратам железа, вводимым даже в очень низких дозах.
Для того чтобы терапия парентеральными препаратами железа была эффективной и безопасной для пациента необходимо строгое выполнение следующих принципов лечения:
· применение современных парентеральных препаратов железа с меньшей токсичностью, без анафилактоидных реакций, опасных для жизни больного;
· определение общего дефицита железа в организме больного по формуле 1;
· прекращение терапии после восполнения общего дефицита железа во избежание опасного перенасыщения организма железом. По этим же соображениям желательно проводить терапию парентеральными препаратами железа под контролем НТЖ;
· соблюдение техники проведения внутримышечной инъекции и внутривенной инфузии препаратов железа;
· обязательное выполнение требования инструкции по применению парентерального препарата железа, если предусмотрено введение пробной дозы перед началом лечения;
· лечение рекомендуется проводить в диапазоне безопасных доз, так как нежелательные явления парентеральных препаратов железа являются дозозависимыми.
Таблица 5. Некоторые современные препараты железа для парентерального введения
| Название препарата | Состав препарата | Количество препарата в ампуле |
| Для внутримышечного введения | ||
| Жектофер | Железо (III)-сорбитол-цитрат | 100 мг в 2 мл |
| КосмоФер | Железо (III)-гидроксид декстран (низкомолекулярный) | 100 мг в 2 мл |
| Мальтофер – раствор для инъекций | Гидроксид железа (III) с полимальтозой | 100 мг в 2 мл |
| Спейсферрон | Водный раствор низкомолекулярного декстрана с микроэлементами – железом и кобальтом | 100 мг в 5 мл |
| Фербитол | Железо (III)-сорбитол | 100 мг в 2 мл |
| Феркайл | Железо (III)-декстран | 100 мг в 2 мл |
| Ферростат | Железо (III)-гидроксид сорбитоловый комплекс | 100 мг в 2 мл |
| Феррум Лек – раствор для инъекций | Гидроксид железа (III) с полиизомальтозой в водном изотоническом растворе | 100 мг в 2 мл |
| Для внутривенного введения | ||
| Аргеферр* | Железо (III)-гидроксид сахарозный комплекс | 100 мг в 5 мл |
| Венофер† | Железо (III)-гидроксид сахарозный комплекс | 100 мг в 5 мл 40 мг в 2 мл |
| КосмоФер* | Железо (III)-гидроксид декстран (низкомолекулярный) | 100 мг в 2 мл |
| Ликферр100* | Железо (III)-гидроксид сахарозный комплекс | 100 мг в 5 мл |
| Феринжект‡ | Железо (III)-карбоксимальтозат | 500 мг в 10 мл 100 мг в 2 мл |
* Противопоказан или назначается с осторожностью детям до 18 лет в связи с недостаточностью данных об эффективности и безопасности.
† У детей с 3-летнего возраста не более 3 мг на 1 кг массы тела.
‡ Противопоказан детям до 14 лет.
Литература
1. Toblli J.E., Brignoli R. Iron (III)-hydroxide polymaltose complex in iron deficiency anemia: review and meta-analysis. Arzneimittelforschung 2007; 57(6A): 431–438.
|
|
|


