 |
Основные рекомендации по ведению больных лимфоаденопатией
|
|
|
|
Ситуационный подход к больным с лимфаденопатиями
| Ситуация | Тактика ведения |
| Наличие ранее диагностированного заболевания, проявляющегося лимфаденопатией | Лечение основного заболевания, динамика лимфаденопатии |
| Наличие очевидной инфекции, позволяющей объяснить наличие лимфаденопатии | Лечение инфекции, динамика лимфаденопатии |
| Наличие ЛУ больших размеров и плотной консистенции, позволяющих предполагать опухолевый процесс | Биопсия ЛУ |
| Сильная обеспокоенность больного о возможности злокачественности и невозможность разубедить его в этом | Биопсия ЛУ |
| Отсутствие изменений в периферической крови | Наблюдение в течение 2–4 нед При отсутствии регресса или увеличении размеров ЛУ – биопсия ЛУ |
Основные рекомендации по ведению больных лимфоаденопатией
| •Выявление дополнительных признаков при первичном осмотре больных •Обязательное исследование периферической крови при первичном обращении больного •Диагностический поиск с учетом выявленных дополнительных признаков •Наблюдение за больными в течение 2–4 нед при "остром" увеличении ЛУ •Назначение антибиотиков только в случаях доказанной бактериальной инфекции •Нецелесообразность назначения глюкокортикоидов при неясных лимфаденопатиях •Строгие показания к биопсии ЛУ (плотные, безболезненные ЛУ размером более 2 см2, надключичная локализация, возраст старше 40 лет) |
Анамнестические сведения (травма конечностей, путешествия, контакт с некоторыми больными и т.д.) позволяют определить направление диагностического поиска, а в ряде случаев могут приобретать решающее значение при дифференциальной диагностике лимфаденопатий (наличие у больного заболевания, проявляющегося увеличением ЛУ, прием некоторых медикаментов).
При первичном осмотре больного с увеличением ЛУ врач выявляет различную локализацию и распространенность лимфаденопатии. Локализация увеличенных ЛУ позволяет заподозрить определенный круг заболеваний с целью проведения дальнейшего целенаправленного исследования. Так, затылочные ЛУ обычно увеличиваются при инфекциях волосистой части головы, а околоушные ЛУ – при инфекционных конъюнктивитах. Часто выявляемое местное увеличение шейных ЛУ является следствием инфекций верхних дыхательных путей, носоглотки, инфекционного мононуклеоза, однако при этом необходимо также исключать как лимфопролиферативные опухоли (лимфогранулематоз), так и метастазы в ЛУ опухолей различной локализации (голова и шея, легкие, молочная и щитовидная железы). В то же время увеличение надключичных и предлестничных ЛУ практически никогда не бывает реактивным, а чаще связано с лимфопролиферативными опухолями (лимфогранулематоз), метастатическим опухолевым процессом (опухоли желудка, яичников, легких, молочных желез). В зависимости от распространенности следует различать следующие варианты лимфаденопатий:
• локальная лимфаденопатия – увеличение одного ЛУ в одной из областей (единичные шейные, надключичные ЛУ);
• регионарная лимфаденопатия – увеличение нескольких ЛУ одной или двух смежных областей (надключичные и подмышечные, надключичные и шейные, затылочные и подчелюстные ЛУ и т.д.);
• генерализованная лимфаденопатия – увеличение ЛУ более трех областей (шейные, надключичные, подмышечные, паховые и др.).
При всей относительности такого разделения распространенность лимфаденопатии может иметь значение при выдвижении предварительной диагностической гипотезы после первичного осмотра больного. Увеличение одного ЛУ чаще требует исключения первичного или метастатического опухолевого процесса или является реактивным в ответ на местный инфекционно-воспалительный процесс в соответствующей области (реактивный паховый лимфаденит при генитальных инфекциях, увеличение подчелюстных ЛУ при остром тонзиллите и т. д.). Регионарная лимфаденопатия с преимущественным увеличением затылочных и заднешейных ЛУ более характерна для инфекционного мононуклеоза. Генерализованная лимфаденопатия обычно выявляется при заболеваниях различной природы, в частности инфекционных (вирусные инфекции, токсоплазмоз), системных (системная красная волчанка), лимфопролиферативных опухолях (хронический лимфолейкоз).
Наряду с распространенностью лимфаденопатии необходимо учитывать размеры и консистенции ЛУ, что не является определяющими признаками, однако может служить обоснованием при выдвижении предварительной диагностической гипотезы. Если размеры ЛУ не превышают 1 см2, то скорее всего речь идет о реактивной лимфаденопатии. У больных с увеличенными ЛУ размером более 2 см2 чаще следует подозревать опухолевый или гранулематозный процесс. В случаях увеличения ЛУ, не превышающего 1,5 см2, и при отсутствии явных признаков инфекции необходимо дальнейшее наблюдение за больными.
Консистенция ЛУ (мягкая, плотная, эластичная), их подвижность и болезненность также могут быть диагностическими ориентирами в процессе дифференциальной диагностики. Плотные ЛУ обычно характерны для метастазов опухолей. Болезненность ЛУ при пальпации обусловлена быстрым растяжением капсулы и свидетельствует обычно о воспалительном процессе (инфекционном или реактивном), хотя при некоторых опухолевых заболеваниях (в частности, при острых лейкозах) может также определяться болезненность ЛУ.
Наличие дополнительных клинических признаков у больного лимфаденопатией является важным при определении направления диагностического поиска. В связи с этим необходимо тщательное клиническое исследование пациента с целью выявления различных дополнительных симптомов (увеличение печени, селезенки, суставной синдром, кожные высыпания, узлы, царапины, легочная симптоматика, ЛОР-осмотр и др.). Выявление увеличенной селезенки у больного лимфаденопатией более характерно для вирусных инфекций (инфекционный мононуклеоз), острого и хронического лимфолейкоза, системных заболеваний (системная красная волчанка, болезнь Стилла у взрослых).
Лимфаденопатия инфекционного происхождения может быть обусловлена непосредственным инфекционным пораженим ЛУ с внедрением инфекционного агента гематогенным или лимфогенным путем в ткань ЛУ (туберкулез, актиномикоз, гнойные лимфадениты, вирусные инфекции) или реактивным воспалением в ответ на инфекционный очаг в данной области (подмышечный лимфаденит при панариции, паховый лимфаденит при рожистом воспалении нижней конечности или генитальной инфекции, подчелюстной лимфаденит при ротоглоточной инфекции и т. д.). Четкое разграничение этих двух форм в известной степени условно и связано с уровнем диагностического обследования (морфологический, иммунологический с использованием полимеразной цепной реакции). При одной и той же инфекции лимфаденопатия может носить как инфекционный, так и реактивный характер (первичный туберкулезный аффект, туберкулез ЛУ).
Далее представлены алгоритмы диагностического поиска при локальных (регионарных) и генерализованных лимфаденопатиях (рис. 2, 3).
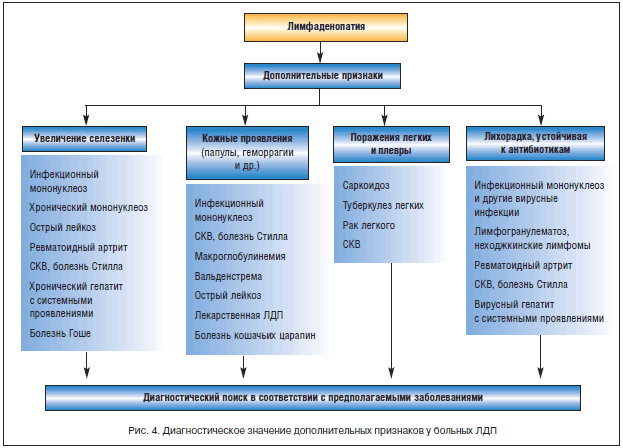
На рис. 4 представлено диагностическое значение дополнительных клинических признаков, выявляемых при первичном осмотре больных лимфаденопатией.
В табл. 1 приводятся вероятные изменения показателей периферической крови, которые могут быть выявлены у больных с наличием лимфаденопатии, и возможные заболевания.
В табл. 2 представлена дифференциальная диагностика лимфопролиферативных опухолей.
|
|
|
|
|
|
|
|
|
Портал Consilium Medicum:
http://con-med.ru/magazines/physician/physician-02-2005/differentsialnyy_diagnoz_pri_limfadenopatiyakh/?¤t_fieldset=SOCSERV




Актуальной и достаточно сложной дифференциально-диагностической проблемой для врачей различных специальностей является лимфаденопатия (ЛА, lymphadenopathia) – состояние, проявляющееся увеличением лимфатических узлов (ЛУ). В клинической практике термин «лимфаденопатия», как правило, выступает или в качестве предварительного диагноза, или ведущего синдрома заболеваний различной этиологии. К сожалению, ЛА не всегда уделяется достаточно серьезное внимание, несмотря на то что она часто может быть клиническим проявлением серьезных и даже фатальных нозологий. В связи с этим в рамках данной публикации мы хотим остановиться на подходах к диагностике данного синдрома.
|
|
|
В организме человека насчитывается около 600 ЛУ, представляющих собой периферические лимфоидные органы, состоящие из клеток различных типов, соединяющиеся с системой кровообращения афферентными и эфферентными лимфатическими сосудами и посткапиллярными венулами. Фибробласты и их производные – ретикулярные клетки – образуют поддерживающую структуру ЛУ. Тканевые макрофаги, дендритные клетки и клетки Лангерганса являются важными антигеннесущими клетками. Лимфоидные фолликулы состоят в основном из В-лимфоцитов. Первичные лимфатические фолликулы заселяются IgM- и IgD-несущими В-клетками и Т-лимфоцитами-хелперами (индукторами) еще до антигенного стимула. Вторичные лимфатические фолликулы образуются в результате антигенной стимуляции и содержат внутреннюю зону (зародышевый центр), состоящую из активированных В-клеток, макрофагов, фолликулярных дендритных клеток и Т-хелперов. Зоны между фолликулами и паракортикальные области состоят в основном из Т-лимфоцитов. Совместное расположение большого числа макрофагов, дендритных клеток, клеток Лангерганса и лимфоцитов позволяет ЛУ выполнять основную функцию специализированной структуры, объединяющей все эти типы клеток для создания эффективной клеточной и гуморальной иммунной реакции организма. В связи с этим увеличение ЛУ, или ЛА, обусловлены:
• увеличением количества доброкачественных лимфоцитов и макрофагов в ходе иммунного ответа на антиген;
• инфильтрацией воспалительными клетками при инфекциях, затрагивающих сам ЛУ (лимфаденит);
• пролиферацией in situ злокачественных лимфоцитов и макрофагов;
• инфильтрацией ЛУ метастатическими злокачественными клетками;
• инфильтрацией их макрофагами, нагруженными продуктами метаболизма при различных болезнях накопления.
Классификация
В зависимости от распространенности различают такие варианты ЛА:
• локальную ЛА – увеличение одного ЛУ в одной из областей (единичные шейные, надключичные и т. д.);
• регионарную ЛА – увеличение нескольких ЛУ в одной или двух смежных областях (надключичные и подмышечные, шейные и надключичные и т. д.);
• генерализованную ЛА – увеличение ЛУ более чем в трех областях (шейные, надключичные, подключичные, подмышечные и др.).
|
|
|
Регионарная ЛА отмечается при стрептококковой, стафилококковой инфекции, туляремии, туберкулезе, сифилисе, генитальном герпесе. Генерализованное увеличение ЛУ описано при инфекционном мононуклеозе, цитомегаловирусной инфекции, токсоплазмозе, бруцеллезе, туберкулезе, ВИЧ/СПИДе, болезнях накопления и др. При этом ЛА возникает в результате попадания в ЛУ бактерий либо вирусов и их токсинов лимфогенным, гематогенным и контактным путями.
В клинической практике также часто выделяют острую ЛА, которая характеризуется коротким продромальным периодом, лихорадкой, локальной болезненностью при пальпации, и хроническую ЛА, отличающуюся большей длительностью, как правило, отсутствием болезненности или ее малой выраженностью. При хроническом воспалении, в отличие от острого, ЛУ обычно не спаяны с окружающими тканями. При развитии острой ЛА отмечается серозный отек, а воспалительные явления не выходят за пределы капсулы ЛУ, однако при деструктивных процессах воспаление может переходить на окружающие ткани и по характеру быть серозным и/или гнойным. Для удобства оценки воспалительной реакции со стороны ЛУ ряд авторов предлагают выделять три степени их увеличения:
• I степень – от 0,5 до 1,5 см в диаметре;
• II степень – от 1,5 до 2,5 см в диаметре;
• III степень – от 2,5 до 3,5 см в диаметре и больше.
Этиология
• ЛА инфекционной природы:
• бактериальные: пиогенные бактерии, болезнь кошачьих царапин, туберкулез, лепра, бруцеллез, сифилис, венерическая лимфогранулема, туляремия;
• вирусные: инфекции, вызываемые вирусом Эпштейна–Барр, корь, ВИЧ-инфекция, цитомегаловирусная инфекция, гепатиты;
• грибковые: гистоплазмоз, кокцидиомикоз, актиномикоз;
• паразитарные: токсоплазмоз, трипаносомоз, филяриоз, токсокароз, эхинококкоз, описторхоз, лямблиоз;
• ЛА при системных заболеваниях:
• ревматоидный артрит: синдром Стилла, синдром Фелти;
• саркоидоз;
• системные заболевания соединительной ткани (системная красная волчанка, системная склеродермия и др.);
• ЛА при опухолевых заболеваниях:
• гемобластозы: лимфопролиферативные опухоли, лейкозы;
• метастазы рака в ЛУ;
• эндокринопатии: надпочечниковая недостаточность, тиреотоксикоз;
• лекарственно-индуцированные ЛА: сывороточная болезнь, после применения аллопуринола, атенолола, каптоприла, карбамазепина, цефалоспоринов, препаратов золота, гидралазина, пенициллина, фенитоина, пириметамина, хинидина, сульфаниламидов.
Диагностика
Р.М. Хаитов, Н.И. Ильина (2009) предлагают удобный для практического применения алгоритм диагностического поиска при ЛА (см. рисунок).
Основными критериями дифференциальной диагностики синдрома ЛА, полученными при первичном осмотре больных, могут служить:
• возраст больных;
• анамнестические сведения;
• характер ЛА: локализация, распространенность, размеры, консистенция, болезненность, подвижность ЛУ;
• наличие других клинических признаков: увеличение печени, селезенки, лихорадка, кожные высыпания, суставной синдром, поражение легких и др.;
• показатели периферической крови.
Возраст пациента можно использовать в диагностическом поиске при ЛА. Так, инфекционный мононуклеоз чаще встречается в детском и юношеском возрасте, а хронический лимфолейкоз – у лиц старших возрастных групп. В 80% случаев регионарная ЛА у лиц моложе 30 лет имеет инфекционное происхождение, а у людей старше 50 лет в 60% – неопластический генез. Однако при этом все же возраст больного может служит лишь одним из ориентиров диагностического поиска.
Анамнестические сведения (травмы, контакт с больными инфекционными заболеваниями, животными, прием медикаментов, наркотических средств, наличие онкологических заболеваний, туберкулеза, профессиональный маршрут, хобби, миграционный анамнез и др.) также нередко позволяют определить направление диагностического поиска и в ряде случаев могут играть важную роль в дифференциальной диагностике ЛА
| Анамнез | Вероятная природа ЛА |
| Контакт с кошками | Болезнь кошачьих царапин, токсоплазмоз |
| Употребление сырого мяса | Токсоплазмоз |
| Заболевание туберкулезом в анамнезе | Туберкулезный лимфаденит |
| Недавние переливания крови или трансплантации органов | Цитомегаловирус |
| Случайные незащищенные половые связи | ВИЧ, сифилис, герпес, цитомегаловирус, гепатит В |
| Внутривенное введение наркотиков | ВИЧ, эндокардит, гепатит В |
| Охотники, рыбаки | Туляремия |
| Работники ферм, скотобоен | Эризипелоид |
| Аризона, Южная Калифорния, Нью-Мексико, Западный Техас, Юго-Запад США | Кокцидиоидомикоз |
| Юго-Восток и центральная часть США, Юго-Восточная Азия, Индия, Северная Австралия | Бубонная чума, гистоплазмоз |
| Центральная или Западная Африка | Африканский трипаносомоз (сонная болезнь) |
| Центральная или Южная Америка | Американский трипаносомоз (болезнь Шагаса) |
| Восточная Африка, Средиземноморье, Китай, Латинская Америка | Лейшманиоз |
| Мексика, Перу, Чили, Индия, Пакистан, Египет, Индонезия | Тифоидная лихорадка |
| Таблица 1. Особенности анамнеза, помогающие в диагностике ЛА |
.
Направление диагностического поиска при ЛА во многом зависит от ее локализации, распространенности, а также от размеров, консистенции, подвижности, болезненности ЛУ, наличия дополнительных клинических симптомов (увеличение печени, селезенки, суставной синдром, кожные проявления, поражения легких и плевры, лихорадка, данные ЛОР-осмотра и др.), которые могут стать ключевыми при проведении дифференциальной диагностики данного синдрома.
| При наличии локализованной ЛА необходимо исследовать области, от которых лимфа оттекает в данную группу ЛУ, на предмет наличия воспалительных заболеваний, поражений кожи, опухолей. Необходимо также тщательное обследование всех групп ЛУ, в том числе и несмежных, для исключения генерализованной ЛА. В случае обнаружения увеличенных ЛУ, как указывалось выше, необходимо определить их размер, болезненность, консистенцию, связь между собой и с окружающими тканями, локализацию, распространенность. |
| В большинстве случаев нормальным размером ЛУ считается диаметр не более 1 см; локтевой ЛУ более 0,5 см, а паховые – более 1,5 см в диаметре следует считать патологически измененными. |

|
Размер ЛУ обычно не дает возможности предположить этиологию ЛА, однако у детей увеличение ЛУ более 2 см в диаметре наряду с наличием патологических изменений при рентгенографии органов грудной клетки и отсутствии воспалительных заболеваний ЛОР-органов могут свидетельствовать о наличии гранулематозного процесса (туберкулез, болезнь кошачьих царапин, саркоидоз) или злокачественного заболевания (лимфома).
Болезненность ЛУ возникает при быстром увеличении его в объеме в результате растяжения капсулы ЛУ. Боль возникает при воспалительном процессе с нагноением ЛУ, а также при кровоизлиянии в некротический центр ЛУ при злокачественном поражении. Наличие или отсутствие боли не позволяет дифференцировать доброкачественные процессы в ЛУ от злокачественных.
| Плотные, как камень, ЛУ типичны для онкопатологии и чаще всего указывают на метастазирование основной опухоли. Плотные эластичные ЛУ чаще свидетельствуют в пользу лимфомы. Более мягкие ЛУ, иногда с флюктуацией, характерны для ЛА инфекционной природы. Термин «картечные ЛУ» применяется чаще у детей при вирусных заболеваниях для характеристики множественных мелких ЛУ под кожей в области головы и шеи. Конгломераты ЛУ встречаются при доброкачественных (туберкулез, саркоидоз, венерическая лимфогранулема) и злокачественных (метастазы рака, лимфомы) заболеваниях. |
В ряде случаев анатомическое расположение ЛУ при локализованной ЛА позволяет сузить диагностический поиск
| Группа ЛУ | Дренируемая область | Возможные причины |
| Подчелюстные | Язык, подчелюстная слюнная железа, губы, полость рта, конъюнктива | Инфекционные процессы головы и шеи |
| Подподбородочные | Нижняя губа, дно полости рта, кончик языка, кожа щеки | Мононуклеозоподобный синдром, вирус Эпштейна–Барр, цитомегаловирус, токсоплазмоз |
| Яремные | Язык, миндалины, ушная раковина, околоушная слюнная железа | Фарингит, краснуха |
| Задние шейные | Кожа головы, шеи, верхних конечностей, грудной стенки, шейные и подмышечные ЛУ | Туберкулез, лимфома, злокачественные заболевания головы и шеи, краснуха |
| Затылочные | Кожа головы и шеи | Местный воспалительный процесс, краснуха |
| Заушные | Наружный слуховой проход, ушная раковина, к ожа голов ы | Местный воспалительный процесс, краснуха |
| Передние ушные | Веки, конъюнктива, височная область, ушная раковина, наружный слуховой проход | Местный воспалительный процесс |
| Правый надключичный ЛУ | Средостение, легкие, пищевод | Поражение легких, пищевода |
| Левый надключичный ЛУ | Грудная клетка, брюшная полость через грудной прото к | Лимфома, злокачественное поражение органов брюшной полости и забрюшинного пространства |
| Подмышечные | Верхняя конечность, грудная стенка, молочная железа | Инфекционные заболевания, болезнь кошачьих царапин, лимфома, рак молочной железы, наличие силиконовых имплантатов, бруцеллез, меланома |
| Кубитальный (локтевой) ЛУ | Локтевая часть предплечья и кисти | Инфекционные заболевания, лимфома, саркоидоз, туляремия, вторичный сифилис |
| Паховые | Пенис, мошонка, вульва, влагалище, промежность, ягодичная область, нижняя часть передней брюшной стенки, анальный канал, нижние конечности | Инфекционные процессы нижних конечностей, заболевания, передающиеся половым путем (например, герпес, гонорея, сифилис, шанкроид, паховая гранулема, венерическая лимфогранулема), лимфома, злокачественные заболевания в области таза, бубонная чума |
| Таблица 2. Связь локализации ЛА с возможной причиной ее развития |
. Так, для болезни кошачьих царапин характерно поражение шейных и подмышечных ЛУ, при инфекциях, передающихся половым п утем, – паховых, надключичная ЛА наиболее часто связана со злокачественными заболеваниями. Увеличение параумбиликальных ЛУ также может служить признаком злокачественного процесса в тазу или брюшной полости.
| При регионарной ЛА в первую очередь необходимо определить наличие местного воспалительного процесса, который чаще всего становится причиной увеличения ЛУ. При сочетании местного воспалительного процесса с ЛА следует предполагать реактивный лимфаденит. Динамическое наблюдение за течением местного воспалительного процесса и регионарной ЛА позволяет окончательно верифицировать природу последней. |
Сохраняющиеся плотные ЛУ требуют проведения гистологического исследования. При ЛУ размером не более 1 см2 чаще отмечается реактивная ЛА, а при их размере больше 2 см2 следует подозревать опухолевый или гранулематозный процесс. Плотные ЛУ обычно характерны для метастазов опухолей. У пациентов с генерализованной ЛА клиническое обследование должно фокусироваться на поиске признаков системного заболевания. Наиболее ценным является обнаружение высыпаний, поражения слизистых оболочек, гепато-, спленомегалии, поражения суставов. Спленомегалия и ЛА встречаются при многих заболеваниях, включая мононуклеозоподобный синдром, лимфоцитарную лейкемию, лимфому, саркоидоз.
Одним из объективных вспомогательных методов дополнительной характеристики увеличенных ЛУ является проведение ультразвукового исследования (УЗИ) ЛУ, которое позволяет уточнить их размеры, определить давность патологического процесса и его остроту. При остром воспалении определяется гипоэхогенность и однородность ЛУ. Спаянные ЛУ позволяют предположить продолжительность заболевания более 2 мес. При хроническом течении процесса эхогенность ЛУ повышается.
Алгоритм параклинического обследования больного с синдромом ЛА предполагает использование различных методов диагностики. Так, при первичном осмотре пациента проводится обязательное лабораторно-инструментальное обследование, включающее в себя:
• клинический анализ крови с определением количества эритроцитов, ретикулоцитов, тромбоцитов, лейкоцитарной формулы, СОЭ;
• общий анализ мочи;
• определение маркеров гепатита В и С, ВИЧ, RW;
• биохимическое исследование крови с определением острофазных белков;
• рентгенографию органов грудной клетки;
• УЗИ органов брюшной полости.
Так, лейкоцитоз и сдвиг формулы влево свидетельствуют в пользу бактериального поражения ЛУ (стафилококковой, стрептококковой, синегнойной, гемофильной этиологии); лимфоцитоз и моноцитоз обычно характерны для заболеваний вирусной этиологии (герпес, цитомегаловирус, вирус Эпштейна–Барр и др.).
При углубленном обследовании пациента с ЛА возникает необходимость в использовании дополнительных инструментальных и лабораторных методов исследования, перечень которых может включать в себя:
• рентгенологическое, эндоскопическое исследования органов пищеварения;
• рентгенологическое исследование придаточных пазух носа;
• УЗИ молочных желез и органов малого таза у женщин, предстательной железы у мужчин, щитовидной железы и др.;
• компьютерную томографию (по показаниям);
• определение опухолевых маркеров;
• серологические исследования, использование метода полимеразно-цепной реакции с целью диагностики инфекционных (микоплазма, хламидиоз, токсоплазмоз и др.) и вирусных (вирус герпеса, цитомегаловирус, вирус Эпштейна–Барр) заболеваний;
• иммунологическое обследование (для исключения первичных иммунодефицитных состояний, сопровождающихся ЛА: острая вариабельная иммунная недостаточность, гипер-IgМ-синдром, синдром Вискотта–Олдрича);
• серологическое исследование крови для исключения группы аутоиммунных заболеваний (системной красной волчанки, ревматоидного артрита и др.);
• пункцию, или биопсию, ЛУ с гистологическим исследованием материала.
Так, в биоптатах ЛУ могут обнаруживаться различные по своей природе морфологические изменения: явления гиперплазии при антигенной стимуляции; признаки острого и хронического воспаления с диффузным поражением ЛУ или очаговыми специфическими и неспецифическими изменениями вследствие реакции на вирусы, бактерии, грибы или паразитов; изменения, характерные для разнообразных опухолей ЛУ и метастазов в них опухолей из других органов. При этом диагностика подразделяется на 3 этапа: выявление диффузных процессов неопухолевой природы, воспалительных процессов, а затем – диффузных опухолевых процессов.
Диагностика заболеваний, проявляющихся синдромом ЛА
При неспецифическом лимфадените чаще поражаются подмышечные и паховые ЛУ. Заболевание начинается с болезненного увеличения и уплотнения ЛУ. Они подвижны, не спаяны между собой и покрывающей кожей. При прогрессировании воспаления образуется плотный, монолитный, очень болезненный инфильтрат. Кожа над ним становится неподвижной, гиперемированной, горячей, позже истончается, приобретает вишневую окраску. Появляются флюктуация, и происходит произвольное вскрытие гнойника. Затем гнойник очищается, патологические симптомы регрессируют и наступает выздоровление. В зависимости от распространения лимфаденита наблюдаются лихорадка, озноб, головная боль, потливость, общее недомогание, лейкоцитоз и увеличение СОЭ. Маловирулентная инфекция может вызвать хронический гипопластический лимфаденит. При этом малоболезненные увеличенные ЛУ со временем рубцуются и превращаются в твердые узелки. Лимфаденит может осложняться абсцессом, флегмоной, флеботромбозом, сепсисом, лимфостазом. Важным мероприятием в диагностике является пункция ЛУ.
Туберкулез периферических ЛУ чаще диагностируется у детей и подростков, реже – у взрослых и пожилых людей; может быть самостоятельной формой туберкулеза, но чаще сочетается с туберкулезом другой локализации. Поражаются чаще шейные и подчелюстные ЛУ, реже – подмышечные, крайне редко – паховые и локтевые. Пораженные ЛУ увеличиваются до 1,5 см в диаметре и больше, имеют мягкую или плотную консистенцию. Заболевание может начинаться остро или подостро, сопровождаться повышением температуры тела и выраженной интоксикацией. Воспалительный процесс может распространяться на подкожную клетчатку и кожу. При вовлечении в процесс окружающих тканей образуются плотные, крупные, малоподвижные пакеты ЛУ. Несвоевременная диагностика синдрома ЛА приводит к нагноению ЛУ, кожа над ними становится гиперемированной, появляется флюктуация, происходит произвольное вскрытие гнойника, как следствие, образуются длительно не заживающие свищи. Хроническое течение туберкулеза периферических ЛУ характеризуется наличием плотных ЛУ, образующих конгломераты или цепочки мелких узелков. В гемограмме нередко отмечаются повышенная СОЭ, умеренно выраженный лейкоцитоз с палочкоядерным сдвигом влево и моноцитозом. Диагностика туберкулеза периферических ЛУ основана на данных анамнеза (контакт с больными туберкулезом, туберкулез легких и других органов, рубцы на шее, поражение глаз), объективных данных, положительных результатах туберкулинодиагностики, обнаружения микобактерий туберкулеза в гное, пунктате ЛУ, цитологического исследования пунктатов и гистологического анализа биопсийного материала.
Инфекционный мононуклеоз относится к заболеваниям, вызванным вирусом Эпштейна–Барр. Инкубационный период колеблется от 4 до 15 дней (чаще около недели). Заболевание, как правило, начинается остро. К 2–4-му дню заболевания лихорадка и симптомы общей интоксикации достигают наибольшей выраженности. С первых дней болезни появляется слабость, головная боль, миалгия и артралгия, несколько позже – боли в горле при глотании. Температура тела достигает 38–40 оС. Длительность лихорадки составляет 1–3 нед, иногда – больше. Тонзиллит появляется с первых дней заболевания или развивается позднее на фоне лихорадки и других проявлений инфекции (с 5–7-го дня). Он может быть катаральным, лакунарным или язвенно-некротическим с образованием фибринозных пленок (напоминающих иногда дифтерийные). Некротические изменения в зеве выражены особенно сильно у пациентов со значительным снижением числа лейкоцитов.
ЛА наблюдается почти у всех больных. Чаще поражаются подчелюстные и заднешейные ЛУ, реже – подмышечные, паховые, локтевые. Поражаются не только периферические, но у части пациентов – и мезентериальные ЛУ. У 25% больных, чаще на 3–5-й день болезни, отмечается экзантема, которая может иметь макуло-папулезный (кореподобный), мелкопятнистый, розеолезный, папулезный характер. Элементы высыпаний сохраняются 1–3 дня и бесследно исчезают. С 3–5-гo дня заболевания почти у всех пациентов увеличивается печень и селезенка; гепатоспленомегалия может сохраняться до 3–4 нед. Особенно выражены изменения печени при желтушных формах инфекционного мононуклеоза, которые сопровождаются увеличением уровня сывороточного билирубина, активности аминотрансфераз, особенно АсАТ, щелочной фосфатазы.
| При заболевании инфекционным мононуклеозом взрослые должны быть обязательно обследованы на наличие антител к ВИЧ. |
Стадия генерализованной ЛА относится к числу закономерных состояний при ВИЧ-инфекции и отмечается у 90% больных. При этом в процесс вовлекаются локтевые, под- и надключичные, подбородочные, подчелюстные, около- и заушные, затылочные и особенно часто – подмышечные и шейные ЛУ. Реже увеличиваются паховые, бедренные и подколенные ЛУ.
| ЛА может рассматриваться как клинический признак ВИЧ-инфекции, если она поражает не менее двух групп ЛУ и сохраняется более 3 мес. |
ЛА может протекать по смешанному типу из-за присоединения к реактивным изменениям вторичных инфекционных (в первую очередь микобактериальная инфекция) и неопластических (обычно саркома Капоши) процессов. Увеличенные ЛУ могут уменьшаться и вновь увеличиваться в размерах, таким образом, II и III стадии ВИЧ-инфекции могут чередоваться. При этом ЛА может сохраняться длительно, сопровождаться периодами обострения и ремиссии, оставаясь единственным клиническим признаком ВИЧ-инфекции. Персистирующая генерализованная ЛА может отмечаться и в поздних стадиях ВИЧ-инфекции, однако в этой стадии она является единственным клиническим проявлением болезни. СПИД-ассоциированный симптомокомплекс обычно формируется на фоне генерализованной ЛА спустя 1,5–3 года от ее начала в результате присоединения в разной последовательности и сочетании многочисленных и разнообразных симптомов со стороны различных органов и систем: головная боль, слабость, недомогание, повышенная утомляемость и потливость, лихорадка, кашель, миалгия, артралгия, снижение аппетита, массы тела, диарея, вторичные инфекции, сосудистые изменения, новообразования и другие патологические процессы. Лабораторные изменения сводятся к лейко-, лимфо-, тромбоцитопении и выраженным нарушениям клеточного иммунитета. Для окончательной верификации ВИЧ-инфекции необходимо обнаружение антител к антигенам ВИЧ с помощью лабораторных методов исследования.
ЛА относится к довольно постоянным признакам краснухи. Для данного инфекционного заболевания характерно умеренное увеличение заднешейных, затылочных, иногда – околоушных, переднешейных, подколенных, подмышечных ЛУ, которое может быть множественным или изолированным в виде несимметричного поражения одного из них, иногда сопровождается незначительной болезненностью. В продромальный период (от нескольких часов до 1–2 дней) у пациентов наблюдаются незначительные симптомы интоксикации в виде повышения температуры тела до субфебрильных цифр, недомогания, утомляемости, иногда – сонливости, головной боли, катаральных явлений со стороны ЛОР-органов. Период высыпаний является постоянным при типичных формах краснухи и наиболее отчетливо выраженным. Он чаще всего продолжается 2–3 дня и характеризуется наличием экзантемы. Высыпания у преобладающего числа больных краснухой бледно-розовые, мелкопятнистые, довольно обильные, их элементы почти одинаковой величины с ровными очертаниями на неизмененном фоне. Появляются они одновременно и уже в течение первых суток покрывают лицо, грудь, живот и конечности. Высыпания, как правило, никогда не наблюдаются на ладонях и стопах, исчезают бесследно, как правило, к 4-му дню от момента появления. В гемограмме на 1-й неделе болезни выявляется лейкопения или тенденция к лейкопении. В лейкоцитарной формуле крови у большинства пациентов имеют место лимфоцитоз и нейтропения. На 2-й неделе заболевания количество лейкоцитов повышается, но у значительной части больных может длительно наблюдаться тенденция к лейкопении и лимфоцитозу.
Основным клиническим проявлением лимфомы Ходжкина (лимфогранулематоза) является увеличение различных групп ЛУ. Из первичного очага (чаще надключичные и медиастинальные ЛУ) путем лимфогенного метастазирования заболевание распространяется в другие группы ЛУ. Позже происходит гематогенная диссеминация патологического процесса. Пораженные ЛУ имеют плотно-эластическую консистенцию, не спаяны с кожей, безболезненны. У части больных отмечается типичный симптом – боли в увеличенных ЛУ после употребления алкоголя. У 90% больных первичное поражение локализовано выше диафрагмы. Кольцо Вальдейера–Пирогова, околоушные, затылочные и локтевые ЛУ поражаются крайне редко. Увеличенные ЛУ болезненны, эластичны. Вследствие частого поражения лимфатической ткани, расположенной в грудной клетке, первым симптомом заболевания может быть затруднение дыхания или кашель вследствие давления ЛУ на легкие и бронхи, но чаще поражение средостения обнаруживается при случайной обзорной рентгенографии органов грудной клетки.
Кроме увеличения ЛУ для лимфогранулематоза характерны необъяснимая потеря массы тела более чем на 10% за последние 6 мес, необъяснимые повышения температуры тела выше 38 оС в течение 3 дней, профузная ночная потливость, генерализованный зуд кожи. В гемограмме пациентов отмечаются увеличение СОЭ, незначительный нейтрофилез, лимфопения, анемия, тромбоцитопения, иногда эозинофилия. Диагноз лимфомы Ходжкина устанавливается исключительно на основании морфологии и считается достоверным при обнаружении специфических двуядер<
|
|
|


