 |
Главная нутрициологическая функция
|
|
|
|
НУТРИЦИОЛОГИЯ КАЛЬЦИЯ
Универсальный строительный материал – так может быть сформулирована главная нутрициологическая функция кальция.
Кажется, как пополнить свой организм этим элементом каждый знает предостаточно (молочные продукты, минеральные воды или минеральные добавки, в конце концов, кусочек белого школьного мела и яичная скорлупа).
И все-таки, будем считать, что это не так, до тех пор, пока человечество не в состоянии справиться с остеопорозом своих костей в возрасте мудрости.
Кроме главной структурной функции кальций влияет на:
- проницаемость клеточных мембран, обеспечивая оптимальную передачу нервных импульсов, сокращение скелетной и гладкой мускулатур, деятельность сердечной мышцы (нейромышечная функция);
- функцию эндокринных желез (гормональная). Из всех элементов лишь кальций регулирует гормональный баланс, влияет на гормон паращитовидной железы и тирокальцитонин. Первый переводит в кровь кальций, содержащийся в костях, если в крови есть его недостаток, а второй – контролирует обратный процесс, если он идет слишком интенсивно;
- свертывание крови, через зависимые от кальция ферменты (при кровотечении необходимо повышенное количество кальция);
- уровень образования молока у кормящих женщин;
- поддерживает тонус сосудов за счет влияния на гладкие мышцы, расположенные в стенках сосудов.
- являясь антагонистом натрия, который задерживает воду в организме, кальций способствует выведению (вместе с водой) солей тяжелых металлов и радионуклидов, оказывает противовоспалительное, противоаллергическое и противотоксическое действия (противоядие). Выводя из организма шлаки и токсичные вещества в виде нейтральных солей, кальций содействует снижению утомляемости, снимает усталость, создает бодрое настроение.
|
|
|
2 Элемент Са вокруг нас. Применение.
Содержание в воде и продуктах питания
Кальций занимает пятое место по распространению в природе (содержание в земной коре 2,96%). Несмотря на широкое распространение, даже химики и то не все видели металлический кальций, т.к. он очень активен.
Природных минералов кальция – 385: известняки, мел, мрамор, кальцит, жемчуг, исландский шпат, сталактит, сталагмит, кораллы, перламутр, (карбонаты кальция); гипс, алебастр, селенит (сульфаты кальция), доломит (карбонат магния и кальция); флюорит (фторид кальция) и др. Многие из них появились благодаря деятельности живых организмов (мел, известняк, жемчуг, коралл, перламутр).
Наиболее распространенная в России порода – известняки (название элемента и происходит от латинского «кальцекс» – известь). Известняки состоят из разнообразных остатков органической жизни: раковины, корненожки, полипы, лишайники, морские лилии, ежи, улитки, – все это перемешано между собой в общей массе. Иногда известняки погружались в глубины Земли, где высокие температуры и давление уплотняли и перекристаллизовывали их, создавая горную породу мрамор, использующуюся скульпторами и как облицовочный материал.
В чистом виде известняки белого или светло-желтого цвета, но примеси придают им более темную окраску. Известняки незаменимы в производстве цемента, карбида кальция, соды, всех видов извести (гашеной, негашеной, хлорной) и многих других веществ. Известняками (щебенкой) укрепляют дороги и в виде порошка уменьшают кислотность почв. В сахарной промышленности известняк используют для очистки свекловичного сока. Наиболее чистый карбонат кальция образует прозрачные кристаллы исландского шпата, широко применяемого в оптике.
Мел (его называют еще писчий мел) – не только зубной порошок и школьные мелки. Его используют в качестве наполнителя в бумажной и резиновой промышленности, при ремонте зданий для побелки.
|
|
|
Доломит – важный огнеупорный материал и сырье для производства цемента. Гипс для скрепления камней использовали со времен египетских пирамид. Природный гипс для приобретения способности твердеть на воздухе подвергают предварительному обжигу. При этом гипс теряет три четверти связанной с ним влаги и получается алебастр (или жженый гипс). В сосудах из алебастра хранили лекарства, мази, благовония, используют его до настоящего времени в строительстве.
Помимо вяжущих свойств у жженого гипса есть еще одно полезное свойство. Затвердевая, он присоединяет потерянную при обжиге воду, увеличивается в объеме, позволяя получать слепки.
Флюорит – плавиковый шпат, соединение кальция и фтора – «рудный цветок» поделочный камень. Из него делают бусы, вазы, подсвечники, пепельницы, шкатулки.
В гомеопатии используют ж емчуг (карбонат кальция) – живой драгоценный камень. Он вырастает внутри моллюска, если в него попадает песчинка. [43, 70].
Почва – еще один важнейший источник кальция на планете, и кажется, что при таких огромных запасах кальция на всех его хватит, и все активно потребляют его: растения, особенно лиственные деревья; животные, человек. Однако из распаханной земли вымывается огромное количество кальция, которое невозможно восполнить. В лесах кальций возвращается в почву с опавшей листвой, но это не более трети от всего кальция, потребляемого растениями. Почвы беднеют год от года, можно сказать, Земля больна остеопорозом – из ее коры невосполнимо теряется кальций. Равновесие почвы в отношении кальция существует лишь в тропическом поясе. Там растения активно накапливают кальций в виде биологических минералов: растительный жемчуг в стволах бамбука, в кокосах (выпадает из насыщенного кальцием кокосового молока).
Кроме названных природных соединений важным является применение хлорида кальция (гексагидрата). Получаемый при нагревании последнего, безводный хлорид кальция сильно гигроскопичен, поэтому хорош для сушки жидкостей и газов. В природе хлорид встречается намного реже, чем карбонат и сульфат кальция. Поэтому его получают (как побочный продукт при производстве соды).
|
|
|
Если раствором хлорида кальция (вместо воды) смочить какую-либо поверхность (например, дороги) она будет сырой значительно дольше, т.к. раствор поглощает влагу воздуха. Растворы хлорида кальция используют из-за низкой температуры замерзания и в холодильных системах и против обледенения. Точка плавления смеси 58,8% гексагидрата кальция и 41,2% снега – минус 55ºС.
Растворы хлорида кальция (чаще внутривенно) применяют для снятия спазмов сердечно-сосудистой системы, улучшения свертываемости крови, борьбы с отеками, воспалениями, аллергией.
Древняя медицина применяла и камни из внутренних костей животных, богатые минералами кальция и легче усваиваемые, чем из пищи. К таким лечебным камням относят буйволиный камень, безоаров камень, индрогоровую кость, медвежий камень, носорожий рог, белужий камень, кабаний камень, олений камень, жабий камень, улиткин камень и др. И это не вымысел [70]. Китай и Вьетнам покупают в ЮАР камни из желчных путей диких буйволов и жирафов для приготовления стимулирующих лекарств, популярных за рубежом (в основном экспортируют во Францию).
Безоаров камень, самый известный из подобных камней, обнаруживался в желудке или кишечнике безоарова козла. Камень, по описанию, имел синевато-серый цвет, был мягким и на вкус очень горьким. Он считался универсальным противоядием при отравлениях и упоминался уже Аристотелем. Великий ученый считал этот минерал «испытанным средством» и был уверен в его целебном могуществе, при условии, что отравленному надо было вовремя вложить этот камень в рот. А в последующие эпохи рекомендовалось растереть камень и запить порошок водой.
Позднее целебные свойства безоара стали считать суеверием, и Наполеон, получив от персидского шаха в подарок безоар, бросил его в огонь, сказав, что он не верит в сказки. Однако в 60-е годы XIX столетия американский химик исследовал камень и обнаружил, что в нем содержится гидрофосфат кальция, обменивающий свой фосфат на арсенат [89].
|
|
|
Как известно, Наполеон умер от отравления мышьяком. Так что, выбросив безоаров камень, он сам сократил срок своей жизни. В настоящее время людям, работающим во вредных условиях вместо безоарова камня, выдают молоко.
Мел, или писчий мел, как его называют, применялся в виде порошка для подкормки животных и при плохом росте у детей: до 1/2 чайной ложки мела в растворе воды давали пить в течение дня.
Яичная скорлупа применяется дачниками как удобрение. Прием такой золы внутрь не менее полезен, чем таблетированные препараты кальция [70]. Современные врачи обычно залитую лимонным (или гранатовым) соком молотую яичную скорлупу называют кальциумитом.
Гидроксид кальция (гашеная известь) используется в качестве дезинфицирующего средства. Кроме того, в форме известковой воды (насыщенного водного раствора) применяется в медицине внутрь и снаружи в качестве противовоспалительного, вяжущего и дезинфицирующего препарата.
Хлорид кальция применяют как успокаивающее при лечении неврозов.
Карбонат кальция применяется внутрь не только как кальциевый препарат, но и для адсорбции, нейтрализации кислот. Идет также на изготовление зубного порошка.
Современные фармокопейные, в том числе гомеопатические препараты кальция, БАДы содержат неорганические (чаще карбонаты и фосфаты), или органические (чаще лактат и глюконат) соли кальция, часто естественного происхождения (мел, мрамор, кальцит, кальциумит) и рекомендуются для периодического употребления практически здоровым людям.
Лучшими пищевыми источниками биодоступного кальция считаются (в мг/100 г): сыр и творог (120–1000), обогащенные кальцием молочные продукты (≈300); молоко и молочные продукты (≈120), минеральные воды со средней минерализацией (≈100), рыба, а особенно кости консервированной рыбы (≈100–700), овощи с низким содержанием щавелевой кислоты, например, капуста, репа, сельдерей, салат, лук-порей, петрушка (30–245).
Кальций из щавеля, шпината усваивается плохо из-за большого содержания в них щавелевой кислоты; из моркови, свеклы – из-за клетчатки; из зерновых – из-за фитина.
Кости нашего организма на 40% состоят из кальция, причем до 98,9% кальция содержится в костях и суставах организма. 0,51% кальция из общего кальция присутствующего в организме находится в зубах и 0,51% – в мягких тканях.
В качестве функциональной добавки к пище чаще используют один из препаратов: кальция глюконат, лактат, хлорид, карбонат или фосфаты кальция.
Наиболее легко кальций усваивается организмом из молочных продуктов (за исключением сливочного масла), при этом наиболее функционально активный кальций содержится в козьем и кобыльем молоке.
|
|
|
Тем не менее, чтобы получить необходимые 800 или тем более 1200 мг кальция за счет молочных продуктов, надо выпивать 0,65–1 л молока или съедать 650–800 г творога ежедневно. Содержание кальция в хлебе, крупах, мясе, рыбе и овощах невелико и не может удовлетворить потребность организма в этом элементе при обычных уровнях потребления.
Таблица 1 – Содержание Са в продуктах, мг/100 г
| Продукты | Содержание кальция, мг/100 г | Кол-во продукта, содержащее суточную норму кальция (800–1200 мг) |
| Сыры: твердые мягкие плавленые Творог Хлеб Рыба Мясо, птица Картофель Овощи, ягоды, фрукты Фасоль, горох Соя | 900–1000 450–750 120–150 20–40 20–50 10–20 20–50 100–150 | 650–1000 г 90–120 г 100–160 г 100–260 г 650–800 г 2,0–6,0 кг 1,5–6,0 кг 4,0–12,0 кг 8,0–12,0 кг 1,5–6,0 кг 0,5–1,2 кг 250–350 г |
Низкая жесткость воды, характерная для поверхностных водоисточников Мурманской, Архангельской, Псковской, Новгородской, Вологодской и других областей, Республики Коми, Карелии делает лучшие минеральные воды (5–7 ммоль/л солей) малодоступными для жителей этих регионов.
Обогащать продукты и воду можно хорошо растворимыми солями кальция: хлоридом Е507, глицерофосфатом Е383, лактатом Е327, глутаматом Е623, глюконатом Е778, аскорбатом Е303, изоаскорбатом Е318, цитратом Е333, рибонуклеотидом Е634, пропионатом Е282, тартратом Е354, карбонатами Е170, формиатом Е238, цитратом Е333, кальциевой солью цикламомой кислоты Е952 (≈ в 40 раз слаще сахарозы) и др.
В отдельных случаях предпочтительно обогащение средне (мало) растворимыми солями, например: сульфатом Е516, лактилатом Е482, гидроксидом кальция Е526, смесью фосфатов Е542 и Е341 или плохо (не) растворимыми в воде: алюмосиликатом Е556, ацетатом Е263, фумаратом Е367. Из указанных солей всех хуже усваивается хлорид кальция. Имеются сведения, что лучше всех (из более неполного списка) усваивается цитрат кальция. Специально подобранные под конкретные случаи композиции солей должны быть проверены на отсутствие примесей тяжелых металлов.
3 Нутрициологическая потребность в Ca.
Проявления дефицита и избытка
Адекватный уровень потребления для детей первого года жизни 400–600 мг; для более старших, в зависимости от возраста, 800–1200 мг; для взрослых 800–1000 мг; для беременных и лактирующих женщин 1000–12000 мг кальция в день. Недостаточное поступление кальция с пищей в детском возрасте, снижение его отложения в костной ткани, служит в дальнейшем одним из главных факторов риска возникновения остеопороза. Особенно высока потребность в кальции у подростков в 14–17 лет, беременных и кормящих женщин [166]. Повышенный расход кальция (на 30–50% выше физиологической нормы) наблюдается при отравлениях тяжелыми металлами и другими химическими веществами (ксенобиотиками).
Ученые насчитали около 300 различных патологических состояний, вызванных дефицитом кальция в организме, среди которых:
- рахитические изменения пропорций черепа, искривление позвоночника, костей нижних конечностей;
- уплощение костей таза, что в будущем у женщин может стать причиной тяжелых родов;
остеопороз (рассасывание костной ткани), склонность к переломам костей у лиц пожилого возраста;
- высокая потливость, раннее облысение, тусклый цвет волос;
- склонность кожи к аллергическим сыпям;
- нарушение роста зубов, раннее разрушение эмали;
- повышенная возбудимость нервной системы, раздражительность, подергивание век;
- плохая свертываемость крови, склонность к длительным кровотечениям;
- мышечная слабость, затруднения координации движения.
С дефицитом кальция связаны и низкое плодородие почв, болезни животных. Если животные испытывают дефицит кальция: птицы несут мало яиц, у моллюсков тонкие раковины, млекопитающие остаются маленькими во взрослом возрасте. В молоке домашних животных сравнительно мало кальция. Дикие животные пасутся в степях, а там, в сухом климате, кальций накапливается в почвах в виде гипса и содержится в большом количестве в травах. Потому домашним животным дают минеральную подкормку с известняком или мелом в измельченном виде, ими же обогащают почву.
99% кальция в организме находится в костях и зубах, ногтях и волосах преимущественно в виде гидроксилапатита (гидроксифосфат кальция Са5(РО4)3ОН), его произведение растворимости ПР = 1,6 ∙10–58. В поверхностных слоях костей содержится более растворимый фосфат кальция (ПР = 1,0 ∙10–25) [99]. С возрастом содержание фосфата кальция уменьшается.
Образование костной соли можно отразить общим уравнением [227]:
минерализация
5Са2 + + 3НРО42 – + 4ОН – ↔ Са5(РО4)3ОН.
деминерализация
У взрослого человека весь кальций кости обновляется каждые 5–10 лет, у растущих детей за 1–2 года.
Роль депо (когда при неблагоприятных условиях кальций выходит во внеклеточное пространство и участвует практически во всех биологических процессах) играет, прежде всего, более растворимый по сравнению с гидроксилапатитом, фосфат кальция:
Са3(РО4)2 + Н2О ↔ Са2 + + НРО42 – + ОН –,
НРО42 – + Н2О ↔ Са2 + + Н2РО4 – + ОН –,
Н2РО4 – + Н2О ↔ Са2 + + Н3РО4 + ОН –,
При недостатке фосфата кальция начинает растворяться гидроксилапатит, чему способствует повышение кислотности среды, концентрации лактатов, цитратов и белков, которые связывают ионы кальция в результате комплексообразования:
Са5(РО4)3ОН + 2Н + ↔ Са2 + + Са4Н(РО4)3 + Н2О,
а при большей кислотности среды:
Са5(РО4)3ОН + 7Н + ↔ 5Са2 + + 3Н2РО4 – + Н2О.
Эти же процессы могут протекать с зубами, ведь в полости рта в результате жизнедеятельности микробов образуются пировиноградная, молочная, янтарная кислоты, не только повышающие кислотность среды, но и связывающие катионы кальция в устойчивые комплексные соединения [227].
Таким образом, уровень кальция сыворотки крови тщательно регулируется организмом (примерно 2,5 ммоль/л), чтобы сохранить внеклеточную концентрацию кальция и, таким образом, обеспечить нормальную нейромышечную и гормональную функцию.
Хотя токсичность кальция низкая, и его избыток автоматически удаляется фильтрующей системой организма, высокое поступление витамина D может привести к гиперкальциумии: отложению солей кальция под кожей, в мышцах, железах, сосудах, почках, уменьшая их эластичность. Желчные и мочевые камни – это практически на 90% оксалаты кальция. Верхним допустимым уровнем потребления считается 2500 мг/сут.
4 Оптимизация усвоения Сa.
Синергисты и антагонисты усвоения
Из 800–1200 мг кальция, которые ежедневно должен потреблять человек, усваивается лишь 25–50%. Процент усвоения кальция напрямую зависит в первую очередь от трех факторов: секреции желудка, количества доступных желчных кислот и уровня почечной реабсорбции.
Несмотря на то, что растворимость солей кальция увеличивается в кислой среде желудка, растворенные ионы могут повторно связываться в желудочно-кишечном тракте (особенно в тощей и подвздошной кишке, где рН близок к нейтральному) глюкозой, жирными кислотами, фосфатами, фитатами и оксалатами, образуя соли и комплексы.
Самым растворимым, и, следовательно, наиболее усвояемым из них является глюконат, цитрат кальция и комплексы с аминокислотами белков. Фитин, входящий в состав зерновых продуктов; фосфаты, которых особенно много в мясе и рыбе; щавелевая кислота, содержащаяся в больших количествах в щавеле, шпинате, какао и шоколаде – существенно снижают усвоение кальция.
Лактоза, подвергаясь сбраживанию, поддерживает в кишечнике низкий уровень рН, что препятствует образованию нерастворимых солей фосфорной кислоты (данные получены для младенцев) [55]. Возможно, лактоза улучшает усвоение кальция и у взрослых.
Избыток жира способствует возникновению конкуренции за желчные кислоты и образованию нерастворимых кальциевых мыл. Пшеничные отруби с высоким содержание фитинов препятствуют всасыванию кальция в такой степени, что это использовалось в терапевтических целях при гиперкальциурии. Пищевая клетчатка снижает усвоение кальция настолько, что замена белой муки (22 г пищевых волокон в день) мукой из цельной пшеницы (53 г пищевых волокон в день) при обычном рационе служит причиной отрицательного баланса кальция даже при употреблении его выше нормы [55]. Необходимо распределение по разным приемам пищи продуктов с высоким содержанием кальция и пищевых волокон.
Всасывание кальция улучшается, если они принимаются вместе с пищей, т.к. пища стимулирует желудочную секрецию и моторику, и источники кальция становятся более измельченными и растворимыми, а также при наличии в пище небольшого количества жира, витаминов D, гр. В, фосфора и магния [102]. Сбалансированным, оптимальным для усвоения считается отношение (Са: Р: Мg близкое к: 1,00:0,50:0,20 – для детей до 29 дней; 1,00:0,80:0,12 – первого полугодия жизни; 1,00:0,83:0,12 – второго полугодия; 1,00:1,00:0,19 – с одного до 3 лет; 1,00:1,21:0,25 – с 4 до 6 лет; 1,00:1,50:0,25 – с 7 до 17 лет; 1,00:1,50:0,50 – для взрослых; 1,00:1,50:0,45 – для беременных и кормящих женщин.
Если фосфора недостаточно, наряду с фосфатом кальция в костях откладываются еще более растворимые, следовательно, быстро вымываемые кровотоком из них гидрофосфат (произведение растворимости 2,7∙10 –7) и дигидрофосфат (произведение растворимости 1,0∙10 –3).
Кроме того кальций находится в биологическом антагонизме с ионами алюминия, цинка, свинца, избытком фосфора (Са:Р свыше 1:2), ионами натрия и калия [102, 147].
Между потреблением с пищей избытка фосфора и выведением кальция с мочой установлена обратная связь. Фосфор увеличивает синтез паратгормона (уменьшающего уровень кальция в моче) и оказывает непосредственное влияние на почечный транспорт кальция. Пациенты, получающие полное паренатальное питание из растворов глюкозы и аминокислот имеют большую потерю кальция с мочой и отрицательный баланс кальция, который восстанавливается, назначением оптимального фосфора в растворах.
Большинство продуктов питания далеки от идеального для усвоения соотношения Са:Р в сторону избытка фосфора: свинина 1:21; греча 1:5,5; картофель 1:6; яйца куриные 1:4, хлеб 1:4. Поэтому избыток фосфора в рационе встречается гораздо чаще, чем недостаток. Неблагоприятное соотношение кальция к фосфору в рационе еще более сдвигается в сторону форфора в связи с широким использованием фосфатсодержащих пищевых добавок, в частности полифосфатов, добавляемых в колбасные изделия в качестве влагоудерживающего средства.
Самый высокий процент усвояемости кальция 58 – младенцами из женского молока. При этом содержание кальция в женском молоке (26–30 мг/100 мл) в 2–4 раза ниже, чем его уровень в коровьем молоке (110–120 мг/100 мл). Соотношение кальция и фосфора в женском молоке равно 1:0,5 (коровьем 1:0,8). Большая часть кальция в женском молоке связана с сывороточными белками, а 10–20% – с мембранами жировых глобул. В отличие от этого, в коровьем молоке 25% кальция представлено в виде цитрата, а остальная часть – в виде суспензии коллоидного фосфата кальция и в мицеллах казеина (ККФА, глава 2.5.6.). Низкое содержание кальция в женском молоке не нарушает всасывание железа (имеющее место при избытке кальция в рационе) и ограничивает выведение из организма жирных кислот в виде нерастворимых кальциевых мыл [166]. Из заменителей женского молока усвояемость кальция ниже – примерно 38%.
Натрий и кальций также совместно участвуют в механизмах реабсорбции в почках. Если к диете здоровых женщин, находящихся в постменопаузе, ежедневно на протяжении 10 лет добавлять 3 и 6 г хлорида натрия, то это приводит к подвижности 7,5 и 10%, соответственно, скелетного кальция и является фактором риска остеопороза.
Усвоенные углеводы и белок имеют кальций-уретический эффект и уменьшение почечной реабсорбции, что не компенсируется предварительным увеличением его адсорбции в кишке. На каждые дополнительные 50 г белка рациона теряются с мочой 60 мг кальция. Богатая белками диета у взрослых приводит не только к отрицательному балансу кальция, но и к образованию кацьциевых камней (особенно при дефиците витамина В6 и др.). Кофеин, алкоголь, избыток сахара также увеличивает потерю кальция с мочой. Алюминий, особенно из препаратов, в которых его много (альмагель и др.) не только отрицательно влияет на всасываемость, но и способствует вымыванию кальция из костей.
Усвоение кальция ухудшает, как уже указывалось, избыток магния, цинка и железа, особенно на фоне дефицита витамина С [102].
Таким образом, для эффективного усвоения организмом человека (или животного) кальция пища должна иметь определенный биоэлементный баланс фосфора, магния, натрия, калия, белков, жиров, углеводов, витаминов D, С, гр. В, др. нутриентов и минимальное содержание щавелевой кислоты (оксалатов), фосфатов, фитатов и клетчатки. Указанные выше лучшие источники нутрициологического кальция, для повышения уровня усвояемости:
- могут быть подвержены лишь небольшой коррекции в составе функциональных продуктов;
- потребляться нативными;
- подвержены технологической обработке способами, минимизирующими снижение этого уровня.
Недостаточное потребление усвояемого кальция, характерное для питания 30–40% людей России в современных социально-экономических условиях связано с:
- избыточным содержанием фосфора, фитатов и др. антагонистов кальция в рационах;
- недостаточным потреблением молока и молочных продуктов.
В среднем, необходимо употреблять 1 литр молока в той или другой форме (кисломолочные продукты, супы, какао) [164].
Существенный вклад в улучшение ситуации могли бы внести расширение рынка функциональных минерализованных вод и функциональных продуктов питания, переход на производство газированных напитков без фосфорной кислоты, на технологии производства хлебобулочных изделий с пониженным содержанием фитатов и т.п. и развитие науки о здоровом питании с повышением нутрициологической грамотности населения.
5 Роль кальция
в структуре мицеллы казеина молока
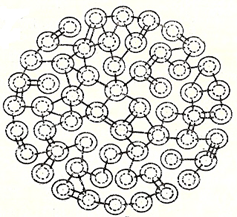
Большая часть (примерно 95%) основного белка молока казеина в молоке содержится в виде субмицелл, связанных фосфатом кальция в мицеллы с молярной массой 108 г/моль.
| 
|
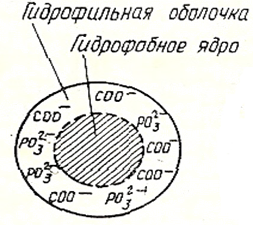
| Р и с. 1 - Строение субмицеллы казеина | Р и с. 2 - Строение мицеллы казеина |
Субмицелла казеина состоит из нескольких фракций различных казеинов, на различиях которых подробно останавливаются авторы всех учебников и учебных пособий по «Химии и физике молока» [50, 243] и будет изучаться вами в соответствующем курсе.
Широк диапазон размеров всегда шаровидных субмицелл казеина 3–300 нм, а средний их размер15–20 нм. Молярная масса казеиновых субмицелл около 250000 г/моль.
Полагают, что ядро субмицеллы состоит из гидрофобных казеиновых молекул и их частей, а гидрофильная оболочка –
из сильно заряженных концевых участков казеинов СОО–, РО32– и др.
Вокруг казеиновых мицелл образуется «гидратная шуба» из молекул воды, которая дополнительно их стабилизирует.
Мицеллы казеина в молоке находятся во взвешенном состоянии в водной фазе, которая содержит:
- растворимый (истинный раствор), в-основном Са(Н2РО4)2, – примерно 30% от общего кальция молока, в том числе около 10% ионизированного кальция;
- коллоидный раствор, в основном, Са3(РО4)2 и фосфатных ассоциатов – в среднем 40% (20–60%).
Мицелярный кальций составляет примерно 30% (20–40%) от общего, в крупных мицеллах его больше.
Между различными состояниями (фракциями) кальция существует взаимообмен кальция. Известно, что за 1 ч в обмене между мицелярным и растворимым кальцием принимает участие 45% атомов кальция [243]:
Са (Н2РО4)2 ↔ Са2 + + 2Н2РО4 –, ПР = 1,0 10–3.
Коллоидный кальций в обмене участвует значительно слабее:
Са3(РО4)2 ↔ 3Са2 + + 2РО43 – , ПР = 1,0 10–25.
Повышение температуры, кислотности и содержания ионизированного кальция способствуют увеличению размеров мицелл. При снижении температуры, кислотности, добавлении воды, цитрата натрия и др. солей, вызывающей образование коллоидных соединений кальция мицеллы мельчают (дисперсность увеличивается).
Соотношение указанных трех видов кальция играет также важную роль в стабилизации белков при тепловой обработке молока. Поэтому различные соли кальция (чаще фосфаты и цитраты) часто добавляют в технологических процессах при производстве молочных продуктов.
Ассоциат казеиновых субмицелл и мицелярного казеината кальция часто называют казеинаткальцийфосфатным комплексом ККФ К [50], что, по мнению автора, не является корректным.
Понятие комплекс устоялось в химической терминологии как соединение имеющие между комплексообразователем и лигандами донорно-акцепторный тип химической связи.
О химической связи между фосфатом кальция казеина и казеином достоверно ничего не известно, есть лишь предположения, что [50]:
- в этой химической связи участвуют карбоксильные СООН– и фосфорсериновые группы РО32–;
- фосфат кальция адсорбирован казеинатами.
Поэтому название ККФК использовать преждевременно, а необходимо говорить о ККФА (казеинаткальцийфосфатном ассоциате), или вообще ограничиваться понятиями мицелла, субмицелла и мицелярный кальций.
Для повышения эффективности свертывания молока сычужным ферментом мицеллы должны быть крупных размеров, т.к. при этом более экономно расходуется фермент, действие которого происходит на поверхности мицелл казеина [163].
При производстве кисломолочных продуктов, чаще всего наоборот, желательны сравнительно небольшие мицеллы, т.к. при этом выше их влагоудерживающая способность, меньше будет происходить отделение сыворотки в готовых продуктах.
2.5.6 Анализ нутриционного статуса в организме,
определение элементов в водах,
продуктах, пищевых добавках
Качественно присутствие кальция можно доказать:
- сжиганием в пламени горелки (кирпично-красный цвет);
- реакцией с оксалатом аммония;
- реакцией с серной кислотой или сульфатами щелочных металлов;
- микрокристаллоскопической реакцией получения сульфата кальция [31].
Количественно ионы кальция могут быть определены:
- с помощью ионселективных электродов;
- фотометрически;
- люминисцентным методом с применением соединений (например, флюорексона), которые с солями кальция в растворах дают флюоресцирующие комплексы;
- комплексонометрическим методом с индикатором кислотным хромовым темно-синим. В шелочной среде комплекс вишнево-красный цвет комплекса Ind ∙ Са при титровании трилоном Б меняется на сине-сиреневую (цвет индикатора).
Разработан «Костный тест» [241], который помогает определить, не теряют ли кости нужный им кальций, не угрожает ли человеку остеопороз.
[ссылки] И.С. Полянская НУТРИЦИОЛОГИЧЕСКАЯ ХИМИЯ S-ЭЛЕМЕНТОВ
Влияние элементов на здоровье
|
|
|


