 |
Вынужденными колебаниями называют колебания, происходящие под действием внешней, периодически изменяющейся силы.
|
|
|
|
 - дифференциальное уравнение вынужденных колебаний. Резонанс резкое возрастание амплитуды установившихся вынужденных колебаний при приближении частоты внешнего гармонического воздействия к частоте одного из собственных колебаний системы.
- дифференциальное уравнение вынужденных колебаний. Резонанс резкое возрастание амплитуды установившихся вынужденных колебаний при приближении частоты внешнего гармонического воздействия к частоте одного из собственных колебаний системы.
27 Резонанс резкое возрастание амплитуды установившихся вынужденных колебаний при приближении частоты внешнего гармонического воздействия к частоте одного из собственных колебаний системы.
28Волна́ — изменение состояния среды или физического поля (возмущение), распространяющееся либо колеблющееся в пространстве и времени или в фазовом пространстве.
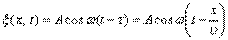 , Уравнение бегущей плоской гармонической волны
, Уравнение бегущей плоской гармонической волны
29 Волна́ — изменение состояния среды или физического поля (возмущение), распространяющееся либо колеблющееся в пространстве и времени или в фазовом пространстве. В поперечной волне колебания происходят в направлении, перпендикулярном направлению распространения волны. Волны, рассматриваемый параметр которых изменяется периодически вдоль оси распространения, называются продольными волнами.
Волново́е число — это отношение 2 π радиан к длине волны:  Длина́ волны́ — расстояние между двумя ближайшими друг к другу точками, колеблющимися в одинаковых фазах.
Длина́ волны́ — расстояние между двумя ближайшими друг к другу точками, колеблющимися в одинаковых фазах.
30 Идеальный газ — математическая модель газа, в которой предполагается, что потенциальной энергией молекул можно пренебречь по сравнению с их кинетической энергией.
 Основное уравнение МКТ
Основное уравнение МКТ
32  барометрическая формула
барометрическая формула
33 Число степеней свободы определяет минимальное количество независимых переменных необходимых для полного описания движения механической системы. Вну́тренняя эне́ргия тела— это сумма энергий молекулярных взаимодействий и тепловых движений молекулы.
|
|
|
34 Теплоёмкость тела) — физическая величина, определяющая отношение бесконечно малого количества теплоты δQ, полученного телом, к соответствующему приращению его температуры δT:
35 Теплопрово́дность — это процесс переноса внутренней энергии от более нагретых частей тела к менее нагретым частям, осуществляемый хаотически движущимися частицами тела.  -закон Фурье
-закон Фурье
36 Диффу́зия — процесс взаимного проникновения молекул одного вещества между молекулами другого, приводящий к самопроизвольному выравниванию их концентраций по всему занимаемому объёму.
37 Явлениями переноса - процесс, в результате которых осуществляется пространственный перенос массы, импульса, энергии.  закон Фика
закон Фика
38 Вя́зкость — одно из явлений переноса, свойство текучих тел (жидкостей и газов) оказывать сопротивление перемещению одной их части относительно другой. Физический смысл коэффициента вязкости заключается в том,
что он показывает, чему равна сила внутреннего трения, действующая на единицу площади поверхности соприкасающихся слоев при единичном градиенте скорости.
39Адиабати́ческий проце́сс — термодинамический процесс в макроскопической системе, при котором система не обменивается тепловой энергией с окружающим пространством
40 Ци́клы — круговые процессы в термодинамике, то есть такие процессы, в которых начальные и конечные параметры, определяющие состояние рабочего тела (давление, объём, температура, энтропия), совпадают.
Цикл Карно́ — идеальный термодинамический цикл. Тепловая машина Карно, работающая по этому циклу, обладает максимальным КПД из всех машин, у которых максимальная и минимальная температуры осуществляемого цикла совпадают соответственно с максимальной и минимальной температурами цикла Карно. Состоит из 2 адиабатических и 2 изотермических процессов. 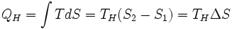

|
|
|

42 Энтропия — функция, устанавливающая связь между макро- и микро- состояниями; единственная функция в физике, которая показывает направленность процессов. Понятие энтропии было впервые введено в 1865 году Рудольфом Клаузиусом. Он определил изменение энтропии термодинамической системы при обратимом процессе как отношение общего количества тепла к величине абсолютной.
43 Теорема Нернста: Энтропия любой системы при абсолютном нуле температуры всегда может быть принята равной нулю. 1-й закон — первое начало термодинамики. Представляет собой формулировку обобщённого закона сохранения энергии для термодинамических процессов. 2-й закон — второе начало термодинамики: Второй закон термодинамики исключает возможность создания вечного двигателя второго рода. Имеется несколько различных, но в то же время эквивалентных формулировок этого закона.
44 Реальный газ — газ, который не описывается уравнением состояния идеального газа Клапейрона — Менделеева. Зависимости между его параметрами показывают, что молекулы в реальном газе взаимодействуют между собой и занимают определенный объём. Состояние реального газа часто на практике описывается обобщённым уравнением Менделеева — Клапейрона: PV3– (RT + bP) vV2+ av2V - abv3= 0. уравнение Ван-дер-Ваальса
45 PV3– (RT + bP) vV2+ av2V - abv3= 0. уравнение Ван-дер-Ваальса.
46 Фаза в термодинамике, термодинамически равновесное состояние вещества, отличающееся по своим физическим свойствам от др. равновесных состояний (других фаз) того же вещества
|
|
|


