 |
Равновесные термодинамические системы. Эквивалентность теплоты и работы. Внутренняя энергия. Первое начало термодинамики.
|
|
|
|
Декремент и логарифмический декремент затухания.
Декремент затухания, количественная характеристика быстроты затухания колебаний. Д. з. d равен натуральному логарифму отношения двух последующих максимальных отклонений х колеблющейся величины в одну и ту же сторону:

Д. з. — величина, обратная числу колебаний, по истечении которых амплитуда убывает в е раз. Например, если d = 0,01, то амплитуда уменьшится в е раз после 100 колебаний. Д. з. характеризует число периодов, в течение которых происходит затухание колебаний, а не время такого затухания. Полное время затухания определяется отношением Т/d.
Добротность колебательной системы.
Добротность колебательной системы, отношение энергии, запасённой в колебательной системе, к энергии, теряемой системой за один период колебания. Добротность характеризует качество колебательной системы, т.к. чем больше Д. к. с., тем меньше потери энергии в системе за одно колебание. Д. к. с. Q связана с логарифмическим декрементом затухания d; при малых декрементах затухания Q " p/d. В колебательном контуре с индуктивностью L, ёмкостью C и омическим сопротивлением R Д. к. с.
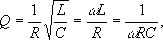
где w — собственная частота контура. В механической системе с массой m, жёсткостью k и коэффициентом трения b Д. к. с.

Добротность — количественная характеристика резонансных свойств колебательной системы, указывающая, во сколько раз амплитуда установившихся вынужденных колебаний при резонансе превышает амплитуду вынужденных колебаний вдали от резонанса, т. е. в области столь низких частот, где амплитуду вынужденных колебаний можно считать не зависящей от частоты. На этом свойстве основан метод измерения Д. к. с. Величина добротности характеризует также и избирательность колебательной системы; чем больше добротность, тем уже полоса частот внешней силы, которая может вызвать интенсивные колебания системы. Экспериментально Д. к. с. обычно находят как отношение частоты собственных колебаний к полосе пропускания системы, т. е. Q = w/Dw. Численные значения Д. к. с.: для радиочастотного колебательного контура 30—100; для камертона 10000; для пластинки пьезокварца 100000; для объёмного резонатора СВЧ колебаний 100—100000.
|
|
|
2. Вопрос
Равновесные термодинамические системы. Эквивалентность теплоты и работы. Внутренняя энергия. Первое начало термодинамики.
Термодинамическое равновесие — состояние изолированной термодинамической системы, при котором в каждой точке для всех химических, диффузионных, ядерных, и других процессов скорость прямой реакции равна скорости обратной.
Термодинамическое равновесие можно делить на термическое, механическое и химическое равновесие, выделяя различные типы физических процессов, на которых достигнуто состояние равновесия.
Согласно нулевому началу термодинамики к термодинамическому равновесию стремитсятермодинамическая система, изолированная от внешних воздействий.
На практике условие изолированности означает, что процессы внутри системы протекают гораздо быстрее, чем обменные процессы с внешней средой.
В реальных процессах часто реализуется неполное равновесие, однако степень этой неполноты может быть существенной и несущественной. При этом возможны три варианта:
1. локальное равновесие — равновесие достигается в какой-либо части (или частях) относительно большой по размерам системы;
2. частичное равновесие — неполное равновесие достигается вследствие разности скоростей релаксационных процессов, протекающих в системе;
3. смешанное — имеют место как локальное, так и частичное равновесие.
|
|
|
МЕХАНИЧЕСКИЙ ЭКВИВАЛЕНТ ТЕПЛОТЫ - количество работы, эквивалентное единице количества теплоты (1 кал или 1 ккал). Понятие M. э. т. возникло с установлением эквивалентности механич. работы ц теплоты и открытием энергии сохранения,закона. Введение M. э. т. потребовалось для сопоставления значений этих физ. величин, измерявшихся в разл. единицах. Экспериментально установлено, что 1 ккал = 426,9 кгс*м.
В Международной системе единиц СИ для работы и кол-ва теплоты принята одна единица измерения - джоуль (1 Дж = 0,239 кал = 0,102 кгс*м), поэтому пользоваться понятием M. э. т. нет необходимости.
Первое начало термодинамики — одно из основных положений термодинамики, являющееся, по существу, законом сохранения энергии в применении к термодинамическим процессам.
Первое начало термодинамики было сформулировано в середине XIX в. в результате работ Ю. Р. Майера, Джоуля и Г. Гельмгольца. Первое начало термодинамики часто формулируют как невозможность существования вечного двигателя 1-го рода, который совершал бы работу, не черпая энергию из какого-либо источника.
Формулировка
Первый закон (первое начало) термодинамики можно сформулировать так:
«Изменение полной энергии системы в квазистатическом процессе равно количеству теплоты Q, сообщенного системе, в сумме с изменением энергии, связанной с количеством вещества N при химическом потенциале μ, и работы A', совершённой над системой внешними силами и полями, за вычетом работы А, совершённой самой системой против внешних сил»:
ΔU = Q − A + μΔN + A'.
Для элементарного количества теплоты δQ, элементарной работы δA и малого приращения (дифференциала) dU внутренней энергии первый закон термодинамики имеет вид:
dU = δQ − δA + μdN + δA'.
Разделение работы на две части, одна из которых описывает работу, совершённую над системой, а вторая – работу, совершённую самой системой, подчёркивает, что эти работы могут быть совершены силами разной природы вследствие разных источников сил.
Важно заметить, что dU и dN являются дифференциалами, а δA и δQ - нет. Приращение теплоты часто выражают через температуру и приращение энтропии: δQ = TdS.
|
|
|


