 |
Окислительно – восстановительные реакции с участием перманганата калия, серной и азотной кислот
|
|
|
|
Цель работы: провести окислительно – восстановительные реакции с участием перманганата калия, серной и азотной кислот.
Оборудование и реактивы: пробирки, пипетки, резиновая груша, стеклянные стаканы, фильтровальная бумага, спиртовка, дистиллированная вода, кристаллический перманганат калия (KMnO4), концентрированные соляная, серная, азотная кислоты (HCl, H2SO4, HNO3), иодид калия (KI), 0,1Н раствор перманганата калия (KMnO4), 10% и 0,1Н раствор серной кислоты (H2SO4), 10% и концентрированный раствор гидроксида натрия (NaOH), раствор сульфита натрия (Na2SO3), гранулы цинка (Zn), медная стружка (Cu), дихромат аммония ((NH4)2Cr2O7), нитрит натрия (NaNO2), сульфат марганца (MnSO4).
Теоретическая часть:
Протекание химических реакций в целом обусловлено обменом частицами между реагирующими веществами. Часто обмен сопровождается переходом электронов от одной частицы к другой. Процесс потери электронов частицей называют окислением, а процесс приобретения электронов – восстановлением. Окисление и восстановление протекают одновременно, поэтому взаимодействия, сопровождающиеся переходом электронов от одних частиц к другим, называют окислительно-восстановительными реакциями.
Протекание окислительно-восстановительных реакций сопровождается изменением степеней окисления элементов участвующих в реакции веществ. При восстановлении степень окисления элемента уменьшается, при окислении – увеличивается. Вещество, в состав которого входит элемент, понижающий степень окисления, называют окислителем, вещество, в состав которого входит элемент, повышающий степень окисления, называют восстановителем.
Практическая часть:
1) В препараторской насыпали в пробирку небольшое количество кристаллического перманганата калия;
|
|
|
2) Добавили несколько капель концентрированной соляной кислоты (наблюдаем шипение и выделение газа - хлора);
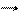 2КMnO4 + 16HCl 5Cl2↑ + 2KCl + 2MnCl2 + 8H2O
2КMnO4 + 16HCl 5Cl2↑ + 2KCl + 2MnCl2 + 8H2O
 |
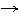 (MnO4)- + 8H+ + 5
(MnO4)- + 8H+ + 5  Mn2+ + 4H2O
Mn2+ + 4H2O
 2Cl- - 2
2Cl- - 2  2Cl0
2Cl0
 2(MnO4)- + 16H+ + 10Cl- 2 Mn2+ + 8H2O + 10Cl0
2(MnO4)- + 16H+ + 10Cl- 2 Mn2+ + 8H2O + 10Cl0
3) Поднесли к отверстию пробирки смоченную раствором йодида калия фильтровальную бумагу. Выделяющийся из пробирки хлор замещал йодид ион в растворе йодида калия. В результате этого мы наблюдали потемнение фильтровальной бумаги вокруг отверстия пробирки, связанное с выделение йода;
 2KI + Cl2 2KCl + I2↓
2KI + Cl2 2KCl + I2↓
4) В 3 пробирки налили по 1 мл. 1Н раствора перманганата калия;
5) В первую пробирку добавили 1 мл. 10% раствор серной кислоты;
6) Во вторую пробирку 10% раствор гидроксида натрия;
7) В каждую из трёх пробирок добавили 1Н раствор сульфида натрия;
В первой пробирке (кислая среда):
 2КMnO4 + 3H2SO4 + 5Na2SO3 K2SO4 + 2MnSO4 + 5Na2SO4 + 3H2O
2КMnO4 + 3H2SO4 + 5Na2SO3 K2SO4 + 2MnSO4 + 5Na2SO4 + 3H2O
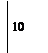
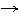 (MnO4)- + 8H+ + 5
(MnO4)- + 8H+ + 5  Mn2+ + 4H2O
Mn2+ + 4H2O
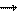 SO32- + H2O - 2
SO32- + H2O - 2  SO42- + 2H+
SO42- + 2H+
 2(MnO4)- + 16H+ + 5SO32- + 5H2O 2 Mn2+ + 8H2O + 5SO42- + 10H+
2(MnO4)- + 16H+ + 5SO32- + 5H2O 2 Mn2+ + 8H2O + 5SO42- + 10H+
Наблюдаем обесцвечение раствора;
Во второй пробирке (щелочная среда):
 2КMnO4 + 2NaOH + Na2SO3 Na2 MnO4 + K2MnO4 + Na2SO4 + H2O
2КMnO4 + 2NaOH + Na2SO3 Na2 MnO4 + K2MnO4 + Na2SO4 + H2O
 |
 (MnO4)- + 1
(MnO4)- + 1  (MnO4)2-
(MnO4)2-
 SO32- + 2OH- - 2
SO32- + 2OH- - 2  SO42- + H2O
SO42- + H2O
 2(MnO4)- + SO32- + 2OH- 2(MnO4)2- + SO42- + H2O
2(MnO4)- + SO32- + 2OH- 2(MnO4)2- + SO42- + H2O
Наблюдаем появление светло – зелёной окраски, из – за появление иона (MnO4)2-;
В третей пробирке (нейтральная среда):
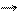 2КMnO4 + 3Na2SO3 + Н2О 2MnO2↓ + 3Na2SO4 + 2KOH
2КMnO4 + 3Na2SO3 + Н2О 2MnO2↓ + 3Na2SO4 + 2KOH

 (MnO4)- + 2H2O +3
(MnO4)- + 2H2O +3  (MnO2)0 + 4OH-
(MnO2)0 + 4OH-
 SO32- + 2OH- - 2
SO32- + 2OH- - 2  SO42- + H2O
SO42- + H2O
 2(MnO4)- + 4H2O + 3SO32- + 6OH- 2(MnO2)0 + 8OH- + 3SO42- + 3H2O
2(MnO4)- + 4H2O + 3SO32- + 6OH- 2(MnO2)0 + 8OH- + 3SO42- + 3H2O
Цвет раствора стал бурым, благодаря появлению оксида марганца (IV);
Вывод:
Перманганат – ион проявляет более высокую окислительно – восстановительную активность в кислой среде.
8) Налили в две пробирки по 1 мл. 0,01Н раствора перманганата калия и добавили несколько капель 10% раствора серной кислоты;
9) В первую пробирку добавили добавили 1Н раствор сульфита натрия, а во вторую 1Н раствор йодида калия до появления устойчивой окраски;
Первая пробирка:
|
|
|
 2КMnO4 + 3H2SO4 + 5Na2SO3 K2SO4 + 2MnSO4 + 5Na2SO4 + 3H2O
2КMnO4 + 3H2SO4 + 5Na2SO3 K2SO4 + 2MnSO4 + 5Na2SO4 + 3H2O
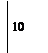
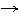 (MnO4)- + 8H+ + 5
(MnO4)- + 8H+ + 5  Mn2+ + 4H2O
Mn2+ + 4H2O
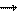 SO32- + H2O - 2
SO32- + H2O - 2  SO42- + 2H+
SO42- + 2H+
 2(MnO4)- + 16H+ + 5SO32- + 5H2O 2 Mn2+ + 8H2O + 5SO42- + 10H+
2(MnO4)- + 16H+ + 5SO32- + 5H2O 2 Mn2+ + 8H2O + 5SO42- + 10H+
Раствор обесцветился;
Вторая пробирка:
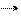 2КMnO4 + 8H2SO4 + 10KI 5I2↓ + 6K2SO4 + 2MnSO4 + 8H2O
2КMnO4 + 8H2SO4 + 10KI 5I2↓ + 6K2SO4 + 2MnSO4 + 8H2O
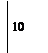
 (MnO4)- + 8H+ + 5
(MnO4)- + 8H+ + 5  Mn2+ + 4H2O
Mn2+ + 4H2O
 2I- - 2
2I- - 2  2I0
2I0
 2(MnO4)- + 16H+ + 10I- 2Mn2+ + 8H2O + 10I0
2(MnO4)- + 16H+ + 10I- 2Mn2+ + 8H2O + 10I0
Выделяющийся йод образовывал с избытком иодида калия йодную воду, вследствие чего раствор приобрёл коричневую окраску;
10) В одну пробирку положили несколько гранул цинка, а во вторую – немного медной стружки;
11) Прилили в обе пробирки 10% раствор серной кислоты;
 Zn + H2SO4 ZnSO4 + H2↑ – выделяется водород;
Zn + H2SO4 ZnSO4 + H2↑ – выделяется водород;
 Сu + H2SO4 Реакция не идёт, так как медь стоит в ряду активности металлов правее водорода и не способна вытеснить водород из кислоты;
Сu + H2SO4 Реакция не идёт, так как медь стоит в ряду активности металлов правее водорода и не способна вытеснить водород из кислоты;
12) Повторили опыт с концентрированной серной кислотой;
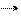 Zn + 2H2SO4 ZnSO4 + SO2 ↑ + 2H2O
Zn + 2H2SO4 ZnSO4 + SO2 ↑ + 2H2O

 Zn0 - 2
Zn0 - 2  Zn2+
Zn2+
 SO42- + 4H+ + 2
SO42- + 4H+ + 2  (SO2)0 + 2H2O
(SO2)0 + 2H2O
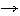 Zn0 + SO42- + 4H+ Zn2+ + (SO2)0 + 2H2O
Zn0 + SO42- + 4H+ Zn2+ + (SO2)0 + 2H2O
 Cu + 2H2SO4 CuSO4 + SO2 ↑ + 2H2O
Cu + 2H2SO4 CuSO4 + SO2 ↑ + 2H2O
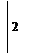
 Cu0 - 2
Cu0 - 2  Cu2+
Cu2+
 SO42- + 4H+ + 2
SO42- + 4H+ + 2  (SO2)0 + 2H2O
(SO2)0 + 2H2O
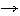 Cu0 + SO42- + 4H+ Cu2+ + (SO2)0 + 2H2O
Cu0 + SO42- + 4H+ Cu2+ + (SO2)0 + 2H2O
В обоих случаях наблюдаем выделение оксида серы (IV);
13) В две чистых пробирки поместили немного медных стружек;
14) В первую пробирку прилили немного концентрированной азотной кислоты, а во вторую немного разбавленной азотной кислоты;
 Сu + 4HNO3 (конц.) Сu(NO3)2 + 2NO2 ↑ + 2H2O – выделяется бурый газ NO2;
Сu + 4HNO3 (конц.) Сu(NO3)2 + 2NO2 ↑ + 2H2O – выделяется бурый газ NO2;
 Cu0 - 2
Cu0 - 2  Cu2+
Cu2+
 (NO3)- + 2H+ +1
(NO3)- + 2H+ +1  (NO2)0 + H2O
(NO2)0 + H2O
 Cu0 + 2(NO3)- + 4H+ Cu2+ + 2(NO2)0 + 2H2O
Cu0 + 2(NO3)- + 4H+ Cu2+ + 2(NO2)0 + 2H2O
 3Сu + 8HNO3 (разб.) 3Сu(NO3)2 +2NO ↑ + 4H2O – выделяется бесцветный газ оксид азота (II)
3Сu + 8HNO3 (разб.) 3Сu(NO3)2 +2NO ↑ + 4H2O – выделяется бесцветный газ оксид азота (II)
 |
 Cu0 - 2
Cu0 - 2  Cu2+
Cu2+
 (NO3)- + 4H+ +3
(NO3)- + 4H+ +3  (NO)0 + 2H2O
(NO)0 + 2H2O
 3Cu0 + 2(NO3)- + 8H+ 3Cu2+ + 2(NO)0 + 4H2O
3Cu0 + 2(NO3)- + 8H+ 3Cu2+ + 2(NO)0 + 4H2O
Вывод:
Перманганат калия, серная и азотная кислоты проявляют сильные окислительные свойства, причём наиболее сильные окислительные свойства перманганат калия проявляет в кислой среде.
|
|
|


