 |
Восстанавливающие дисахариды
|
|
|
|
Билет 71.
Природные дисахариды: мальтоза,лактоза,сахароза,целлюлоза.Их строение,цикла и оксо таутомерия и биологическое значение.Восстанавливающие и невосстанавливающие дисахариды.
Дисахариды состоят из двух моносахаридных остатков, связанных гликозидной связью. Их можно рассматривать как О-гликозиды, в которых агликоном является остаток моносахарида.
Возможно два варианта образования гликозидной связи:
1) за счет гликозидного гидроксила одного моносахарида и спиртового гидроксила другого моносахарида;
2) за счет гликозидных гидроксилов обоих моносахаридов.
Дисахарид, образованный первым способом, содержит свободный гликозидный гидроксил, сохраняет способность к цикло-оксо-таутомерии и обладает восстанавливающими свойствами.
В дисахариде, образованном вторым способом, нет свободного гликозидного гидроксила. Такой дисахарид не способен к цикло-оксо-таутомерии и является невосстанавливающим.
В природе в свободном виде встречается незначительное число дисахаридов. Важнейшими из них являются мальтоза,, лактоза и сахароза.
Мальтоза содержится в солоде и образуется при неполном гидролизе крахмала. Молекула мальтозы состоит из двух остатков D-глюкозы в пиранозной форме. Гликозидная связь между ними образована за счет гликозидного гидроксила в a-конфигурации одного моносахарида и гидроксильной группы в положении 4 другого моносахарида. 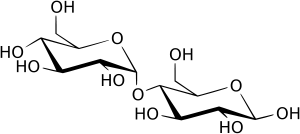


Мальтоза – это восстанавливающий дисахарид. Она способна к таутомерии и имеет a- и b-аномеры
Лактоза с одержится в молоке (4-5%). Молекула лактозы состоит из остатков D-галактозы и D-глюкозы, связанных b-1,4-гликозидной связью. Лактоза – восстанавливающий дисахарид.
|
|
|


Сахароза содержится в сахарном тростнике, сахарной свекле, соках растений и плодах. Она состоит из остатков D-глюкозы и D-фруктозы, которые связаны за счет гликозидных гидроксилов. В составе сахарозы D-глюкоза находится в пиранозной, а D-фруктоза – в фуранозной форме. Сахароза – невосстанавливающий дисахарид. 

Целлюлоза тоже является природным полимером. Ее макромалекула состоит из многих остатков молекул глюкозы. Белое твердое вещество, нерастворимое в воде, молекула имеет линейное (полимерное) строение, структурная единица — остаток β-глюкозы [С6Н7О2(OH)3]n. Полисахарид, главная составная часть клеточных оболочек всех высших растений.

Роль сахарозы:
Переваривание сахарозы начинается в тонком кишечнике.Кратковременное воздействие амилазы слюны существенной роли не играет,так как в просвете желудка кислая среда инактивирует этот фермент.
В тонком кишечнике сахароза под действием фермента сахаразы,продуцируемой клетками кишечника,не выделяясь в просвет, а действуя на поверхности клеток (пристеночное пищеварение)
Расщепление сахарозы приводит к высвобождению глюкозы и фруктозы.Проникновение моносахаридов через клеточные мембраны (всасывание)происходит путем облегченной диффузии при участии специальных транслоказ.Глюкоза всасывается еще и путем активного транспорта за счет градиента концентрации ионов натрия.Это обеспечивает ее всасывание даже при низкой концентрации в кишечнике.
МАЛЬТОЗЫ:
Мальтоза легко усваивается организмом человека. Расщепление мальтозы до двух остатков глюкозы происходит в результате действия фермента a-глюкозидазы, или мальтазы, которая содержится в пищеварительных соках животных и человека, в проросшем зерне, в плесневых грибах и дрожжах. Генетически обусловленное отсутствие этого фермента в слизистой оболочке кишечника человека приводит к врождённой непереносимости мальтозы — тяжёлому заболеванию, требующему исключения из рациона мальтозы, крахмала и гликогена или добавления к пище фермента мальтазы.
|
|
|
ЛАКТОЗЫ:
Биологическая роль лактозы такая же, как и у всех углеводов. В просвете тонкого кишечника под воздействием фермента лактазы она гидролизуется до глюкозы и галактозы, которые и усваиваются. Кроме того, лактоза облегчает всасывание кальция и является субстратом для развития полезных лактобактерий, которые составляют основу нормальной микрофлоры кишечника.
ЦЕЛЛЮЛОЗЫ:
целлюло́за
(клетчатка), полисахарид, полимер глюкозы. В клеточных стенках растений играют роль арматуры (каркаса), обеспечивая механическую прочность и эластичность растительных тканей. Особенно много целлюлозы в древесине – до 50%. Большинство животных не усваивает клетчатку, т.к. она, в отличие от крахмала, не расщепляется ферментом амилазой. Травоядные животные (жвачные) усваивают её благодаря целлюлазе – ферменту, вырабатываемому симбиотическими микроорганизмами, присутствующими в их желудке (гл. обр. в его отделе – рубце). Целлюлоза – один из самых распространённых природных полимеров.
Восстанавливающие дисахариды
В этих дисахаридах один из моносахаридных остатков участвует в образовании гликозидной связи за счет гидроксильной группы (чаще всего при С-4). В дисахариде имеется свободная полуацетальная гидроксильная группа, вследствие чего сохраняется способность к раскрытию цикла.
Восстановительные свойства таких дисахаридов и мутаротация их растворов обусловлены цикло-оксо-таутомерией.
Представителями восстанавливающих дисахаридов являются мальтоза, целлобиоза, лактоза
Невосстанавливающие:
К этой группе принадлежит небольшое число дисахаридов, важнейшим из которых является сахароза.
В невосстанавливающих дисахаридах «вторая» молекула моносахарида в названии получает характерный для гликозидов суффикс –озид, например «фруктофуранозид» в сахарозе.
Наиболее характерной реакцией дисахаридов является кислотный гидролиз, приводящий к расщеплению гликозидной связи с образованием моносахаридов (во всех таутомерных формах). В общих чертах эта реакция аналогична гидролизу алкилгликозидов
|
|
|

Билет 73
Брожение углеводов, его применение. Молочнокислое брожение - процесс анаэробного окисления углеводов, конечным продуктом при котором выступает молочная кислота. Название получило по характеру продукта - молочной кислоте. Для молочнокислых бактерий является основным путём катаболизма углеводов и основным источником энергии в виде АТФ. Также молочнокислое брожение происходит в тканях животных в отсутствие кислорода при больших нагрузках.
Белки молока являются отличным источником азотистого питания для молочнокислых бактерий, которые расщепляют молочный сахар, превращая его в молочную кислоту, повышают кислотность среды, и молоко свёртывается, образуя плотный однородный сгусток.
Виды молочнокислого брожения. Различают гомоферментативное и гетероферментативное молочнокислое брожение, в зависимости от выделяющихся продуктов помимо молочной кислоты и их процентного соотношения. Отличие также заключается и в разных путях получения пирувата при деградации углеводов гомо- и гетероферментативными молочнокислыми бактериями.
Гомоферментативное молочнокислое брожение. Поскольку расщепление лактозы происходит внутри клетки микроорганизма, ключевым этапом этого метаболического пути является поступление глюкозы в клетку. При переносе лактозы снаружи в цитоплазматическую мембрану и в клетку микроорганизма для превращения в фосфат лактозы участвуют четыре белка (последовательно: фермент II, III, I и HPr). Лактозо-6-фосфат гидролизуется b-фосфогалоктогеназой (b-Pgal) на его моносахаридные компоненты. Галактоза и глюкоза затем катаболизируются через тагатозный путь и путь Эмбдена-Мейергофа-Парнаса (EMP). Возможно дефосфорилирование галактозы, и в этом случае она неусваивается и выводится из клетки микроорганизма. В обоих случаях глюкоза и галактоза превращаются дигидроксиацетон-фосфат и глицеринальдегид-3-фосфат, где трёхуглеродные сахара окисляются дальше до фосфоенолпирувата, а затем образуют молочную кислоту при помощи лактатдегидрогеназы. Продуктом гомоферментативного молочнокислого брожения является молочная кислота, которая составляет не менее 90% всех продуктов брожения. Примеры гомоферментативных молочнокислых бактерий: Lactobacillus casei, L. acidophilus, Streptococcus lactis.
|
|
|
Гетероферментативное молочнокислое брожение. Лактозу и глюкозу по гетероферментативному пути образуют только бифидобактерии. При катаболизме глюкозы СО2 не образуется, поскольку отсутствует начальный этап, включающий декарбоксилирование. Лактоза транспортируется в клетку с помощью пермеазы, а затем гидролизуется в глюкозу и галактозу. Альдолаза и глюкозо-6-фосфатдегидрогеназа у этого вида отсутствуют. Гексозы подвергают катаболизму путём гексозомонофосфатного шунта с участием фруктозо-6-фосфат-фосфокетолазы. Продуктами ферментации видами Bifidobacterium являются лактат и ацетат, а ферментация двух молекул глюкозы даёт три молекулы ацетата и две молекулы лактата. Побочными продуктами являются: уксусная кислота, этанол. Примеры гетероферментативных молочнокислых бактерий: L. fermentum, L. brvis, Leuconostoc mesenteroides, Oenococcus oeni.
Молочнокислое брожение используется в молочной промышленности для изготовления простокваши, творога, сметаны, кефира, сливочного масла, ацидофильного молока и ацидофильной простокваши, сыров, квашеных овощей, при приготовлении хлебных заквасок, молочной кислоты. Молочнокислые бактерии широко применяют также при силосовании кормов, при выделке меховых шкурок и в производстве молочной кислоты.
Большое значение эти бактерии имеют при квашении овощей, силосовании кормов (растительной массы) для животных, в хлебопечении, особенно при изготовления ржаного хлеба. Положительные результаты дают исследования по использованию молочнокислых бактерий при изготовлении некоторых сортов колбас, солено-вареных мясных изделий, а также при созревании слабосоленой рыбы для ускорения процесса и придания продуктам новых ценных качеств(вкуса, аромата, консистенции и др.).
Промышленное значение имеет также применение молочнокислых бактерий для получения молочной кислоты, которую используют в безалкогольных напитках.
Спиртовое брожение (осуществляется дрожжами и некоторыми видами бактерий), в ходе него пируват расщепляется на этанол и двуокись углерода. Из одной молекулы глюкозы в результате получается две молекулы питьевого спирта (этанола) и две молекулы углекислого газа. Этот вид брожения очень важен в производстве хлеба, пивоварении, виноделии и винокурении. Если в закваске высока концентрация пектина, может также производиться небольшое количество метанола. Обычно используется только один из продуктов; в производстве хлеба алкоголь улетучивается при выпечке, а в производстве алкоголя двуокись углерода обычно уходит в атмосферу, хотя в последнее время её стараются утилизировать.
|
|
|
Молочнокислое брожение, в ходе которого пируват восстанавливается до молочной кислоты, осуществляют молочнокислые бактерии и другие организмы. При сбраживании молока молочнокислые бактерии преобразуют лактозу в молочную кислоту, превращая молоко в кисломолочные продукты (йогурт, простокваша и др.); молочная кислота придаёт этим продуктам кисловатый вкус.
Билет 74
Номенклатура,
классификация аминокислот.
Билет 75
Стериоизомерия аминокислот. Кислотно-основные свойства, биополярная структура аминокислот. Аминокислотами называются органические карбоновые кислоты, у которых как минимум один из атомов водорода углеводородной цепи замещен на аминогруппу. В зависимости от положения группы —NН2 различают α, β, γ и т. д. L-аминокислоты. К настоящему времени в различных объектах живого мира найдено до 200 различных аминокислот. В организме человека содержится около 60 различных аминокислот и их производных, но не все они входят в состав белков.
Аминокислоты делятся на две группы:
1. протеиногенные (входящие в состав белков)
Среди них выделяют главные (их всего 20) и редкие. Редкие белковые аминокислоты (например, гидроксипролин, гидроксилизин, аминолимонная кислота и др.) на самом деле являются производными тех же 20 аминокислот.
Остальные аминокислоты не участвуют в построении белков; они находятся в клетке либо в свободном виде (как продукты обмена), либо входят в состав других небелковых соединений. Например, аминокислоты орнитин и цитруллин являются промежуточными продуктами в образовании протеиногенной аминокислоты аргинина и участвуют в цикле синтеза мочевины; γ-амино-масляная кислота тоже находится в свободном виде и играет роль медиатора в передаче нервных импульсов; β-аланин входит в состав витамина — пантотеновой кислоты.
2. непротеиногенные (не участвующие в образовании белков)
Непротеиногенные аминокислоты в отличие от протеиногенных более разнообразны, особенно те, которые содержатся в грибах, высших растениях. Протеиногенные аминокислоты участвуют в построении множества разных белков независимо от вида организма, а непротеиногенные аминокислоты могут быть даже токсичны для организма другого вида, т. е. ведут себя как обычные чужеродные вещества. Например, канаванин, дьенколевая кислота и β-циано-аланин, выделенные из растений, ядовиты для человека.
|
|
|


