 |
Уравнение Клапейрона - Клаузиуса (пример использования теоремы Карно)
|
|
|
|
Процесс перехода вещества из жидкого состояния в газообразное (пар) называется испарением. Вылетающая с поверхности жидкости молекула должна преодолеть притяжение молекул, остающихся у нее «за спиной». Это могут сделать только наиболее быстрые молекулы, кинетическая энергия которых значительно превышает среднюю кинетическую энергию молекул в системе. Напомним, что среднее значение кинетической энергии молекул определяется температурой. Удаляясь от поверхности, испаряющиеся молекулы замедляются, так что температура пара оказывается равной температуре жидкости.
В результате ухода быстрых молекул жидкость охлаждается. Для поддержания ее температуры постоянной требуется подвод теплоты. Количество тепла, которое необходимо подвести к системе, чтобы изотермически перевести из жидкости в пар единицу массы вещества, называется удельной теплотой испарения. Часто бывает удобно использовать молярную теплоту испарения l, т.е. количество тепла, необходимое для изотермического перевода одного моля вещества из жидкости в пар.
Наряду с испарением идет обратный процесс - процесс конденсации, т.е. переход вещества из пара в жидкость. Подлетая к поверхности жидкости, молекула пара ускоряется под действием сил притяжения, поэтому кинетическая энергия приходящих молекул значительно превышает среднюю. Это ведет к повышению температуры жидкости. Чтобы обеспечить неизменность температуры, необходимо отводить тепло. Количество тепла, выделяющееся при изотермической конденсации некоторого количества пара, равно количеству тепла, поглощаемому при испарении такого же количества жидкости.
Рассмотрим закрытую двухфазную однокомпонентную систему, например, жидкость и ее пар, находящуюся в цилиндре с поршнем. Система находится в равновесии, а пар называется насыщенным, если число молекул, переходящих в единицу времени из жидкости в пар в среднем равно числу молекул, возвращающихся из пара в жидкость. Такое равновесие при заданной температуре может иметь место только при определенном давлении пара.
|
|
|
Используем теорему Карно для нахождения зависимости Р (Т) - давления насыщенного пара от температуры.
 Рис. 12.1
Рис. 12.1
|
Проведем цикл Карно, используя в качестве рабочего тела рассматриваемую двухфазную систему. Так как давление насыщенного пара однозначно определяется температурой, то для такой системы изотермы T = const являются в то же время изобарами Р = const. На диаграмме P-V (рис. 12.1)изотермы будут прямыми, параллельными оси V. Пусть начальное состояние системы изображается точкой 1. Приведя систему в тепловой контакт с нагревателем, имеющим температуру Т, будем проводить квазистатическое изотермическое расширение до состояния 2. При этом некоторое количество жидкости (n молей) превращается в пар. Разность объемов V 2 – V 1 можно выразить через молярные объемы жидкости ua и пара ub
V 2 – V 1 = n×(ub - ua).
Чтобы обеспечить изотермическое превращение в пар n молей жидкости, система в процессе 1-2 должна получить от нагревателя количество тепла
Q 1 = n×l.
После этого устраним контакт с нагревателем и, адиабатически изолировав систему, заставим ее расширяться по бесконечно короткой адиабате 2-3. При испарении жидкости без подвода тепла температура системы понижается до температуры холодильника T – dT, которая бесконечно мало отличается от температуры нагревателя Т. Давление пара при этом также понизится до величины P – dP. Из состояния 3 вернем систему по изотерме 3-4 и адиабате 4-1 в исходное состояние 1.
В результате система совершит бесконечно малый цикл Карно. Работа цикла равна площади, охватываемой им на P-V диаграмме. Так как адиабаты 2-3 и 4-1 бесконечно короткие, фигуру 1-2-3-4 можно считать параллелограммом, основание которого V 2 – V 1, а высота – dP.
|
|
|
Тогда работа А, совершаемая системой за цикл, равна
A = (V 2 – V 1) ×dP = n×(ub - ua)× dP.
КПД цикла
 . (12.1)
. (12.1)
Согласно теореме Карно, КПД цикла Карно определяется только температурами нагревателя Т 1 и холодильника Т 2, и не зависит от рода рабочего тела
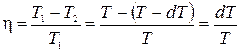 . (12.2)
. (12.2)
Сравнивая выражения (12.1) и (12.2) получим
 .
.
Отсюда следует уравнение Клапейрона-Клаузиуса
 . (12.3)
. (12.3)
Отметим, что если теплоту фазового перехода l и объемы ua и ub относить к единице массы вещества, уравнение (12.3) сохранит свой вид.
Уравнение Клапейрона-Клаузиуса дает (в дифференциальной форме) связь между давлением и температурой, при которых две фазы находятся в равновесии друг с другом. Соотношение (12.3) определяет условия равновесия фаз не только для жидкости и пара, но и для систем жидкость – твердое тело и твердое тело – пар. Для системы жидкость-пар уравнение (12.3) при некоторых упрощающих предположениях удается проинтегрировать.
Если температура системы значительно меньше критической (при которой исчезает различие между жидкостью и паром), то молярным объемом жидкости ua можно пренебречь по сравнению с молярным объемом пара ub (ua << ub). Пар при этом можно считать идеальным газом, так что P× ub = RT. Тогда уравнение (12.3) можно переписать в виде
 или
или  .
.
Интегрируя, получим  . Чтобы найти константу интегрирования, достаточно знать давление насыщенного пара Р 0при некоторой температуре Т 0. Тогда
. Чтобы найти константу интегрирования, достаточно знать давление насыщенного пара Р 0при некоторой температуре Т 0. Тогда  .
.
Окончательно получим  . (12.4)
. (12.4)
|
|
|


