 |
Кинетика гомогенных реакций
|
|
|
|
Скорость и равновесие
Химических реакций
Скорость химических реакций. Общие понятия.
Кинетика гомогенных реакций
Химические реакции очень сильно различаются по скорости. Одни из них протекают за доли секунды (реакции при взрыве), а другие – в течение многих лет (процессы в недрах Земли). Это связано с разным механизмом химических реакций. Раздел химии, который изучает скорость и механизм химических реакций, называется химической кинетикой.
При изучении кинетики химических реакций учитывают фазовый состав систем, в которых они протекают. По агрегатному состоянию реагентов различают газофазные, жидкофазные и твердофазные реакции. Реакции могут протекать в одной фазе или на границе фаз. Соответственно выделяют гомогенные и гетерогенные реакции.
Гомогенные химические реакции протекают в пределах одной фазы. Примерами гомогенных реакций могут быть любые реакции в смесях газов или в растворах.
Гетерогенные химические реакции протекают на границе раздела фаз. Например, реакции на границе твердое–газ, твердое–жидкое, твердое–твердое, жидкое–газ, жидкое–жидкое. Так, реакция растворения металла в кислоте является гетерогенной.
Знакомство с кинетикой химических реакций начнем с гомогенных реакций. В данном разделе будем рассматривать преимущественно химические реакции, протекающие в газовой фазе.
Одними из основных понятий кинетики химических реакций в газах и растворах являются их скорость и зависимость скорости от концентраций реагирующих веществ.
Скорость химической реакции (u) выражается изменением концентрации какого-либо из участвующих в ней веществ в единицу времени.
|
|
|
Допустим, задана реакция
Н2(г) + СО2(г) ® СО(г) + Н2О(г).
Вещества взаимосвязаны уравнением реакции. Поэтому скорость реакции можно измерить по изменению концентрации любого реагента, включая исходные вещества или продукты реакции. На рис. 7.1 схематически показано изменение концентраций исходных веществ и продуктов конкретной реакции. Концентрации обозначены химическими формулами веществ в квадратных скобках.
Допустим, скорость реакции выражается через изменение концентрации СО, D[CO], за интервал времени D t:

Величина  представляет собой среднюю скорость реакции за период времени D t.
представляет собой среднюю скорость реакции за период времени D t.
Поскольку зависимость [CO] от t не является прямолинейной, то таким путём можно определить только среднюю скорость для ограниченного интервала времени D t. Графически это означает, что кривую линию на некотором участке принимаем в качестве прямой, проводя касательную к точке а, расположенной на середине выбранного участка кривой. Если интервалD t ® 0, то получаем истинную скорость реакции в точке а, она выражается производной концентрации по времени:
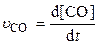
или


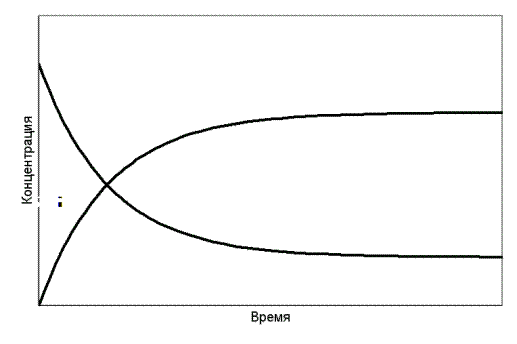
Рис. 7.1. Изменение концентраций реагентов и продуктов реакции
во времени(реагенты взяты в эквимолярных количествах)
Отрицательный знак в выражении для u H2необходим для сохранения положительного знака у скорости реакции в условиях, когда концентрация реагента уменьшается в ходе реакции. Таким образом, при одинаковом времени с начала реакции
 =
= 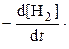
Однако такая зависимость выполняется, по меньшей мере, в том случае, когда в уравнении реакции эти вещества имеют равные коэффициенты, в соответствии с которыми они вступают во взаимодействие. Допустим, химическая реакция выражается в общем виде уравнением
А ® 2В.
В этом случае вероятно соотношение
 =
= 
Анализ приведенных зависимостей показывает, что скорость реакции зависит от концентраций реагирующих веществ. Именно градиент концентраций является движущей силой для химических реакций (рис. 7.1). Количественно эти зависимости определяются кинетическим уравнением.
|
|
|
Если химическую реакцию представить в общем виде уравнением
a А + в В® d D + c C,(7.1)
то кинетическое уравнение для неё имеет вид
u = k [A] n [B] m, (7.2)
где k – константа скорости реакции; [A] и [B] – концентрации реагентов;, n и m – коэффициенты, устанавливаемые экспериментальным путем, они определяют порядок реакции.
Коэффициенты n и m в общем случае не равны стехиометрическим коэффициентам реакции. Совпадение между ними встречается весьма редко. Порядок реакции определяется ее механизмом. Константа k равна скорости химической реакции при условии, что все концентрации или парциальные давления газов (для реакций в газовой фазе) равны единице. Можно подобрать также равным единице их произведение.
С учетом сказанного кинетическое уравнение выражает зависимость скорости реакции от концентраций реагентов, взятых в степенях, значения которых определяются механизмом реакции.
Приведенное кинетической уравнение (7.2) выражает зависимость скорости реакции от концентрации реагентов для гомогенных реакций. Реагенты гомогенных реакций находятся в одной фазе, т.е. все они газы или растворенные вещества. Гетерогенные реакции протекают на поверхности раздела между фазами реагентов, например на поверхности твердого тела, выступающего в качестве одного из реагентов, а другие реагенты находятся в газовой фазе или в растворе. Кинетическое уравнение гетерогенной реакции включает в себя площадь поверхности твердого тела S и концентрацию реагента в поверхностном слое сS.
Так, для реакции
a А(к) + в В(г)® c C(г),
кинетическое уравнение имеет вид
u = kScSn, (7.3)
где k – константа скорости гетерогенной реакции; n – порядок реакции по газообразному (или растворенному) компоненту.
Иным механизмам гетерогенных реакций соответствуют другие уравнения.
Температурная зависимость константы скорости. Проиллюстрируем ее конкретным примером.
П р и м е р.
Исследовали скорость разложения N2О5, растворенного в CCl4(ж), при различных температурах. При разложении идёт реакция
|
|
|
N2O5 ® 2NO2 + 1/2O2(г).
Получили следующие экспериментальные данные:
| Температура, ° С | Константа скорости, с -1 |
| 3,44×105 | |
| 13,5×105 | |
| 49,8×105 | |
| 150×105 |
О б щ и й в ы в о д: каждое повышение температуры на 10 ° С приводит к возрастанию величины k и соответственно u N2O5в 3–4 раза. Эту величину называют температурным коэффициентом скорости реакции.
Согласно правилу Вант-Гоффа
u2 = u1×g  , (7.4)
, (7.4)
где u1 = u2 – скорости реакции при температурах соответственно t 1 и t 2 (при t 2 > t 1); g – температурный коэффициент скорости реакции. Для большинства реакций g находится в интервале от 2 до 4.
Казалось бы, скорость реакции должна быть прямо пропорциональна числу соударений реагирующих частиц. Но в действительности эта зависимость имеет более сложный характер. Не каждое соударение частиц приводит к их взаимодействию. Эффективными являются лишь те соударения, при которых частицы благоприятно ориентированы относительно друг друга и имеют энергию, превышающую некоторый минимальный уровень.
Минимальная энергия, которая необходима частицам для их активного соударения, приводящего к взаимодействию, называется энергией активации.
Количественная зависимость константы скорости реакции от температуры выражается уравнением Аррениуса:
k = А е –Е а / RT, (7.5)
где R – универсальная газовая постоянная; А – предэкспонентный множитель; Т – абсолютная температура (К).
В логарифмической форме уравнение Аррениуса становится уравнением прямой линии:
ln k = ln A –  (7.6)
(7.6)
Наклон прямой, выражающей зависимость ln k от 1/ Т, равен – Е а / R, что позволяет вычислить величину Е а.
Комбинируя уравнения Аррениуса для двух температур: Т 1 и Т 2, можно привести их к форме, более удобной для практических расчетов:
 (7.7)
(7.7)
Пример 7.2. Для реакции Н2(г) + I2(г) ® 2HI(г) определены значения константы скорости при двух температурах: k 1 = 2,7×10–4 л × моль –1× с –1 при Т 1 = 600 К, k 2 = 9,9×10–3 л×моль –1× с –1 при Т 2 = 673 К. Вычислим энергию активации Еа и значение константы скорости реакции k 3 при Т 3 = 723 К.
|
|
|
Решение. Вычислим значение Еа, используя уравнение Аррениуса (7.7).

Вычислим значение k 3 при Т 3 = 723 К.
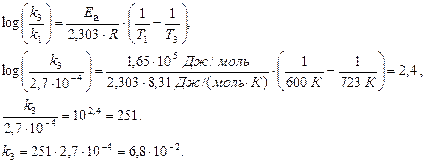
Ответ: Е а = 165 кДж/моль, k 723 = 6,8×10–2.
________________________________________________________________________
Химическое равновесие
Химические реакции подразделяют на необратимые и обратимые.
Необратимые реакции протекают только в одном направлении до полного взаимодействия взятых в стехиометрическом соотношении исходных веществ или до израсходования одного из реагирующих веществ, взятом в недостатке. Обычно в ходе необратимых реакций образуется малорастворимое соединение, которое выпадает в осадок, или малодиссоциирующее вещество, например Н2О, или выделяется продукт реакции в газообразном состоянии.
Примером может служить реакция нейтрализации сильного основания сильной кислотой:
NaOH(р) + HCl(р) ® NaCl(р) + H2O(ж).
Такую реакцию нельзя провести в обратном направлении без использования новых реагентов и без затрат энергии.
Однако известно множество обратимых реакций.
Обратимые реакции проявляют способность одновременно протекать в двух взаимно противоположных направлениях, т.е. в прямом и в обратном согласно
уравнению.*
Возвратимся к рис. 7.1. Обратим внимание на ход зависимостей при больших значениях времени прохождения реакции. Концентрации реагентов и продуктов реакции становятся постоянными. Наступает химическое равновесие.
Природа химического равновесия требует специального обсуждения. Но первые представления о равновесном состоянии системы даёт сопоставление скоростей прямой и обратной реакций.
Ещё раз обратимся к уравнению реакции
Н2О(г) + СО(г) ® Н2(г) + СО2(г).
Сразу же после смешения реагентов начинается реакция. Скорость реакции в начальный момент времени максимальная, а затем понижается по мере уменьшения концентрации исходных веществ. Концентрация же продуктов реакции в начальный момент времени нулевая. Затем их концентрация начинает повышаться, что приводит к взаимодействию между ними, т.е. к реакции в обратном направлении.
Н2(г) + СО2(г) ® Н2О(г) + СО(г).
Скорость обратной реакции постепенно возрастает. В конечном итоге скорости прямой и обратной реакций становятся равными и наступает химическое равновесие. Изменение скоростей прямой и обратной реакции во времени схематически показано на рис. 7.7.
Следовательно, химическое равновесие – это состояние, которое достигает реакционная смесь, когда скорости прямой и обратной реакций становятся равными.
Состояние химического равновесия обозначают в уравнении химической реакции знаком  между реагентами и продуктами:
между реагентами и продуктами:
|
|
|
Н2О(г) + СО(г)  Н2(г) + СО2(г).
Н2(г) + СО2(г).
Химическое равновесие имеет динамический характер. Прямая и обратная реакции при равновесии не прекращаются, но идут с равными скоростями, что сохраняет на постоянном уровне концентрации реагентов и продуктов.

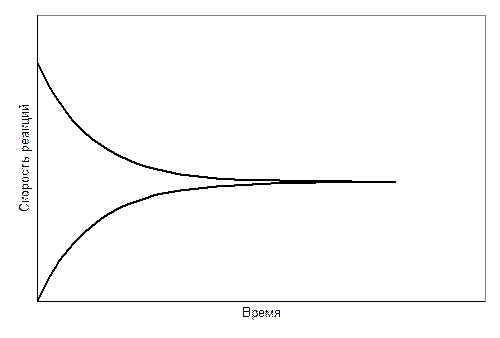
Рис. 7.7. Изменение скоростей прямой ( u пр ) и обратной ( u обр ) реакций
Норвежские исследователи К. Гульдберг и П. Вааге в 1864 г. сформулировали закон действующих масс, который даёт общее описание условий равновесия. Под термином «действующие массы» авторы закона понимали «концентрации».
Рассмотрим закон действующих масс на примере реакции
a А + в В  с С + d D. (7.18)
с С + d D. (7.18)
Допустим, что стехиометрические коэффициенты в уравнении реакции равны порядкам реакции по соответствующим веществам, тогда уравнения скорости прямой и обратной реакции будут иметь вид
u пр= k 1×[A] a ×[B] b; u обр= k– 1[C] c ×[D] d,
k 1и k –1– константы скорости прямой и обратной реакции соответственно.
В условиях химического равновесия
u пр= u обр и k 1×[A] a ×[B] b = k– 1[C] c ×[D] d.
Соответственно приходим к выражению константы равновесия
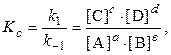 (7.19)
(7.19)
где Kс – концентрационная константа равновесия, т.к. она выражена через равновесные концентрации реагирующих веществ; подстрочный индекс с образован от англ. concentration.
Полученное выражение показывает также, что константа равновесия равна отношению констант скоростей прямой и обратной реакций.
Для состояния равновесия порядок реакций не имеет значения. Несмотря на то, совпадают ли стехиометрические коэффициенты с порядком реакции или нет, в выражении константы равновесия концентрации веществ приводятся в степенях, равных стехиометрическим коэффициентам.
Таким образом, константа равновесия равна отношению, в числитель которого входит произведение равновесных концентраций продуктов реакции, а в знаменатель – произведение концентраций исходных веществ, при этом все значения концентраций берутся в степенях, равных стехиометрическим коэффициентам в уравнении реакции.
С учетом введенных понятий возвратимся к обсуждению закона действующих масс.
Закон действующих масс утверждает, что константа равновесия реакции есть величина постоянная при определенной температуре и не изменяется, если в её выражение подставляются любые равновесные концентрации реагирующих веществ.
Смешивая реагенты, можно задать любое их соотношение и любые концентрации. Соответственно равновесные концентрации веществ также будут разные. Но отношение, выражающее константу равновесия, для данной реакции останется постоянным (при постоянной температуре).
Физические состояния веществ при химических реакциях могут быть самые разнообразные. Если все реагирующие вещества находятся в одной фазе, например все они газы или все растворенные вещества, то такие системы относятся к гомогенным.
Равновесие в гомогенных системах называют гомогенным равновесием.
Выражение константы гомогенного равновесия записывают именно так, как было рекомендовано ранее (уравнения (7.18) и (7.19)).
П р и м е р: для реакции
Н2(г) + СО2(г)  Н2О(г) + СО(г)
Н2О(г) + СО(г)
выражение константы равновесия записывается следующим образом:
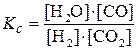 ,
,
для реакции
N2(г) + 3Н2(г)  2NH3(г)
2NH3(г)
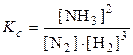 ,
,
для реакции
Ag+(р) + 2NH3(р)  [Ag(NH3)2]+ (р)
[Ag(NH3)2]+ (р)

В том случае, когда реагирующие вещества образуют более чем одну фазу, устанавливается гетерогенное равновесие.
Так, в реакции
СО2(г) + С(к)  2СО(г)
2СО(г)
С – углерод (графит) – находится в твердом состоянии, а остальные вещества – в газообразном. Уравнение выражает гетерогенное равновесие. Концентрация графита, как чистого вещества, остаётся в объеме твердого тела постоянной вплоть до его полного израсходования в химической реакции. Как постоянную её целесообразно включить непосредственно в величину Kс. Отсюда выражение константы гетерогенного равновесия для данной реакции имеет вид

Так же поступают при описании гетерогенных равновесий в водных растворах. При этом не имеет значения, является ли твердое вещество исходным веществом или продуктом реакции.
П р и м е р ы:
AgCl(к) + 2NH3(р)  [Ag(NH3)2]+ (р) + Cl–(р),
[Ag(NH3)2]+ (р) + Cl–(р),
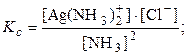
Ba2+(р) + SO42–(р)  BaSO4(к),
BaSO4(к), 
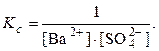
При протекании химических реакций в водных растворах вода нередко является одним из реагирующих веществ. Обычно вода как растворитель находится в большом избытке по отношению к другим реагирующим веществам. В этих условиях изменением концентрации воды в растворе при прохождении химической реакции можно пренебречь. Если принять концентрацию воды постоянной, то её целесообразно включить в величину Kс.
С учетом сказанного для реакции
NH3(р) + H2O(ж)  NH4+(р) + OH–(р)
NH4+(р) + OH–(р)
константа равновесия

Концентрация воды не входит в выражение константы равновесия.
Представление о состоянии химического равновесия и понятие константы равновесия играют исключительно важную роль в химии. Если фактическое отношение концентраций продуктов реакции и исходных веществ в их смеси (Qс) не равно константе равновесия (Kс), то между веществами может произойти взаимодействие (т.е. химическая реакция в прямом или обратном направлении), которое будет продолжаться до тех пор, пока не наступит состояние химического равновесия. Равновесие – это предел, до которого может идти химическая реакция. Если оказалось так, что концентрации продуктов и исходных веществ в смеси изначально соответствуют их равновесным значениям, то в системе сразу же установится состояние динамического равновесия, при котором скорости прямой и обратной реакций будут равны друг другу.
Значения констант равновесия используют также при вычислении равновесных концентраций реагирующих веществ. Поскольку состояние равновесия – предел для прохождения реакции, то равновесные концентрации продуктов реакции характеризуют предельный выход реакции.
Рассмотрим некоторые простые примеры расчетов, связанные с химическим равновесием.
Пример 7.4. Рассмотрим химическую реакцию
Н2(г) + СО2(г)  Н2О(г) + СО(г).
Н2О(г) + СО(г).
При 1120 ° С установилось равновесие реакционной смеси. Значения равновесных концентраций веществ следующие:
[H2] = 0,01 M, [CO2] = 0,01 M, [CO] = 0,01 M, [H2O] = 0,02 M.
Вычислим величину Kс.
Решение. Система гомогенная. Составим выражение константы равновесия, подставим в него известные величины и произведём вычисление.
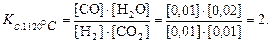
Комментарий. Bысокие значения Kс свидетельствуют о том, что равновесие реакционной смеси устанавливается при избытке продуктов по сравнению с реагентами и, следовательно, реакция более полно идёт в прямом направлении. Именно при высоких значениях Kс числитель отношения больше знаменателя.
В данном примере Kс = 2, т.е. величина небольшая, но в условиях равновесия при 1120 ° С некоторый избыток продуктов реакции по сравнению с исходными веществами достигается. При другой температуре результат может быть иным, т.к. Kс будет иметь другое значение.
Пример 7.5. Рассмотрим реакцию
Fe(к) + Cu2+(р)  Cu(к) + Fe2+(р).
Cu(к) + Fe2+(р).
Для неё известна величина Kс,25° С = 3×1026. Определим, пойдет ли реакция, если исходные концентрации следующие: [Cu2+] = 1×10–10 M и [Fe2+] = 0,1 M.
Решение. Вычислим величину Qс и сравним её с величиной Kс.

Вывод: Qс < Kс, и реакция пойдет в прямом направлении.
Комментарий. Если величина Qc < Kc, то концентрации продуктов реакции (числитель отношения) ниже, чем в равновесном состоянии, а концентрации исходных веществ (знаменатель отношения), наоборот, выше. Следовательно, для достижения равновесия реакционной смеси реакция должна идти в прямом направлении.
_______________________________________________________
Соотношение величин Qc и Kc определяет направление химических реакций, что позволяет сформулировать вывод в общей форме:
если Qc < Kc, то реакция идет в прямом направлении;
если Qc > Kc, то реакция идет в обратном направлении;
если Qc = Kc, то реакционная смесь находится в состоянии химического равновесия.
Величина Kc характеризует полноту прохождения химической реакции до достижения ею химического равновесия. Если Kc не очень сильно отличается от единицы, то химическое равновесие устанавливается при низком выходе продуктов реакции. Для повышения их выхода приходится целенаправленно изменять условия: концентрации веществ, давление, температуру. Выбор этих условий проводится в соответствии с принципом Ле Шателье.
Общая формулировка принципа Ле Шателье следующая: если на систему, находящуюся в состоянии химического равновесия, воздействовать извне, изменяя какой-либо из параметров (концентрацию, давление или температуру), определяющих положение равновесия, то в системе усилится то из направлений процесса, которое ослабляет влияние произведенного воздействия. Положение равновесия также сместится в направлении ослабления эффекта внешнего воздействия.
Далее рассмотрим на конкретных примерах применение принципа Ле Шателье для определения направления сдвига химического равновесия.
Роль концентрации веществ можно проанализировать, руководствуясь соотношением между Qc и Kc.
Рассмотрим реакцию
N2(г) + 3H2(г)  2NH3(г).
2NH3(г).
Для нее концентрационная константа равновесия

Поскольку Kc < 1, то при химическом равновесии концентрации исходных веществ выше, чем продуктов реакции.
Введем в равновесную смесь реагирующих веществ дополнительное количество N2. Исходя из выражения
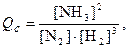
следует ожидать уменьшения величины Qc по сравнению с Kс. При Qc < Kс реакция пойдет в прямом направлении, т.к. необходимо понизить концентрацию исходных веществ (знаменатель отношения) и повысить концентрацию продуктов реакции (числитель отношения). Реакция прекращается, когда будет достигнуто новое состояние химического равновесия. Переход от одного состояния химического равновесия к другому интерпретируется как сдвиг химического равновесия.
Если в систему ввести дополнительно NH3, т.е. продукт реакции, то устанавливается соотношение Qc > Kс и химическое равновесие сдвигается в сторону обратной реакции.
Пример 7.6. Рассмотрим химическое равновесие
N2(г) + 3H2(г)  2NH3(г).
2NH3(г).
Определим равновесные концентрации NH3 для двух равновесных смесей:
1. [N2] = 0,1 M и [H2] = 0,1 M.
2. [N2] = 1,0 М и [H2] = 0,1 M.
Во втором варианте концентрация N2 в равновесной смеси увеличена. Kс = 6,0×10‑2 при 525 ° С.
Решение. Составим выражение для Kс, подставим в него известные величины, и произведем вычисления.
Первый вариант химического равновесия:
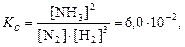
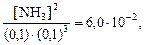 откуда [NH3] = 2,4×10‑3 М.
откуда [NH3] = 2,4×10‑3 М.
Второй вариант химического равновесия:
 откуда [NH3] = 7,7×10–2 М.
откуда [NH3] = 7,7×10–2 М.
Вывод. При увеличении в равновесной смеси концентрации N2 (реагента) повышается концентрация NH3 (продукта реакции).
__________________________________________
Роль давления. Влияние давления на химическое равновесие может проявляться в том случае, когда хотя бы один из участников реакции является газообразным веществом. Конечно, сказанное относится и к системам, где весь набор реагирующих веществ – газы. Для веществ в конденсированном состоянии (жидкости, твердые вещества) влиянием давления пренебрегают.
Изменение давления можно связать с изменением концентрации вещества. Согласно законам идеальных газов (раздел 8.2) соблюдается пропорциональность
P µ  µ
µ  ,
,
где Р – давление газа; V – объем газа; n – число молей газа; µ – знак пропорциональности.
Применим эти зависимости для предсказания направления сдвига химического равновесия под влиянием изменения давления при синтезе аммиака:
N2(г) + 3H2(г)  2NH3(г).
2NH3(г).
При сжатии реакционной смеси газов в 10 раз (например в сосуде с поршнем) её объем уменьшается в 10 раз, а давление возрастает во столько же раз. Отразим эти изменения в выражении Qc.
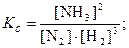
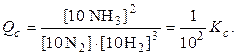
Ранее было показано, что в условиях, когда Qc < Kс, концентрация исходных веществ выше равновесной и химическое равновесие сдвигается в направлении прямой реакции. Направление сдвига равновесия при изменении общего давления зависит от соотношения числа молей газов в левой и правой частях уравнения. Так, в уравнении реакции синтеза аммиака 4 моль газов в левой части и 2 моль в правой части. При увеличении общего давления равновесие сдвигается в сторону меньшего числа молей газов. В других реакциях может быть иной порядок распределения молей газов в уравнении и будет другой результат влияния давления на сдвиг химического равновесия. Например, в уравнении реакции
2C(к) + O2(г)  2CO(г)
2CO(г)
1 моль газа в левой части и 2 моль в правой части. Нетрудно показать, что повышение общего давления в этом случае приведёт к соотношению Qc > Kс и химическое равновесие сдвинется в сторону обратной реакции.
Если в уравнении химической реакции число молей газов одинаково в обеих частях, то изменение давления не скажется на состоянии химического равновесия.
П р и м е р такой ситуации:
N2(г)+ О2(г)  2NО(г).
2NО(г).
Если все реагирующие вещества находятся в конденсированном состоянии, то изменение давления также не скажется на составе реакционной смеси.
Упрощенно можно сказать, что увеличение общего давления приводит к сдвигу химического равновесия в том направлении по уравнению реакции, где меньше молей газообразных веществ. Таким путём система при уменьшении своего объема стремится ограничиться меньшим количеством газа. При уменьшении общего давления обнаруживается противоположный эффект.
Температура широко используется для управления скоростью реакций и химическим равновесием. Прежде всего, достигается повышение скорости реакций с увеличением температуры, что сокращает время, необходимое для достижения химического равновесия. Далее, температура влияет на величину константы равновесия. Принцип Ле Шателье позволяет предсказывать направление сдвига равновесия в зависимости от знака теплового эффекта реакции.
Если в результате реакции происходит выделение теплоты q, то реакцию называют экзотермической, а если при реакции идет поглощение теплоты, то её называют эндотермической.
Согласно принципу Ле Шателье, при повышении температуры химическое равновесие сдвигается в сторону той реакции, прямой или обратной, которая происходит с поглощением теплоты, т.е. в сторону эндотермической реакции, а при понижении температуры – в сторону экзотермической реакции.
Так, реакция синтеза аммиака является экзотермической:
N2(г) + 3H2(г)  2NH3(г), + q.
2NH3(г), + q.
Поэтому повышение температуры приведёт к сдвигу равновесия в сторону обратной реакции, которая будет эндотермической.
Несмотря на отрицательное влияние температуры на полноту прохождения экзотермической реакции, синтез аммиака производят при температурах около 450 ° С. Именно при этой температуре лучше работает катализатор.
* Существует различие понятий «химически обратимые реакции» и «термодинамически обратимые реакции» (раздел 6.1).
|
|
|


