 |
Характеристики отдельных видов топлива
|
|
|
|
Глава 1. Энергетические ресурсы
Основные понятия и сведения
Энергетические ресурсы - это материальные объекты, в которых сосредоточена возможная для практического использования человеком энергия. Энергоресурсы подразделяются на:
-возобновляемые и невозобновляемые;
- топливные и нетопливные;
- природные (первичные) и искусственные (вторичные).
Существуют 4 основных критерия энергетических ресурсов:
- объём запасов;
- энергоёмкость;
- стоимость добычи и транспортировки;
- влияние технологии использования ресурсов на экологию.
Представление о природных ресурсах энергии и их величинах можно получить, исходя из следующих данных, с учетом, что ежегодное мировое потребление энергоресурсов  :
:
а) невозобновляемые ресурсы (общие запасы):
| Ресурсы | 
| Относительные единицы |
| Термоядерная энергия | 
| ~200 |
| Ядерная энергия деления | 
| ~10 |
| Химическая энергия органического топлива | 
| |
| Внутреннее тепло Земли | 
| ~0,0025 |
б) ежегодно возобновляемые ресурсы:
| Ресурсы | 
| Относительные единицы |
| Энергия солнца | 
| ~10 |
| Энергия морских приливов | 
| ~1,2 |
| Энергия ветра | 
| ~0,3 |
| Энергия рек | 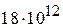
| ~0,0003 |
в) соотношение между различными категориями запасов органического топлива:
| Категория запасов | Время полного использования | Относительные единицы |
| Геологические запасы | 500-1000 лет | |
| Разведанные запасы | 100-200 лет | 0,5 |
| Готовые к использованию в современных условиях | 50-100 лет | 0,25 |
Около 90% используемых в настоящее время энергоресурсов составляют невозобновляемые (уголь, нефть, природный газ, уран и т.п.) благодаря их относительно высокому энергетическому потенциалу, относительной доступности и целесообразности добычи.
|
|
|
Для характеристики степени использования энергетических ресурсов (ЭР) в технологических процессах и установках применяется энергетический КПД технологического процесса (%):
 , ,
|
где 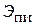 – количество полезно использованной энергии;
– количество полезно использованной энергии;  – количество подведенной энергии к данной установке. Энергетический КПД данного технологического процесса, называемый также коэффициентом топливоиспользования, определяется в общем случае из выражения:
– количество подведенной энергии к данной установке. Энергетический КПД данного технологического процесса, называемый также коэффициентом топливоиспользования, определяется в общем случае из выражения:
 , ,
|
где  – КПД добычи, транспорта и переработки топлива;
– КПД добычи, транспорта и переработки топлива; 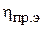 – КПД производства энергии (тепловая и электрическая энергия);
– КПД производства энергии (тепловая и электрическая энергия);  – КПД транспорта энергии;
– КПД транспорта энергии;  – КПД приводов механизмов;
– КПД приводов механизмов;  – КПД рабочей машины, технологического агрегата.
– КПД рабочей машины, технологического агрегата.
Суммарный КПД использования ЭР составляет 30-50%. Остальные 50-70% - это потери, в том числе в процессах, в %:
- добыча, транспорт и переработка топлива……… 3-5;
- генерирование энергии ………………………….15-21;
- распределение энергии…………………………… 2-4;
- использование энергии………………………… 30-40.
По возможности устранения потерь они могут быть классифицированы на неизбежные (или собственные) и технические.
Под неизбежными потерями понимаются такие, которые при данном принципе организации процесса не могут быть устранены или снижены без радикального изменения самого процесса. Потери, уменьшение или устранение которых технически возможно при данном принципе организации процесса, относятся к техническим.
На повышение КПД влияет снижение потерь во всех элементах цепи технологического процесса и особенно при генерировании и использовании энергии. Важным направлением повышения КПД является регенерация энергии, а также более полное использование вторичных энергетических ресурсов (ВЭР).
Для определения КПД по приведенному выражению используются энергобалансы технологических процессов и установок. Эти балансы дают наглядную картину количественного расхода энергоресурсов для процессов, где применяется один вид энергоносителя. В промышленности (химия, металлургия, энергетика и т.д.) широко распространены технологические процессы и установки, в которых одновременно используются энергоносители нескольких видов. В этом случае необходим также учет качественного различия разных видов энергоресурсов.
|
|
|
Согласно второму закону термодинамики существует два класса видов энергии: виды, способность которых к преобразованию не ограничена, и виды, преобразуемые из одного вида в другой только в ограниченной мере. Следовательно, любой вид энергии можно представить в виде двух составляющих: энергии, которая при заданных свойствах окружающей среды может быть преобразована в любой другой вид энергии и энергии, преобразование которой в данных условиях в другие виды невозможно. Первая составляющая энергии называется эксергией, вторая – анергией, при этом каждая из этих составляющих в данном виде энергии может равняться нулю.
К неограниченно преобразуемым относятся механические виды энергии и электрическая энергии, т.е. они полностью состоят из эксергии. Ограниченно превратимыми являются внутренняя и тепловая энергии, которые состоят из двух составляющих – эксергии и анергии.
Например, подведенное к тепловому двигателю тепло полностью преобразовать в механическую работу невозможно, поскольку тепло лишь частично состоит из эксергии. Причем величина доли эксергии в тепловой энергии существенно зависит от свойств окружающей среды. КПД, определяемый формулой  , оценивает эффективность теплосиловой установки несовершенно, т.к. сравнивает достигнутое,
, оценивает эффективность теплосиловой установки несовершенно, т.к. сравнивает достигнутое, 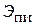 , не с эксергией подведенного тепла, а с теплом, полное преобразование которого не может быть достигнуто.
, не с эксергией подведенного тепла, а с теплом, полное преобразование которого не может быть достигнуто.
Поэтому целесообразнее оценивать совершенство теплосиловых установок по эксергическому КПД:
 ,
,
где  – величина затраченной эксергии;
– величина затраченной эксергии;  – потери эксергии;
– потери эксергии;  – затраты энергии при идеальном ведении технологического процесса.
– затраты энергии при идеальном ведении технологического процесса.
Например, КПД простой паросиловой установки составляет ~ 35%, в то время как эксергический КПД ~ 75%.
Отклонение эксергического КПД от единицы служит мерой принципиально устранимых потерь эксергии, уменьшение которых возможно при более рациональном проведении процессов и использовании более совершенного оборудования
|
|
|
Таким образом, определение потерь эксергии в различных звеньях любого технологического процесса или установки позволяет выявить и количественно оценить причины низкого уровня энергоиспользования и дать информацию о возможностях повышения КПД этих процессов или установок.
Оценивая эффективность тех или иных ЭР с помощью энергетического или эксергического КПД, необходимо иметь ввиду, что невозможно добыть и использовать все 100% ЭР, имеющегося в данном месторождении. Коэффициент извлечения зависит от вида топлива, характера месторождения и техники добычи: для нефти он равен 0,3-0,4, для природного газа – 0,5-0,8, для угля – 0,25-0,5.
Наконец, что касается общей структуры мирового потребления энергетических ресурсов:
| Ресурс | 1980 г. | 2000 г. | 2020 г. |
| Уголь | 25% | 25% | 30% |
| Нефть | 45% | 35% | 25% |
| Природный газ | 14% | 14% | 10% |
| Возобновляемые ресурсы | 13% | 15% | 20% |
| Ядерная энергия | 3% | 11% | 15% |
§2. Классификация, состав и основные технические характеристики топливных невозобновляемых ресурсов
Топливные ресурсы, или топливо - это горючие вещества, выделяющие при сжигании значительное количество теплоты, которая используется непосредственно в технологических процессах или преобразуется в другие виды энергии и не даёт вредных продуктов сгорания. К ним относятся полезные ископаемые органического происхождения – уголь, горючие газы, горючие сланцы, нефть, торф, а также древесина и растительные отходы.
В ядерной энергетике применяется понятие ядерного топлива - вещества, ядра которого делятся под действием нейтронов, выделяя при этом энергию в основном в виде кинетической энергии осколков деления ядер и нейтронов.
В зависимости от агрегатного состояния органическое топливо делится на:
1) газообразное;
2) жидкое;
3) твёрдое.
Каждое из них в свою очередь делится на:
1) естественное (природное) – добытое в недрах Земли и
|
|
|
2) искусственное (переработанное природное).
Доля органического топлива в балансе мировой энергетики составляет около 65 %, из которых 39 % приходится на уголь, 16 % на природный газ, 9 % на жидкое топливо.
Для анализа тепловых характеристик топлив, определения состава газов и других расчетов необходимо знать химическую структуру каждого вида топлива. Органическая часть твердых и жидких топлив состоит из большого количества сложных химических соединений, в состав которых в основном входят пять химических элементов: углерод С, водород Н, кислород О, сера S и азот N. Кроме того, топливо содержит минеральные примеси А и влагу W, представляющие вместе внешний балласт топлива.
Химический состав твердых, жидких и газообразных топлив определяют не по количеству соединений, а по суммарной массе химических элементов (в процентах на 1 кг или 1 куб. м топлива), т.е. устанавливают элементарный состав топлива. Различают три основных элементарных состава топлива:
1) рабочая масса топлива C + H + O + N + S + A + W =100%;
2) сухая масса топлива C + H + O + N + S+A =100%;
3) горючая масса топлива C + H + O + N =100%.
 Рабочей считается масса топлива в том виде, в каком она поступает на предприятие.
Рабочей считается масса топлива в том виде, в каком она поступает на предприятие.
Если топливо нагреть до 102-105ºС, то испарится влага, тогда получится сухая масса топлива. Название горючей массы является условным, так как входящие в его состав азот и кислород не являются горючими элементами и составляют внутренний балласт топлива. Азот и кислород способствуют процессу горения топлива.
Горючими элементами топлива являются углерод, водород и сера. Углерод – основной, горючий элемент топлива. Он имеет высокую теплоту сгорания (33600 кДж/кг) и составляет большую часть рабочей массы топлива (50-75% для твердых топлив и 80-85% для мазутов). Водород имеет более высокую теплоту сгорания чем углерод (примерно 130000 кДж/кг), однако его количество в твердых топливах невелико (2-6%) и несколько больше в жидких (около 10%). Это делает теплоту сгорания жидких топлив выше, чем твердых.
Сера имеет невысокую теплоту сгорания (9000 кДж/кг). Содержание ее в топливах невелико (0,2-4%), поэтому сера, как горючая составляющая, не ценится.
Наличие окислов серы в продуктах сгорания при определенных концентрациях опасно для организмов и растений и требует определенных мер и средств для ее улавливания.
Основными техническими характеристиками топлива являются:
1) теплота сгорания;
2) выход газообразных веществ при нагреве;
3) зольность топлива;
4) свойства зольного остатка;
5) влажность топлива;
6) сернистость топлива.
Теплота сгоранияявляется основной характеристикой топлива. Это количество тепловой энергии, которая может выделиться в ходе химических реакций окисления горючих компонентов топлива с газообразным кислородом, измеряется в кДж/кг для твердого и жидкого, и в кДж/м3 для газообразного топлив. Различают высшую и низшую теплоту сгорания. Высшей теплотой сгорания  называют количество тепла, которое выделяется при сгорании 1 кг твердого (жидкого) или 1 куб. м газообразного топлива. Низшая теплота сгорания
называют количество тепла, которое выделяется при сгорании 1 кг твердого (жидкого) или 1 куб. м газообразного топлива. Низшая теплота сгорания  отличается от высшей на теплоту испарения влаги и влаги, образующейся при горении водорода. Чем больше влажность топлив, тем меньше будет величина
отличается от высшей на теплоту испарения влаги и влаги, образующейся при горении водорода. Чем больше влажность топлив, тем меньше будет величина  .
.
|
|
|
Высшая величина сгорания твердого и жидкого топлива определяется экспериментально. Низшая теплота сгорания положена в основу классификации топлив.
Для сравнения различных видов топлива их приводят к единому эквиваленту – условному топливу, имеющему теплоту сгорания 29308 кДж/кг. Для пересчета реального топлива в условное, используется тепловой эквивалент:  .
.
Выход летучих веществ.Если сухую массу топлива поместить в тигель и постепенно нагревать в инертной среде без доступа воздуха, то будет происходить уменьшение ее массы. При высоких температурах начинается разложение кислородосодержащих молекул топлива с образованием газообразных продуктов, получивших название летучих веществ. Выход летучих веществ из твердых топлив происходит в интервале температур от 110 до 1100ºС.
Выход летучих веществ определяет температуру воспламенения топлива и условия его хранения, сильно влияет на конструкцию топок, где сжигается это топливо.
Чем больше выход летучих веществ, тем легче воспламеняется топливо (газообразные, летучие вещества имеют низкую температуру воспламенения).
Зольность топлива.В процессе горения топлива его минеральная часть подвергается химическим преобразованиям. Масса несгораемого остатка – золы оказывается на 10-15% меньше, чем масса исходной минеральной части топлива и существенно отличается от нее по составу. Свойства золы играют большую роль при сжигании топлива.
Образовавшаяся после сгорания топлива зола – это смесь минералов, а их сплавы, возникающие в зоне высоких температур, называют шлаками. Суммарное количество золы и шлаков принято называть зольностью топлива.
Влажность топлива.Влажность топлива (W) в процентах от его рабочей массы определяется опытным путем его сушки при температуре 105ºС до достижения постоянства массы.
Большая влажность топлива вызывает трудности при сжигании. Снижается теплота сгорания, растет расход топлива, увеличиваются потери тепла с уходящими газами. Влажность топлива вызывает усиление коррозии металла отдельных конструкций топок, приводит к повышенному загрязнению поверхностей нагрева.
Сернистость топлива. При сжигании сера создает серьезные экологические проблемы. Окислы серы и азота, образующиеся в зоне высоких температур, представляют большую опасность для жизнедеятельности. Для улавливания этих окислов строят сложные очистные сооружения, что приводит к удорожанию примерно вдвое энергетических установок.
К природному твёрдому топливу относятся:
1) древесина;
2) торф;
3) бурый уголь;
4) каменный уголь;
5) антрацит;
6) горючие сланцы.
К искусственному твёрдому топливу относят:
1) кокс;
2) угольную пыль и угольные брикеты.
К природному жидкому топливу относится нефть.
Ко вторичному жидкому топливу "принадлежат" продукты переработки нефти:
1) бензин,
2) керосин,
3) мазут,
4) дизельное топливо.
Природное газообразное топливо- природный газ (сухой газ) и попутный газ.
Искусственное газообразное топливо может быть получено в ряде технологических процессов переработки твёрдых и жидких топлив:
1) генераторный газ;
2) коксовый газ;
3) доменный газ;
4) продукты перегонки нефти;
5) водород.
Ядерное (расщепляющееся) топливо – природный изотоп урана 235  и искусственно получаемый изотоп плутония 239
и искусственно получаемый изотоп плутония 239  .
.
Ядерным топливом для термоядерной реакции являются изотопы водорода – дейтерий и тритий.
Твёрдое органическое топливо используется в основном на тепловых электростанциях, для отопления и технологических нужд промышленности, а также, в незначительной степени, для судовых и локомотивных двигателей. До 70% и более жидких топлив сжигается на транспорте - авиация, автомобили, тракторы, суда, а в последние годы всё больше и на железнодорожном транспорте; менее 30% - в виде мазута на тепловых электростанциях. Наконец, газообразное топливо применяется на ТЭС, для технологических нужд промышленности и для отопления в быту (плюс в незначительных количествах на транспорте).
Жидкое и газообразное органические топлива имеют ряд преимуществ перед твёрдым:
1) добыча их (особенно газа) и транспортировка обходятся гораздо дешевле;
2) теплота сгорания выше;
3) перемешивание с окислителем (смесеобразование) проще и совершеннее, т.е. совершеннее и процесс горения;
4) продукты сгорания не содержат твёрдых и жидких (например, смолы) составляющих, что исключает износ или засорение элементов генераторов полезной энергии.
Характеристики отдельных видов топлива
Средняя удельная теплота сгорания основных видов топлива (в кДж/кг(м3)):
| Углерод | Бензин | ||
| Водород | Керосин | ||
| Древесина | Диз.топливо | ||
| Торф | Мазут | ||
| Бурый уголь | Сжиженный газ | ||
| Каменный уголь | Природный газ | 28000-46000 | |
| Антрацит | Попутные газы | ||
| Кокс | Сланцевый газ | ||
| Сланцы | Изотопы урана | 8  109 109
|
Характеристики видов топлива находятся в зависимости от химического возраста этих топлив.
Торф.Самый молодой вид топлива. Энергетические установки сжигают преимущественно фрезерный торф, получаемый путем срезания с поверхности тонкого слоя фрезами. Фрезерный торф имеет высокую влажность рабочей массы (W до 50% и более) и в связи с этим низкую теплоту сгорания Q = 8500 кДж/кг. Как молодое топливо торф обладает большим выходом летучих веществ (V = 70%), что позволяет успешно его сжигать в пылевидном состоянии. Из-за большой влажности и низкой теплотворности его не перевозят на расстояния более 100 км. Торф используют как местное сырье.
Бурые угли по содержанию влаги в рабочей массе делятся на сильно влажные, повышенно влажные, влажные. Кроме большой влажности, бурые угли имеют высокую зольность и невысокую теплоту сгорания (Q = 6,7-17000 кДж/кг), поэтому дальние перевозки также нецелесообразны. Большой выход летучих веществ обеспечивает высокоэкономичное сжигание этих углей в виде подсушенной пыли.
Каменные углиобъединяют большое количество углей различного химического возраста. Молодые каменные угли по выходу летучих веществ, близки к бурым углям, но имеют меньшую влажность и зольность. Это увеличивает их теплоту сгорания (Q = 19000-27000 кДж/кг). Средняя, по возрасту группа углей отличается повышенной зольностью. Их теплота сгорания ниже, чем у молодых углей. Более старые угли имеют малую влажность, невысокую зольность и соответственно высокую теплотворную способность (Q = 25000-27000 кДж/кг), однако низкий выход летучих веществ затрудняет их воспламенение в топках.
Полуантрациты и антрациты – это наиболее старые угли с низким выходом летучих веществ, низкой влажностью и зольностью. Также являются хорошим сырьем для металлургической промышленности.
Горючие сланцы. Благодаря большому содержанию водорода сланцы являются ценным сырьём для производства газа и жидкого топлива.
Нефть. В состав нефти входят: углерод - 80%, водород - 15% и кислород с серой - 5%. При первичной добыче добывается только 20% всей нефти (под действием естественного давления), после вторичной - 50-60% (с помощью закачки воды под слой нефти или нагнетания газа выше уровня нефти) и третичной - 90% (при закачке азота или водяного пара). Высокая удельная теплота сгорания, отсутствие балласта, лёгкая транспортировка - всё это присуще нефти. Нефть обычно не сжигается как топливо, а идёт на переработку для получения искусственных видов топлива и других продуктов для химической промышленности.
Бензин— горючая смесь лёгких углеводородов с температурой кипения от 30 до 200 °C. Плотность около 0,75 г/см³. Температура замерзания ниже −60 °C в случае использования специальных присадок.
Бензин получают путем возгонки и отбора фракций нефти, выкипающих в определенных температурных пределах; до 100 °C — бензин I сорта, до 110 °C — бензин специальный, до 130 °C — бензин II сорта, до 270 °C — керосинобыкновенный, примерно до 300 °C — производится отбор масляных фракций. Остаток считается мазутом.
Так как запасы нефти ограничены, а некоторым потребителям необходимо только жидкое топливо, получаемое в результате переработки нефти, то большое значение приобрёл вопрос о получении жидкого искусственного топлива - керосина, бензина - из угля, ресурсов которого гораздо больше. В настоящее время имеются 4 основных способа переработки угля в жидкое топливо:
- синтез, в основе которого лежит превращение под давлением угля в смесь горючих газов с использованием при этом водяного пара, воздуха или кислорода;
- экстракция, т.е. термическое растворение угля, причём в качестве растворителей используются вещества, участвующие в процессах дальнейшей переработки угля;
- гидрирование (гидрогенизация) - способ, заключающийся в насыщении угля водородом и взаимодействии угля с содержащими водород веществами при высоких температуре и давлении;
- пиролиз - нагрев угля в отсутствии окислителя.
Ни один из названных способов не имеет явного преимущества над другими, и каждый из них заслуживает дальнейшей разработки.
Естественные горючие газы подразделяется на газы природные и газы нефтяные попутные.
Месторождения, содержащие только природное газовое топливо, в зависимости от состава последнего делятся на чисто газовые и газоконденсатные.
Природные газы преимущественно содержат метан и его гомологи (этан, пропан, бутан и другие). В них также присутствуют углекислый газ, азот, сероводород и другие компоненты. Природные газы – это высокоэкономичное энергетическое топливо, имеющее высокую теплоту сгорания.
Газ чисто газовых месторождений состоит почти из одного метана. Этан и пропан содержатся в общем объеме в незначительных количествах, другие углеводороды и прочие газы практически отсутствуют. При таком составе газ называют бедным или тощим.
Газ газоконденсатных месторождений помимо метана содержит значительное количество высших углеводородов, главным образом пропан и бутан. Газ с высоким содержанием гомологов называют богатым или жирным.
Газы нефтяные попутные содержат в значительных количествах гомологи, в том числе высокомолекулярные предельные углеводороды, кроме того, в них присутствуют пары воды, углекислый газ, азот, сероводород, редкие газы - гелий, аргон. Попутный газ (нефтепромысловый) получают при разработке нефтяных месторождений. Количество газов (в куб. м), приходящихся 1 т добытой нефти (т. н. газовый фактор), зависит от условий формирования и залегания нефтяных месторождений и может изменяться от 1-2 до нескольких тысяч куб. м/т нефти.
Искусственные газы содержат больше негорючих компонентов (балласта). Газ коксовых печей содержат до 57% водорода, 22% метана, около 7% окиси углерода, остальное – балластные газы. Газ получают в процессе коксования каменного угля, то есть при нагревании его без доступа воздуха до 900—1100 ° С. Теплота сгорания коксового газа около 17000 кДж/кг. Доменный газ содержат около 30% горючих компонентов, остальное - балласт. Поэтому теплота сгорания доменного газа низкая и немного превышает 4000 кДж/кг.
Генераторный газ ( воздушный газ) — газовая смесь, содержащая окись углерода СО и молекулярный водород Н2.
Получают генераторный газ путём пропускания воздуха над раскалённым каменным углём или коксом в специальных печах — газогенераторах (КПД процесса 65-70 %). Далее окись углерода смешивается с водяным паром и получается водородная составляющая генераторного газа.
Генераторный газ применяется как топливо в металлургической, стекольной, керамической промышленности, для двигателей внутреннего сгорания, а также для синтеза аммиака.
Водород - высококалорийный газ, который может найти применение в авиации и у многих других потребителей вместо жидкого топлива. Большим преимуществом водорода является то, что в результате его сжигания образуется только водяной пар, вследствие чего не происходит загрязнения атмосферы. Водорода на Земле так много, что его ресурсы можно рассматривать как неисчерпаемые. В настоящее время большой интерес вызывает вопрос о получении водорода путём электролиза воды и использовании его вместо дефицитного жидкого топлива. Существенно, что электролиз воды может проводиться в часы, когда потребление электрической энергии относительно невелико, т.е. в ночное время, выходные и праздничные дни. Поэтому проведение электролиза воды и получение водорода хоть и сопровождается большим расходом электроэнергии, экономически может оказаться приемлемым.
Получать водород можно, кроме того, с помощью химических процессов с участием реагентов, содержащих водород, а также катализаторов. Использование водорода в энергетике - вопрос перспективный, и он заслуживает большого внимания.
Ядерное топливо.Природный уран состоит из трёх изотопов: 238  (99,282 %), 235
(99,282 %), 235  (0,712 %) и 234
(0,712 %) и 234  (0,006 %). Он не всегда пригоден как ядерное топливо, особенно если конструкционные материалы и замедлитель интенсивно поглощают нейтроны. В этом случае ядерное топливо изготавливают на основе обогащённого урана. В энергетических реакторах на тепловых нейтронах используют уран с обогащением менее 6 %, а в реакторах на быстрых и промежуточных нейтронах обогащение урана превышает 20 %. Обогащённый уран получают на специальных обогатительных заводах.
(0,006 %). Он не всегда пригоден как ядерное топливо, особенно если конструкционные материалы и замедлитель интенсивно поглощают нейтроны. В этом случае ядерное топливо изготавливают на основе обогащённого урана. В энергетических реакторах на тепловых нейтронах используют уран с обогащением менее 6 %, а в реакторах на быстрых и промежуточных нейтронах обогащение урана превышает 20 %. Обогащённый уран получают на специальных обогатительных заводах.
Ядерное топливо делится на два вида:
1) природное урановое, содержащее делящиеся ядра 235  , а также сырьё 238
, а также сырьё 238  , способное при захвате нейтрона образовывать плутоний 239
, способное при захвате нейтрона образовывать плутоний 239  ;
;
2) вторичное топливо, которое не встречается в природе, в том числе 239  , получаемый из топлива первого вида, а также изотопы 233
, получаемый из топлива первого вида, а также изотопы 233  , образующиеся при захвате нейтронов ядрами тория 232
, образующиеся при захвате нейтронов ядрами тория 232  .
.
Ядерным топливом для термоядерной реакции являются изотопы водорода – дейтерий и тритий. Дейтерий D - это водород Н, но более тяжёлый, его атомное ядро состоит из протона и нейтрона, а тритий Т - ещё более тяжёлый водород, его атомное ядро состоит из одного протона и двух нейтронов.
Следует заметить, что тяжёлый изотоп водорода тритий - вещество радиоактивное, и период его полураспада - около 12 лет. Поэтому тритий на Земле практически не встречается. Но это не создаёт безвыходного положения. Тритий можно получать из щелочного металла лития (Li) путём бомбардировки его атомных ядер быстрыми нейтронами, образующимися, в частности, в той же термоядерной реакции слияния ядер дейтерия и трития. Можно даже вместо трития помещать в термоядерный реактор "тритиевое сырьё" - литий, и в процессе работы реактора тритий в нужных количествах будет воспроизводиться из лития.
Таким образом, что касается ресурса ядерного топлива для термоядерной дейтерий-тритиевой реакции, то в конце концов дело сводится к запасам лития. Действительно, ресурс дейтерия на Земле очень велик, и при использовании дейтерия, содержащегося в воде морей и океанов (а получение дейтерия из воды рассматривается как дело несложное и экономически вполне оправданное), его запасы по энергетическому эквиваленту во много миллионов раз превышают ресурсы всех видов органического топлива, вместе взятых. В отношении же лития, даже с учётом того, что для получения трития "в дело идёт" только изотоп лития 6 Li, содержащийся в природном литии в количестве 7.4%, можно сказать, что его запасы достаточно велики.
|
|
|
12 |


