 |
A. вещества, в молекулах которых содержатся гидрофильные и гидрофобные группы
|
|
|
|
B. растворённые газообразные вещества
C. малорастворимые вещества
D. вещества с развитой поверхностью
E. ионы растворённых неорганических солей
12. Укажите ионы, которые будут адсорбироваться на осадке иодида серебра, полученного в реакции AgNO3 + KI:
A.  или
или 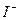
B.  или
или 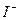 .
.
C.  или
или  ..
..
D.  или
или  .
.
E.  или
или  .
.
13. При каком значении электрокинетического потенциала золь более стабилен?
A. = 120 мВ;
B. = 100 мВ;
C. = 50 мВ;
D. = 10 мВ;
E. = 5 мВ.
14. Выберите ион, который в наибольшей степени вызывает коагуляцию положительного золя:
A. РО43- ;
B. Ва2+;
C.  ;
;
D. Cl-;
E.  .
.
15. Растворы биополимеров относятся к системам:
A. гомогенным, термодинамически устойчивым;
B. гомогенным, термодинамически неустойчивым;
C. гетерогенным, термодинамически устойчивым;
D. гетерогенным, термодинамически неустойчивым;
E. гомогенные, неустойчивые.
16. Способность растворов ВМС со временем уплотнять свою структуру с выделением жидкой фазы называется:
A. синерезисом;
B. тиксотропией;
C. коацервацией;
D. высаливанием;
E. синергизмом.
17. Механизм процесса высаливания белков под действием электролитов основан на:
A. разрушении гидратных оболочек молекул ВМС.
B. адсорбции ионов электролита на заряженных частичках раствора ВМС;
C. внедрение ионов электролита в макромолекулу белка;
D. образовании гидратных оболочек молекул ВМС;
E. абсорбция ионов электролита на заряженных частичках раствора ВМС.
18. Неполярный полимер лучше набухает:
A. в неполярном растворителе;
B. в полярном растворителе;
C. в воде;
D. в ратсворе NaOH;
|
|
|
E. в растворе HCl.
19. Каким законом определяется зависимость скорости химической реакции от концентрации реагирующих веществ?
A. законом действующих масс;
B. законом Генри;
C. законом Аррениуса;
D. законом Вант-Гоффа;
E. законом Авагадро.
20. Каков порядок ферментативной реакции при низких концентрациях субстрата?
A. первый;
B. нулевой;
C. второй;
D. третий;
E. не имеет порядка реакции.
21. Константа скорости химической реакции – это:
A. скорость реакции при единичных концентрациях реагирующих веществ;
B. скорость реакции при одинаковых концентрациях реагирующих веществ;
C. скорость химической реакции в стандартных условиях;
D. скорость реакции при разных концентрациях реагирующих веществ;
E. скорость химической реакции в нормальных условиях.
22. Укажите, какое из соединений азота: NН3, HNO2, KNO3, NO2 или HNO3 проявляет только восстановительные свойства.
A. NН3;
B. NO2;
C. HNO3;
D. HNO2;
E. KNO3.
23. При определении рН биологических жидкостей в качестве электрода определения (индикаторного электрода) можно использовать:
A. Sb,Sb2O3|H+
B. Ag,AgCl|KClнас
C. Hg,Hg2Cl2|KClнас
D. Ag / AgCl;
|
E. Pt|
24. Какое из приведённых веществ наиболее существенно уменьшает поверхностное натяжение воды?
A. C5H11OH
B. C4H9OH
C. C3H7OH
D. C2H5OH
E. CH3OH
25. Ионы, какого из приведенных электролитов, будут адсорбироваться на частицах Mg3(PO4)2:
A. MgCl2;
B. Al(NO3)3;
C. CaCl2;
D. NaOH;
E. NH4OH.
26. У людей пожилого возраста возникает риск возникновения заболеваний, связанных с явлениями коагуляции: мочекаменная болезнь, атеросклероз, тромбофлебит и т.д. Какой из факторов может быть причиной этих явлений?
A. Понижается защитное действие белков и других биополимеров;
|
|
|
B. Понижается содержание глюкозы в крови;
C. Понижается содержание солей в крови.
D. Повышается содержание глюкозы в крови;
E. Повышается защитное действие растворов ВМС.
27. Отличие денатурации белка от его высаливания заключается в следующем:
A. процесс необратим;
B. раствор разделяется на две фазы;
C. происходит при добавлении воды;
D. процесс обратим;
E. происходит смаопроизвольно.
28. Способность растворов ВМС образовывать новую жидкую фазу за счет слияния гидратных оболочек нескольких белковых молекул называется:
A. коацервацией;
B. синерезисом;
C. тиксотропией;
D. высаливанием;
E. денатурацией.
29. Действие высоких концентраций нейтральных солей на растворы ВМС вызывает их:
A. высаливание;
B. синерезис;
C. коацервацию;
D. коагуляцию;
E. флокуляцию.
30. Способность растворов ВМС восстанавливать структуру геля после механического перемешивания называется:
A. тиксотропией;
B. коацервацией;
C. коагуляцией;
D. синерезисом;
E. высаливанием.
31. Разрушение клеточных мембран в организме в основном происходит за счет пероксидного окисления липидов. Эта реакция относится к следующему типу реакций:
A. цепные;
B. циклические;
C. окислительно-восстановительные;
D. параллельные;
E. последовательные;
32. Каков порядок ферментативной реакции, если ее кинетическое уравнение: v = vmax
A. 0;
B. 1;
C. 2;
D. 3;
E. нельзя дать ответ.
33. Константа Михаэлиса равна:
A. концентрации субстрата при скорости реакции, равной половине максимальной;
B. концентрации субстрата при скорости реакции, равной максимальной;
C. отношению концентраций фермента и субстрата;
D. концентрации продукта реакции при скорости равной половине максимальной;
E. концентрации фермента при максимальной скорости реакции;
34. Как повлияет повышение давления на равновесие следующей реакции:
CO(газ) + Cl2(газ)  COCl2(газ) :
COCl2(газ) :
A. сместит равновесие в сторону образования продуктов;
B. равновесие не сместится;
C. сместит равновесие в сторону образования исходных веществ;
D. равновесие сместится влево;
E. равновесие сместится в сторону образования реагентов.
|
|
|
35. Ферменты – это:
A. биологические катализаторы белковой природы.
B. органические вещества, способные инициировать новые реакции;
C. ингибиторы химических реакций;
D. неорганические катализаторы клеток;
E. биологические промоторы химических реакций.
36. Укажите, какое из соединений хлора: НCl, НClО3, HClO, KCl или НClО4 проявляет только окислительные свойства.
A. НСlО4;
B. НC1;
C. НСlО3;
D. HClO;
E. KCl.
37. Изменение изобарно-изотермического потенциала связывает изменение энтальпии и энтропии уравнением:
A. DG = DН - ТDS.
B. DG = ТDS - DН.
C. DG = DН + ТDS.
D. DG = ТDS+DН.
E. DF = DН - ТDS.
38. Для процесса самопроизвольного гидролиза АТФ в клетке какое выражение справедливо:
A. DS > 0;
B. DS < 0;
C. DS = DН;
D. DS = 0.
E. DS £ 1.
39. Метод сорбционной детоксикации организма, который осуществляется при прохождении сорбента через систему пищеварения, называется:
A. энтеросорбцией;
B. апликационной терапией;
C. гемосорбцией;
D. ликвосорбцией;
E. экзосорбцией.
40. Какое выражение отражает суть второго закона термодинамики?
A. Самопроизвольно могут протекать процессы, для которых D G < 0;
B. Самопроизвольно могут протекать процессы, для которых D G > 0;
C. Самопроизвольно могут протекать процессы, для которых D Н > 0;
D. Самопроизвольно могут протекать процессы, для которых D S < 0;
E. Самопроизвольно могут протекать процессы, для которых D F < 0
41. Укажите метод, которым можно получить коллоидный раствор:
- конденсация;
- седиментация;
- коагуляция;
- електрофорез;
- ультрафильтрация.
42. Выберите параметры, от которых зависит константа скорости химической реакции:
A. температура;
B. концентрация исходных веществ;
C. концентрация продуктов реакции;
D. давление;
E. объём.
43. Какие из приведённых ионов будут избирательно адсорбироваться на частицах сульфата кальция?
A. SO42-
B. Cl-
C. PO43-
D. Fe2+
|
|
|
E. Fe3+
44. Какой фактор не влияет на смещение химического равновесия?
A. Катализатор;
B. Давление;
C. Концентрация исходных веществ;
D. Концентрация продуктов реакции;
E. Температура.
45. Какой из ионов имеет наименьшую пороговую концентрацию при коагуляции отрицательного золя?
A. ион бария;
B. ион хлора;
C. ион натрия;
D. сульфат-ион;
E. ион цезия.
46. Характерной особенностью строения молекул поверхностно-активных веществ (ПАВ) является:
A. дифильность;
B. полярность;
C. гидрофильность;
D. гидрофобность;
E. лиофильность.
47. Электрокинетический потенциал возникает на границе:
A. адсорбционный слой противоионов – диффузионный слой противоионов;
B. ядро – потенциалопределяющие ионы;
C. потенциалопределяющие ионы - адсорбционный слой противоионов;
D. ядро – диффузный слой противоионов;
E. адсорбционный слой противоионов – гранула.
48. Если изоэлектрическая точка белка равна 4,7, то частицы белка заряжены положительно при рН равном:
A. 3,0;
B. 4,7;
C. 7,0;
D. 12,7;
E. нет ответа
49. Для экзергонических реакций справедливо выражение:
A. DG < 0,
B. DG > 0,
C. DS < 0,
D. DН > 0,
E. DН < 0.
50. Укажите эндергонический процесс в организме человека:
A. синтез полисахаридов;
B. гидролиз полисахаридов;
C. окисление глюкозы;
D. окисление жирных кислот.
E. окисление белков
51. Гидролиз полисахаридов в организме относится к следующему типу реакций:
A. последовательные;
B. окислительно-восстановительные;
C. параллельные;
D. циклические;
E. цепные.
52. От чего зависит величина энергии активации вещества в реакции?
A. природы реагирующего вещества;
B. концентрации;
C. молярной массы вещества;
D. давления;
E. молярной концентрации вещества.
53. Образование костной ткани можно выразить обшей схемой:
5Са2+ + ЗНРО42- + НОН Û Ca5 (OH)(PO4)3 + 4Н+
Укажите среду, при которой идет преимущественное образование костной ткани:
A. щелочная,
B. кислая;
C. нейтральная;
D. рН < 7;
E. pH = 0.
54. Укажите, какое из соединений серы: Н2S, S, SO3, SO2, H2SO4 проявляет только восстановительные свойства.
A. Н2S;
B. S;
C. SO2;
D. SO3;
E. H2SO4.
55. Укажите термодинамическую функцию состояния системы:
A. Внутренняя энергия;
B. Температура;
C. Давление;
D. Концентрация вещества;
|
|
|
E. Масса компонентов системы.
56. Стационарное состояние системы характеризуется:
A. Постоянным значением параметров за счет внешнего воздействия на систему;
B. Постоянным изменением параметров при отсутствии внешнего воздействия на систему;
C. Постоянным изменением параметров за счет внешнего воздействия на систему;
D. Постоянным значением параметров при отсутствии внешнего воздействия на систему;
E. Постоянным значением функций состояния системы при отсутствии внешнего воздействия на систему.
57. Первое следствие закона Гесса касается:
A. DНобр.;
B. DНсгор.;
C. DНпл.;
D. DНсубл.;
E. DНравн.
58. К электродам 1-го рода относится:
A. Zn½ Zn2+;
B. Hg, Hg2Cl2½KClнас.;
C. ст. эл.½Н+
D. Pt½H+х.г.;
E. 
59. При помещении водородного электрода в раствор соляной кислоты величина его электродного потенциала по сравнению с водой:
A. увеличится;
B. не изменится;
C. уменьшится.
D. станет равной электродному потенциалу хлорсеребряного электрода;
E. будет равной электродному потенциалу каломельного электрода.
60. Потенциал действия на клеточной мембране возникает в результате:
A. увеличения прницаемости мембраны для ионов натрия;
B. различной растворимости катионов и анионов в липидных слоях мембраны;
C. повреждения клеточной мембраны;
D. увеличения прницаемости мембраны для ионов калия;
E. увеличения проницаемости клеточной мембраны для ионов хлора.
61. Выберите реакцию, за счет которой возможен перенос электронов при клеточном дыхании в митохондриях:
A. Cu+ -e = Cu2+;
B. Ag – e = Ag+;
C. Al – 3e = Al3+;
D. Au2+– e = Au3+;
E. Na – e = Na+.
62. Учитывая окислительно-восстановительную способность, из какого металла необходимо изготовить электроды, которые применяются, например, в кардиохирургии для подключения к аппарату, стимулирующего работу сердечной мышцы?
A. Золото;
B. Железо;
C. Медь;
D. Алюминий;
E. Цинк
63. По какому признаку системы классифицируют на аэрозоли, лиозоли, солеозоли?
A. по агрегатному состоянию дисперсионной среды
B. по степени устойчивости;
C. по величине межфазного взаимодействия;
D. по степени дисперсности;
E. по агрегатному состоянию дисперсной фазы.
64. Укажите метод очистки коллоидного раствора от примесей:
A. диализ;
B. седиментация;
C. електрофорез;
D. конденсация;
E. ультрацентрифугирование.
65. Что такое хемосорбция?
A. химическое взаимодействие адсорбента и адсорбтива;
B. накопление одного вещества внутри другого;
C. растворение одного вещества в другом;
D. накопление одного вещества на поверхности другого;
E. образование однородной смеси;
66. Мицелла золя имеет строение: {(BaSO4)m . nSO42- (2n –x) Na+}x- xNa+.
Какое вещество является стабилизатором?
A. Na2SO4;
B. BaCl2
C. BaSO4;
D. NaCl;
E. Ba(NO3)2.
67. За катионообменные свойства биологических структур ответственны в основном:
A. Карбоксильные и фосфатные группы;
B. Меркапто-группы.
C. Гидроксильные группы;
D. Метиленовая группа.
E. Аминогруппы белков.
68. Какие ионы стабилизатора определяют заряд гранулы?
A. Содержащиеся в ядре или имеющие сродство к ядру;
B. Содержащиеся в большом количестве.
C. Имеющие большой заряд;
D. Не имеющие заряда;
E. Не имеющие сродства к ядру.
69. Наименьшая растворимость (набухание) белков при:
A. рН = рНИЭТ ;
B. рН < рНИЭТ ;
C. рН > рНИЭТ ;
D. рН ¹ рНИЭТ;
E. рН ³ рНИЭТ.
70. Ионы, какого из приведенных электролитов, будут адсорбироваться на частицах AgCl:
A. CaCl2;
B. Mg(ОН)2;
C. NaOH;
D. Na2S;
E. NH4OH.
71. Какая температура является оптимальной для ферментативного катализа?
A. 37-43 оС;
B. 28-32 оС;
C. 45-50 оС;
D. 50-60 оС;
E. 37-49 0С.
72. Каким законом определяется зависимость скорости химической реакции от температуры?
A. законом Аррениуса;
B. законом Генри;
C. законом действующих масс;
D. законом Гесса;
E. законом эквивалентов.
73. Влияние рН на ферментативную активность обусловлено:
A. содержанием ионогенных групп в белке-ферменте;
B. содержанием неионогенных групп в белке-ферменте;
C. наличием оптимума по температуре для активности фермента;
D. содержанием гидрофобных групп в белке-ферменте;
E. содержанием неполярных групп в белке-ферменте.
74. Константа скорости химической реакции не зависит от:
A. концентрации реагирущих веществ;
B. природы растворителя;
C. температуры;
D. природы реагирующих веществ.
E. от наличия катализатора.
75. Укажите, какая из приведенных схем представляет собой процесс восстанов ления:
A.  ;
;
B.  ;
;
C.  ;
;
D.  S+2 S+4;
S+2 S+4;
E.  2Cl- Cl2.
2Cl- Cl2.
76. Для изохорного процесса справедливо выражение:
A. V = const;
B. Р = const;
C. T = const;
D. Р = const, T = const.
E. Р = const, V = const.
77. Причиной возникновения мембранного потенциала является:
A. различная проницаемость мембраны для катионов и анионов;
B. влияние полярных молекул растворителя;
C. наличие разных зарядов у катионов и анионов
D. -
E. одинаковая проницаемость мембраны для катионов и анионов.
78. Какая из приведенных гальванических цепей может быть использована для определения рН биологических жидкостей в лабораторно-клинических исследованиях?
A. Стекл.эл½рН½½ рНх½Стекл.эл.;
B. Pt½Sn4+½Sn2+½½ Fe3+½Fe2+½Pt;
C. Fe½Fe2+½½ Au+½Au;
D.  Pt½MnO4–, Mn2+½½ KClнас.½AgCl, Ag;
Pt½MnO4–, Mn2+½½ KClнас.½AgCl, Ag;
E. 
 Pt(H2) H+ Sb2O3, Sb.
Pt(H2) H+ Sb2O3, Sb.
79. Диффузионный потенциал в клетке возникает вследствие:
A. повреждения клеточной мембраны;
B. наличие ионов разного размера внутри и снаружи;
C. возбуждения клетки;
D. различной растворимости катионов и анионов в липидных слоях мембраны.
E. различной проницаемости мембраны для катионов и анионов
80. Какой знак заряда имеет гранула в мицелле: {(СaSO4)m . nSO42- (2n –x) Na+} nNa+
A. отрицательный;
B. положительный;
C. не имеет заряда.
D. имеет заряд в зависимости от среды.
E. нет ответа
81. Чем образована наружная поверхность клеточных мембран?
A. гидрофильными группами фосфолипидов;
B. гидрофобными группами фосфолипидов;
C. ионами растворённых веществ;
D. молекулами белков;
E. молекулами животного крахмала-гликогена.
82. Ионы, какого из приведенных электролитов, будут адсорбироваться на частицах NiS:
A. Na2S;
B. NaOH;
C. CaCl2;
D. MgCl2;
E. NH4OH.
83. Укажите фактор, уменьшающий коагуляцию золя:
A. лиофилизация гранулы мицеллы белком;
B. уменьшение дзета- потенциала;
C. увеличение концентрации добавляемого электролита;
D. облучение золя.
E. добавлением одноименных ионов с противоионами.
84. Денатурация белков – это:
A. специфическое осаждение, сопровождающееся изменением их структуры;
B. уменьшение растворимости ВМС путем замены растворитеря;
C. обратимое осаждение белков под действием растворов электролитов;
D. обратимое осаждение белков путем увеличения концентрации ВМС;
E. слияние водных оболочек нескольких частиц.
85. Зависимость скорости ферментативной реакции от концентрации субстрата описывается уравнением:
A. Михаэлиса-Ментен;
B. Вант-Гоффа;
C. Аррениуса;
D. Авогадро;
Е: Рауля.
86. Механизм энергетического сопряжения в биологических системах осуществляется с помощью:
A. фосфат -иона;
B. карбонат-иона;
C. сульфат -иона;
D. хлорид-иона.
E. иодид-иона.
87. Свободная энергия Гиббса характеризует:
A. изобарно-изотермический процесс;
B. изотермический процесс;
C. изохорный процесс;
D. изохорно-изотермический процесс.
E. изобарный процесс
88. Диффузионный потенциал возникает на границе:
A. раствор – раствор;
B. мембрана – раствор;
C. электрод – раствор;
D. осадок – раствор
E. нет ответа
89. Укажите, где гальваническая цепь записана правильно:
A. Zn½ZnSO4½½ CuSO4½Cu;
B. Cu½CuSO4½½ ZnSO4½ Zn;
C. Zn½ZnSO4½½ KClнас.
D. не корректный вопрос
E. нет правильного ответа
90. Как правило, в ионселективных электродах потенциал:
A. мембранный;
B. дифузионный;
C. фазовый;
D. нет однозначного ответа.
E. диффузионно-фазовый
91. Какие из приведённых веществ положительно адсорбируются на поверхности воды?
A. C4H9-COOH
B. NH4Cl
C. CuSO4
D. KAl(SO4)2
E. NaCl
92. Какие ионы преимущественно адсорбируются на частицах, образующихся в реакции: H2SO4 + BaCl2 ®?
A.  или
или  ..
..
B.  или
или  .
.
C.  или
или  .
.
D.  или
или  .
.
E.  или
или  .
.
93. В организме человека гели входят в состав кожи. Старение ее происходит за счет уплотнения структуры геля и потери влаги. Этот процесс называется:
A. синерезисом;
B. тиксотропией;
C. коагуляцией;
D. коацервацией.
E. денатурацией
94. При острой почечной недостаточности, например, при отравлениях солями ртути, сульфаниламидными препаратами, при уремии после переливания крови, ожогах и т.д. используют аппарат «Искусственная почка». На каком принципе основано действие этого аппарата?
A. Диализ;
B. Электрофорез;
C. Светорассеивание.
D. Светопоглощение
E. нет ответа
95. Выберите значение энергии активации при которой скорость реакции наибольшая:
A. 4кДж;
B. 8 кДж;
C. 12 кДж;
D. 16 кДж;
96. Состояние живых организмов определяется как:
A. неравновесное стационарное;
B. неравновесное;
C. равновесное стационарное;
D. равновесное;
E. стабильное
97. При написании термохимического уравнения обязательно следует указывать:
A. тепловой эффект и агрегатное состояние вещества;
B. тепловой эффект;
C. агрегатное состояние вещества;
D. температуру реакции;
E. наличие катализатора
98. Для процессов растворения и диффузии какое выражение справедливо:
A. DS > 0;
B. DS < 0,
C. DS = 0;
D. DS = DН
E. DS < DН
99. Укажите, какое из соединений фосфора: Н3Р, Р, Н3РO3, Н3РO4 проявляет только окислительные свойства.
- Н3РO4;
- Н3Р;
- Р;
- Н3РO3
- нет ответа
100. Расчет потенциала водородного электрода проводят по формуле:
A. Е = - 0,059 рН;
B. Е = Е0 + 0,059 рН;
C. Е = - 0,059(рН2 – рН1);
D. 
E. нет ответа
101. При формировании потенциала покоя внутренняя поверхность клеточной мембраны заряжена:
A. отрицательно;
B. не имеет заряда;
C. положительно;
D. нужны дополнительные сведения.
E. нет ответа
102. В зонде Линара используется гальваническая цепь:
A. Sb,Sb2O3|H+ || KClнас|Hg2Cl2,Hg;
B. Hg,Hg2Cl2|KClнас || HClх.г.|Pt;
C. Pt (H2)|H+ || KClнас|AgCl,Ag
D. стекло|H+|| KClнас|Hg2Cl2,Hg
E. зонд Линара не использует гальваническую цепь
103. Какая из реакций может быть использована для получения коллоидного раствора конденсационным методом:
A. Na2SO4 + BaCl2 «BaSO4¯ + 2NaCl;
B. Na2CO3 + H2SO4 «Na2SO4 + CO2 + H2O
C. HCl + NaOH «NaCl + H2O;
D. Н2CO3 « CO2 + H2O
E. CO2 + H2O «Н2CO3
104. Какие из частичек мицеллы {(AgCl)m . nCl-(n –x) Na+}x- xNa+ относятся к противоионам?
A. ионы натрия;
B. (AgCl)m;
C. хлорид-ионы;
D. (AgCl)m . nCl-
E. вода
105. Какие из приведённых ионов будут избирательно адсорбироваться на частицах малорастворимой кремниевой кислоты (Н2SiO3)?
A. H+
B. Na+
C. Ca2+
D. Al3+
E. SO42-
106. Какое из приведённых веществ не явля е тся поверхностно-активными?
A. CuSO4
B. C5H11-NH2
C. 
D. C3H7COOH
E. 
107. С какой целью принимают внутрь активированный уголь (карболен)?
A. связывание ядов и токсинов, попавших в желудочно-кишечный тракт;
B. образование комплексных соединений;
C. уменьшение растворимости питательных веществ;
D. образование поверхностных плёнок;
E. изменение рН желудочного сока.
108. В клинической практике при постановке диагноза широко используется показатель СОЭ. Какое свойство коллоидных систем лежит в основе этого определения?
A. седиментация;
B. диффузия;
C. осмос;
D. солюбилизация;
E. светорассеивание
109. Основным фактором термодинамической устойчивости растворов ВМС является:
A. лиофильность;
B. лиофобность;
C. большая молярная масса;
D. пространственная структура.
E. наличие неполярных групп
110. К какому из электродов будут двигаться молекулы белка, находящиеся в изоэлектрическом состоянии?
A. двигаться не будут;
B. катоду;
C. аноду;
D. зависит от концентрации.
E. нет ответа
111. Энтальпия – это:
A. Функция, характеризующая теплосодержание в системе;
B. Функция, характеризующая скорость протекания превращения в системе;
C. Функция, характеризующая направление протекания превращения в системе;
D. Функция, характеризующая вероятность протекания превращения в системе;
E. нет ответа
112. Фотохимические реакции относятся к следующему типу реакций:
A. цепные;
B. параллельные;
C. циклические;
D. последовательные.
E. циклически-последовательные
113. Скорость какой реакции отвечает выражению: V = k [H2]?
A. H2 + S¯ ® H2S;
B. H2 + I2 ® 2HI;
C. H2 + CO2 ® C + H2O;
D. 2H2 + O2 ® 2H2O
E. нет ответа
.
114. Укажите, какое из соединений йода: Нl, НlО3, 12 или НlО4 проявляет только восстановительные свойства:
A. Нl
B. Н1О3; ;
C. НlО4
D. 12
E. нет ответа
115. Зонд Линара применяется для:
A. внутрижелудочной рН-метрии;
B. измерения рН слюны;
C. измерения рН спинно-мозговой жидкости;
D. измерения рН крови.
E. измерения рН мочи
116. При формировании потенциала покоя внешняя поверхность клеточной мембраны заряжена:
A. положительно;
B. не имеет заряда;
C. отрицательно.
D. нельзя дать однозначного ответа.
E. нет ответа
117. Некоторые лекарственные репараты являются коллоидными растворами. Каков диаметр частичек соответствует коллоидному состоянию?
A. 10-9-10-7м;
B. 10-5-10-4м;
C. 10-7-10-5м;
D. 10-11-10-9м
E. 10-12-10-14м
118. Электрофорез – это:
A. движение твердой фазы золя относительно жидкой в электрическом поле;
B. движение жидкой фазы золя относительно твердой в электрическом поле;
C. движение золя через капилярную систему;
D. оседание твердой фазы в жидкой среде.
E. растворение твердой фазы
119. Какие из приведённых веществ являются поверхностно-активными?
A. C17H35COONa;
B. Na2SO4;
C. BaCl2;
D. Cu(NO3)2;
E. H2SO4.
120. Который из спиртов обладает наибольшей поверхностной активностью?
A. С5Н11ОН;
B. С4Н9ОН;
C. С3Н7ОН;
D. С2Н5ОН;
E. СН3ОН;
121. Какие из приведённых веществ являются поверхностно-активными?
A. C3H7-NH2
B. AlCl3
C. NaOH
D. NH3
E. NH4OH
122. Что такое адсорбция?
A. накопление одного вещества на поверхности другого
B. накопление одного вещества внутри другого
C. растворение одного вещества в другом
D. химическое взаимодействие между веществами
E. перемешивание веществ
123.Как влияет повышение температуры на величину физической адсорбции веществ на поверхности твёрдых тел?
A. адсорбция уменьшается
B. адсорбция увеличивается
C. не изменяется
D. влияние зависит от природы адсорбента
E. влияние зависит от природы адсорбируемого вещества
124.Как влияет увеличение давления газа на величину его физической адсорбции на твёрдом адсорбенте?
A. адсорбция увеличивается
B. адсорбция уменьшается
C. не изменяется
D. влияние зависит от природы адсорбента
E. влияние зависит от природы газа
125.Что такое адсорбент?
A вещество, на поверхности которого происходит адсорбция
B дсорбирующееся вещество
C растворитель
D растворяемое вещество
E малорастворимое вещество
126.Что такое обменная адсорбция?
A. замещение на адсорбенте одного вещества другим, находящимся во внешней среде
B. накопление одного вещества внутри другого
C. растворение одного вещества в другом
D. накопление одного вещества на поверхности другого
E. избирательное накопление веществ на поверхности адсорбента
127.На чём основан метод адсорбционной хроматографии?
A. избирательной адсорбция веществ из смесей
B. различии в распределении веществ между несмешивающимися жидкостями
C. обмене ионов между раствором и адсорбентом
D. образовании химических соединений
E. различной растворимости веществ, составляющих смесь
128. Какие вещества могут быть поверхностно-активными на границе вода-воздух?
A. вещества, в молекулах которых содержатся гидрофильные и гидрофобные группы
B. растворённые газообразные вещества
C. малорастворимые вещества
D. вещества с развитой поверхностью
E. ионы растворённых неорганических солей
129. Зависимость скорости ферментативной реакции от температуры (Т) имеет вид:
A. выпуклой кривой
B. вогнутой кривой
C. восходящей прямой
D. нисходящей прямой
E. нет ответа
130.Зависимость скорости ферментативной реакции от температуры (Т) имеет оптимум из-за:
A. потери нативной (активной) структуры ферментом при высоких Т;
B. увеличения количества эффективных соударений фермента и субстрата при увеличении Т;
C. возрастания скорости химической реакции при увеличении Т;
D. нет точного обьяснения
131. Введение катализатора в систему CO + Cl2 = COCl2 смещает равновесие:
A не смещает
B влево;
C вправо;
D зависит от температуры
E зависит от концентрации
132. Второе следствие из закона Гесса касае
|
|
|


