|
Средства защиты трубопроводов и инженерных систем от коррозии
|
|
|
|
Содержание
Введение………………………………………………………………………1
Руководящие документы….…………………………………………….....2
Механизмы коррозии……………………………………………………….3
Ряд напряжений……………………………………………………………..5
Коррозионная активность грунтов и методы ее определения………...8
Пассивная и активная защита……………………………………………24
Пассивная изоляция……………………………………………………….26
Приборы контроля за состоянием системы ЭХЗ……………………....29
Активные средства защиты инженерных коммуникаций……………30
Протекторная защита. Назначение устройства. Алгоритм расчета..30
Катодная защита……………………………………………………………33
Принцип расчета катодной защиты……………………………………..34
Электродренажная защита………………………………………………..35
Схема технологии систем электро-химической защиты (СЭХЗ)…….36
Состав проекта при выполнении СМР………………………………….36
Пуско-наладочные работы (ПНР)…………………………………….....36
Средства защиты трубопроводов и инженерных систем от коррозии
| Лекция 1 | |||||||||||||||||||||||||||||||||||
| Введение | |||||||||||||||||||||||||||||||||||
| Трубопроводы и сооружения подвергаются коррозии, которая наносит огромный ущерб инженерным системам, а также снижает их устойчивость и способствует аварийным ситуациям и авариям. Особо опасна почвенная коррозия. Почвенную коррозию подразделяют на: - химическую (возникает от действия на металл различных газов и жидких электролитов) - электрохимическую (является результатом взаимодействия металла, который выполняет роль электродов, с агрессивными растворами грунта, выполняющими роль электролита) - электрическую (возникает под действием блуждающих токов) | |||||||||||||||||||||||||||||||||||
| Системы жизнеобеспечения ТГВ+ВВ | |||||||||||||||||||||||||||||||||||
| ТГВ | ВВ | ||||||||||||||||||||||||||||||||||
| Источники энергии – «топливо» (ИЭ-Т) Газоснабжение – «Г» (СГРГП) Источники тепла – «ИТ» (ТГУ) Теплоснабжение – «горячее водоснабжение» (Т-ГВС) Отопление – «О» Вентиляция и кондиционирование – «ВК» Защита от коррозии – «СЭХЗ» | Источник энергии – «вода, сточные воды» (ИЭ-В+СВ) Водоснабжение поселений – «ВП» Водоотведение поселений – «ВоП» Водоснабжение промпредприятий – «ВПП» Водоотведение промпредприятий – «ВоПП» Оборотное водоснабжение – «ОВС» Системы пожаротушения – «СПТ» Защита от коррозии – «СЭХЗ» | ||||||||||||||||||||||||||||||||||
| Термины и определения (см. Приложения) | |||||||||||||||||||||||||||||||||||
| Нормативно-техническая литература (см. Приложения) | |||||||||||||||||||||||||||||||||||
| Лекция 2 | |||||||||||||||||||||||||||||||||||
| Руководящие документы | ГОСТ | ||||||||||||||||||||||||||||||||||
| РД 153.39.4 – 091-91. «Инструкция по защите городских подземных трубопроводов от коррозии» РД 153-34.0-20.518-2003 «Типовая инструкция по защите трубопроводов тепловых сетей от наружной коррозии» | ГОСТ 9.602-2005 «Единая система защиты от коррозии и старения» | ||||||||||||||||||||||||||||||||||
| Основные положения при защите металлических городских газопроводов | |||||||||||||||||||||||||||||||||||
| 1. Все организации, проводящие весь цикл работ должны иметь лицензию и руководствоваться ГОСТ 9.602 - 05 и др. НТД. В городах, поселениях все металлические трубопроводы и сооружения должны быть защищены весьма усиленной изоляцией, а при наличии блуждающих токов – иметь обязательно активную защиту. 2. Мероприятия по защите трубопроводов от коррозии должны быть предусмотрены проектом, который разрабатывается одновременно с проектом строительства или реконструкции трубопровода. Проект разрабатывается на основании коррозийной агрессивности грунтов и наличии блуждающих токов. Проект выполняется на основе технических условий. 3. Все виды защиты от коррозии должны быть введены в эксплуатацию до сдачи газопроводов (допускается работа без защиты в зоне блуждающих токов сроком не более 1 месяца, в остальных случаях - 6 месяцев). 4. Основные работы по контролю за коррозийным состоянием трубопроводов осуществляет эксплуатационная организация | |||||||||||||||||||||||||||||||||||
| Лекция 3 | |||||||||||||||||||||||||||||||||||
| Механизмы коррозии | |||||||||||||||||||||||||||||||||||
| Первопричиной коррозии металлов, в том числе и электрохимической коррозии, является их термодинамическая неустойчивость. При взаимодействии с электролитами металлы самопроизвольно растворяются, переходя в более устойчивое окисленное (ионное) состояние. | |||||||||||||||||||||||||||||||||||
| Химический механизм растворения металлов в электролитах | Электрохимический механизм растворения металлов в электролитах | ||||||||||||||||||||||||||||||||||
| Проходит на одном и том же участке поверхности в одну стадию, независимо от потенциала металла химической реакции, без участия свободных электронов, когда металл, отдавая окислителю валентные электроны, вступает с ним в химическое соединение или образует ионы; может иметь место и в электролитах. | Протекает с участием свободных электронов электрохимической реакции, при которой ионизация атомов металла и восстановление окислительного компонента коррозионной среды проходят не в одном акте и их скорости зависят от величины электродного потенциала металла; имеет место в подавляющем большинстве случаев коррозии металлов в электролитах и является, таким образом, преобладающим. | ||||||||||||||||||||||||||||||||||
| Гальвано-, микро- и макропары | |||||||||||||||||||||||||||||||||||
Протекание электрохимической коррозии обычно характеризуется локализацией анодного и катодного процессов на различных участках корродирующей поверхности металла, что приводит к неравномерному или местному характеру коррозионного разрушения. Эти отличающиеся по своим физическим и химическим свойствам участки, являются в зависимости от их размеров короткозамкнутыми макрогальваническими (имеющими размеры, хорошо различимые невооруженным глазом) или микрогальваническими (обнаруживаемыми лишь при помощи микроскопа) элементами.
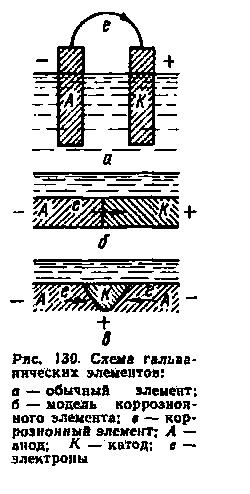 Таким образом, электрохимическая коррозия металлов напоминает работу гальванического элемента, в котором отрицательный электрод (например, цинк) растворяется, когда он соединен проводником со вторым электродом, на котором восстанавливаются ионы водорода или другие вещества. Поэтому ее можно рассматривать как результат работы большого числа коррозионных гальванических элементов на корродирующей поверхности металла, соприкасающейся с электролитом.
Таким образом, электрохимическая коррозия металлов напоминает работу гальванического элемента, в котором отрицательный электрод (например, цинк) растворяется, когда он соединен проводником со вторым электродом, на котором восстанавливаются ионы водорода или другие вещества. Поэтому ее можно рассматривать как результат работы большого числа коррозионных гальванических элементов на корродирующей поверхности металла, соприкасающейся с электролитом.
| |||||||||||||||||||||||||||||||||||
| Коррозионные гальванические элементы и причины их возникновения | |||||||||||||||||||||||||||||||||||
| Поверхность корродирующего металла представляет собой обычно многоэлектродный, т.е. состоящий из нескольких (более двух) отличающихся друг от друга электродов, гальванический элемент. В первом приближении эту поверхность можно рассматривать как двухэлектродную систему, т.е. состоящую из участков двух видов — анодных (одного сорта) и катодных (тоже одного сорта). | |||||||||||||||||||||||||||||||||||
| Причины возникновения электрохимической гетерогенности (неоднородности) поверхности раздела металл- электролит: | |||||||||||||||||||||||||||||||||||
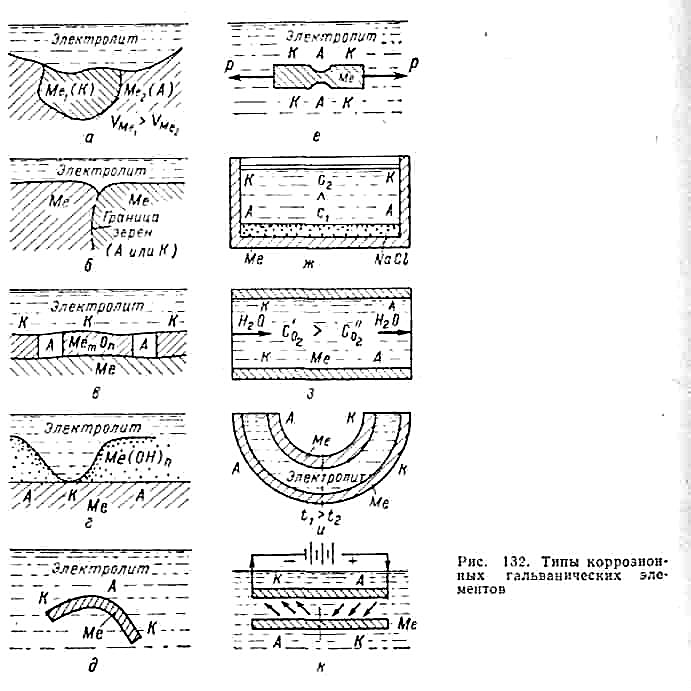
| Общая причина возникновения гетерогенности | Конкретная причина возникновения гетерогенности | Схематичное изображение гетерогенности | |||||||||||||||||||||||||||||||||
| Неоднородность металлической фазы Неоднородность поверхности металла Неоднородность защитных пленок на поверхности металла Неоднородность физических условий | Макро- и микровключения; Неоднородность сплава Наличие границ блоков и зерен кристаллов Анизотропность металлического кристалла Макро- и микропоры в окисной пленке Неравномерное распределение на поверхности металла вторичных продуктов коррозии Различие температуры Неравномерное распределение лучистой энергии Неравномерное наложение внешнего электрического поля | 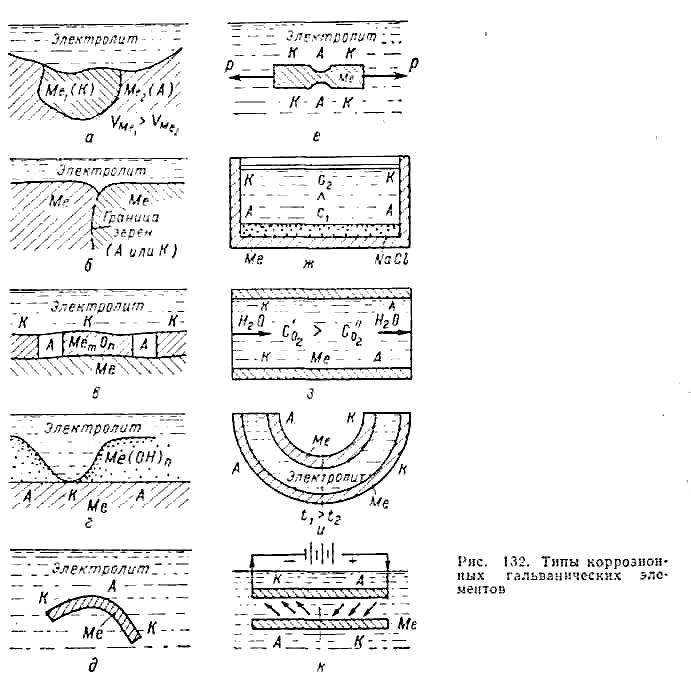


| |||||||||||||||||||||||||||||||||
| Таким образом, электрохимическая гетерогенность поверхности корродирующего металла приводит к дифференциации последней на анодные (с более отрицательным электродным потенциалом φa) и катодные (с более положительным электродным потенциалом φк) участки. Степень гетерогенности этой поверхности характеризуется разностью электродных потенциалов анодных и катодных участков: φa - φк. | |||||||||||||||||||||||||||||||||||
| Лекция 4 | |||||||||||||||||||||||||||||||||||
| Ряд напряжений | |||||||||||||||||||||||||||||||||||
| Если один из электродов принять за стандартный и сравнивать с ним вез остальные, то металлы могут быть расположены в порядке возрастания электродных потенциалов, т.е. образует ряд напряжений (потенциалов). На схеме представлены некоторые распространённые металлы, расположенные в порядке уменьшения их электродных потенциалов. Na – Al – Mn – Zn – Cr – сталь – Ni – Pb – Cu – Ag Выводы: 1. Коррозия металла обычно возникает в присутствии кислорода и воды. 2. Коррозия сопровождается движением электронов. 3. Коррозия металла не происходит на поверхности равномерно, т.к. есть неоднородности, где возникает точечная коррозия. 4. Продукт коррозии - ржавчина, может образовываться на некотором расстоянии от места зарождения коррозии. 5. Высокая концентрация кислорода способствует образованию катода и, непосредственно примыкающей участок, становится анодом и коррозирует. 6. Интенсивность коррозионного взаимодействия между металлами зависит от ЭДС, определяемой разностью потенциалов между металлами, природой электролита, соотношения площади поверхности двух металлов и расстояния между ними. 7. Металл с плотно прилегающими нерастворёнными плёнками обладают более высокой коррозионной стойкостью, чем металл с растворёнными плёнками. Разрушение плёнок вызывают дальнейшую коррозию, обнажая металл. 8. На коррозию металла оказывает большое влияние окружающая среда (температура, концентрация, рабочие условия). 9. На коррозию металла оказывает влияние химический состав и микроструктура. 10. В материаловедении фазовая составляющая, находящаяся в равновесии при конкретных температурах, давлениях и составе сплавов, может быть определена экспериментально и представлена в виде диаграммы. | |||||||||||||||||||||||||||||||||||
| Простейшая коррозионная диаграмма | |||||||||||||||||||||||||||||||||||

| а – анодная кривая; к – катодная кривая; φMeравн, φoxравн – равновесные потенциалы металла и окислителя; φc – стационарный потенциал корродирующего металла. | ||||||||||||||||||||||||||||||||||
| Основные способы защиты от коррозии | |||||||||||||||||||||||||||||||||||
| Принцип защиты ПМС от ЭХК | Пример | ||||||||||||||||||||||||||||||||||
| 1) создание на поверхности металла химически инертного слоя, по возможности, непроницаемого для компонентов среды, участвующих в реакциях ЭХК. Эти слои называются изоляционными или барьерными покрытиями. 2) уменьшение концентрации в среде агрессивного реагента, участвующего в одной из сопряжённых реакций. 3) снижение скорости анодного и катодного процессов путём введения в среду ингибиторов, тормозящих процесс коррозии. 4) ЭХЗ, при которой скорость анодного процесса за счёт изменения потенциала, снижает до значений, не превышающих технически допустимую величину. 5) нанесение на поверхности стали анодных металлических покрытий (А1, Zn, Cr). 6) рациональное проектирование и эксплуатирование ПМС включает: | На практике к ним относятся битумные, эпоксидные, полиэтиленовые, каменноугольные и другие покрытия. Деаэрация воды в системах горячего водоснабжения, т.е. снижение концентрации растворённого кислорода и воздуха. Ингибиторы вводят в защитные органические покрытия, особенно в первый слой, наносимый непосредственно на металл - грунтовка или праймер, раствор битума марки 4 в изоляционном бензине Б70,в соотношении 1-КЗ. Если для этого используются специальные источники постоянного тока, то ЭХЗ называют катодной (станция катодной защиты). Если потенциал понижают при соединении защитного объекта к протектору, т.е. к металлу, со значительно более отрицательным потенциалом коррозии (Mg, Al, Zn), то защита называется протекторной или гальванической. · выбор трассы; · выбор защитных покрытий с учётом агрессивности почвы (весьма усиленная); · обеспечение требований качества изоляционных покрытий; · систематический контроль в процессе эксплуатации; · исключение контактов труб с арматурой железобетона; · максимальное уменьшение возможности образования электрических контактов. | ||||||||||||||||||||||||||||||||||
| Лекция 5 | |||||||||||||||||||||||||||||||||||
| Коррозионная активность грунтов и методы ее определения | |||||||||||||||||||||||||||||||||||
| Коррозионная активность зависит от многих факторов: температуры, влажности, солевого состава, щелочности и т.д. Для определения активности грунтов применяют понятие электропроводности почв, которая играет существенную роль в коррозионном процессе. У большинства почв коррозионная активность возрастает с увеличением их проводимости, которая характеризует удельное электросопротивление р (Ом/м). Чем ниже р, тем выше коррозионная активность (см. табл.). | |||||||||||||||||||||||||||||||||||
| Таб. Характеристика коррозионной активности грунтов и средства защиты | |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| Наиболее распространенные виды коррозии и меры их предотвращения | |||||||||||||||||||||||||||||||||||
| Общие сведения | |||||||||||||||||||||||||||||||||||
| Любой коррозионный процесс является химически сложным: он не соответствует тому простому случаю, при котором один материал окисляется до ионного состояния, а другой восстанавливается путем приобретения электронов. Полезной может оказаться такая модель, согласно которой в первую очередь следует считаться с поверхностными явлениями, которые вызывают коррозионный процесс, а затем с совокупным влиянием индивидуальных коррозионных поражений. Нерациональная деятельность человека привела к усилению коррозионной активности атмосферы; почвы и природных вод. Вместе с этим возрастает сложность коррозионных проблем. | |||||||||||||||||||||||||||||||||||
| Кавитационные повреждения | |||||||||||||||||||||||||||||||||||
Повреждение материала, связанное со схлопыванием пустот в жидкости на поверхности ее раздела с твердым телом называется кавитационным разрушением.

| |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| Слабое физическое повреждение защитных пленок (кавитационная коррозия), сильную деформацию и разрушение поверхности (кавитационная деформация) или повторяющийся процесс схлопывания паровых пузырей – усталостное разрушение поверхности металла (кавитациопная усталость). Области пониженного давления образуются при расширении потока, вращении жидкости, наличии препятствий на пути потока или вследствие вибрации. | Избегать условий, при которых абсолютное давление надает ниже давления паров жидкости. Сводить к минимуму разности гидродинамических давлений. Понижать перенос вибрации. Выбирать соответствующие геометрические формы или углы поверхности. Препятствовать доступу диспергированного воздуха. Обеспечивать качественную обработку поверхности. Наносить эластичные покрытия или облицовки. Использовать катодную защиту. Вводить или генерировать в жидкости более крупные воздушные или газовые пузыри, амортизирующие процесс кавитации. | ||||||||||||||||||||||||||||||||||
| Щелевая коррозия | |||||||||||||||||||||||||||||||||||
Концентрационный элемент – это гальваническая ячейка, ЭДС которой обусловлена разностью концентраций одной пли более реакционноспособных составляющих электролитического раствора.
Щелевая коррозия – локализованная коррозия, возникшая в результате образования щели (зазора) между двумя поверхностями, по крайней мере одна из которых металлическая.

| |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| Кислородные концентрационные элементы существуют в щелях (зазорах), а также в зонах ватерлинии на участках со сцепленными осадками (отложениями) и значительными углублениями, которые препятствуют диффузии кислорода и создают разности концентраций раствора. Концентрационные элементы, возникающие из-за различной концентрации ионов металла, подобно кислородным концентрационным элементам, стремятся сократить различие концентраций. Так, когда раствор над одним участком металла содержит больше ионов металла, чем над другим, металл переходит в раствор там, где концентрация ионов ниже. | Уменьшать до необходимого минимума зазоры, в особенности в зонах теплообмена или там, где водные среды содержат неорганические соединения (в растворенном виде) или растворенный кислород. При конструировании избегать острых углов, а также возможности образования застойных зон. Стремиться к полному дренажу и обеспечивать однородность среды. Предотвращать доступ коррозионных агентов в зазоры путем улучшения подгонки при сборке, употребления непроницаемых уплотнительных материалов, капсулирования, обертывания и уплотнения. Избегать щелевого эффекта между изоляцией и подложкой. Вместо болтовых и заклепочных соединений применять стыковые сварные швы. | ||||||||||||||||||||||||||||||||||
| Эрозионная коррозия | |||||||||||||||||||||||||||||||||||
Эрозионная коррозия – это коррозионная реакция, ускоренная истирающим действием при быстром относительном перемещении среды; истирающее действие обычно достигается присутствующими в среде твердыми частицами.
Ударная коррозия – локализованная, коррозия, возникающая вследствие непосредственного воздействия и эрозии (совместно и по отдельности) при столкновении жидкости с поверхностью, столкновении жидкости с
поверхностью.
| |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| Ударная коррозия возникает под действием водяного потока, разрушающего коррозионные окисные пленки и растворяющего металл; причиной разрушения под действием струи пара является скорость влажного пара. Действие ударной коррозии зависит главным образом от скорости жидкости, количества содержащегося в ней воздуха или числа твердых частиц, а также всех других факторов, влияющих на скорость образования защитных пленок. | Снижать скорость потока жидкости и обеспечивать условия ламинарного течения. Регулировать содержание воздуха в жидкой среде в соответствии со стойкостью металла. Создавать условия безвихревого течения; избегать конструктивных форм, вызывающих турбулентность или сужение потока. Сводить к минимуму резкие изменения в направлении потока. Выравнивать трубные секции. Скруглять входные и выходные кромки. Увеличивать толщину стенок материала в уязвимых местах. Подбирать соответствующие материалы. | ||||||||||||||||||||||||||||||||||
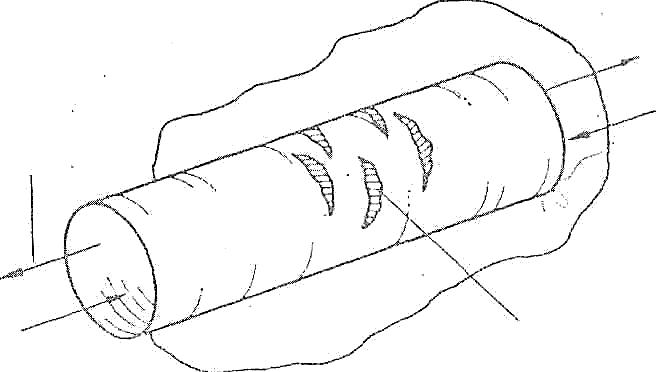
| Коррозионная усталость | |||||||||||||||||||||||||||||||||||
Разрушение, вызываемое приложением переменных нагрузок в присутствии коррозионной среды и протекающее в форме растрескивания.
| |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| В значительной степени подобно тому, как при сочетании статических напряжений с коррозией возникает коррозионное растрескивание, при сочетании циклических возникает коррозионная усталость. нагрузок с коррозией Она выражается в разрушении металла, происходящем при существенно более низком пределе усталости, чём в некоррозионных условиях. Эффект разрушения при комбинированном воздействии коррозии и циклической нагрузки больше, чем сумма соответствующих эффектов при отдельном воздействии коррозии и циклической нагрузки. | Максимально уменьшать или устранять циклические нагрузки. Увеличивать размеры, массу или локальную прочность в критических сечениях. Уменьшать концентрацию напряжений или перераспределять их. Придавать обтекаемую форму галтелям для уменьшения концентрации напряжений. Распределять напряжения и деформации по всему конструктивному элементу. Выбирать правильную форму критических сечений. Изменять форму и размеры деталей с целью перераспределения неиспользуемого материала в незагруженных элементах па находящиеся под критической нагрузкой сечения. | ||||||||||||||||||||||||||||||||||
| Фреттинг-коррозия | |||||||||||||||||||||||||||||||||||
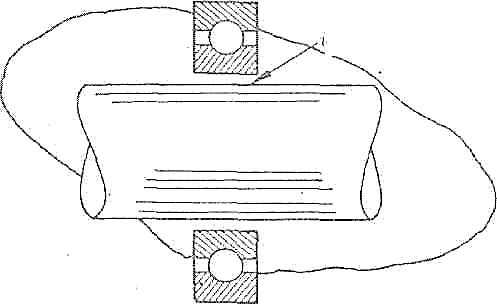 Локализованное разрушение на поверхности раздела между двумя контактирующими поверхностями, ускоряемое относительным движением с амплитудой, достаточной для обеспечения скольжения одной поверхности относительно другой. Локализованное разрушение на поверхности раздела между двумя контактирующими поверхностями, ускоряемое относительным движением с амплитудой, достаточной для обеспечения скольжения одной поверхности относительно другой.
| |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| Эта коррозия развивается при тесном контакте двух поверхностей, обычно находящихся под достаточно большой нагрузкой иподвергающихся очень слабому относительному движению (малейшие скольжения, вызываемые вибрациями высокой частоты). Различия в упругой деформации поверхностей могут быть достаточной причиной для возникновения в этих условиях фреттинг-коррозии, которая, по-видимому, вызывается сваркой контактирующих выступов с последующим их разрушением. Местное воздействие может вызывать образование усталостных трещин, особенно при концентрации напряжений или наличии питтинга на сопряженных поверхностях. Изнашивание поверхностных защитных пленок может вызывать контактную коррозию и коррозию, обусловленную работой концентрационного элемента. | Устранять конструктивные элементы, передающие вибрацию. Вводить барьер между металлами, скользящими относительно друг друга. Увеличивать сжимающую нагрузку (но не перегружать!) до прекращения взаимного скольжения. Подбирать соответствующие материалы. Предусматривать защитные покрытия из пористого (удерживающего смазку) материала. Изолировать движущиеся детали от неподвижных. Увеличивать абразивную устойчивость сопряженных поверхностей специальной обработкой одной из них или обеих. Обеспечивать недоступность опорных поверхностей для кислорода. Подбирать совместимые материалы. Улучшать смазку путем обеспечения лучших условий поступления смазочных материалов. Обеспечивать смывание мельчайших обломков (окисных пленок и металла), используя движение смазки. Подбирать соответствующие смазки. | ||||||||||||||||||||||||||||||||||
| Контактная коррозия | |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| Когда два различных металла, помещенных в электропроводную среду, находятся в непосредственном контакте либо электрически соединены проводником или проводящей средой, происходит преимущественное разрушение одного из металлов, являющегося анодным, тогда как коррозия другого, являющегося катодным, тормозится или прекращается совсем. | Избегать гальванопар (если они не необходимы по конструктивным соображениям), иначе обеспечивать полную электрическую изоляцию одного металла от другого. Для такой изоляции подбирать подходящие и эффективные материалы. Избегать неблагоприятного эффекта, вызываемого сочетанием малого анода с большим катодом. Увеличивать расстояние между неодинаковыми металлами в проводящей среде. Избегать размещения гальванопар из разнородных металлов в пористых, поглощающих влагу материалах. Предусматривать нанесение эффективных непористых покрытий, в особенности на катодные поверхности контактных пар. | ||||||||||||||||||||||||||||||||||
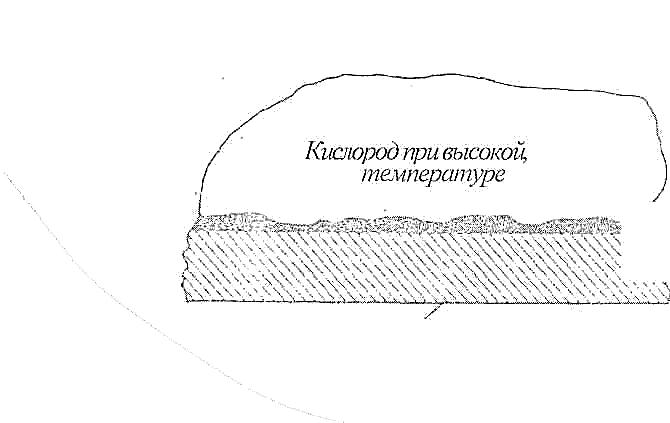
| Высокотемпературная коррозия | |||||||||||||||||||||||||||||||||||
Коррозия, связанная с влиянием атмосферных условий, различных газов, расплавленных металлов и солей при высоких температурах.
| |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| Вызывается воздействием высоких температур и определяется составами основного металла и окружающей среды (газы, соли, металлические расплавы), температурой и временем выдержки. Сильно изменяет свою скорость и формы в зависимости от этих факторов. На металлах с малым удельным весом (меньшим удельного веса их окислов) образуется слой, который не является защитным и утолщается с течением времени. Этот слой затем отслаивается и образуется вновь. | Выбирать стойкие материалы. Подбирать оптимальные температуры и составы сред. Регулировать продолжительность нежелательного контакта изделия с агрессивной средой. | ||||||||||||||||||||||||||||||||||
| Водородное разрушение | |||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| Механическое повреждение металла, обусловленное присутствием водорода или взаимодействием с ним. Водородное вспучивание и водородное охрупчивание вызывается внедрением атомарного водорода в металл. Обезуглероживание вызывается водородом при высоких температурах. Дезинтеграция кислородсодержащего металла в присутствии водорода называется водородной болезнью. Появление водорода связано с технологическими операциями обезжиривания, травления, катодной защиты, сварки. | Использовать металл с чистой поверхностью. Использовать устойчивый (монометаллический или плакировочный) металл. Использовать сварочные электроды с низким содержанием водорода в обмазке и обеспечивать проведение сварки в сухих условиях. Обеспечивать правильную подготовку поверхности и ее обработку. Исключать ошибки при выполнении операций травления и нанесения металлопокрытий. Обеспечивать металлизацию водородостойким металлом или использовать биметалл с соответствующей водородостойкой плакировкой. Удалять водород из металла горячей сушкой (93—149°С). Обеспечивать контроль за химическим составом, среды (применение ингибиторов, устранение сульфидов, соединений мышьяка, цианидов и фосфорсодержащих ионов). | ||||||||||||||||||||||||||||||||||
| Межкристаллитная коррозия | |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| По ряду причин происходит избирательное разъедание и межкристаллитное растрескивание вдоль границ между зернами металла. В некоторых аустенитных нержавеющих сталях в процессе охлаждения после сварки происходит выпадение карбидов хрома па границах между зернами. Коррозия разрушает участки, обедненные хромом (разрушение швов, ножевая коррозия). | Подбирать материалы, не склонные к обеднению границ между зернами (стабилизированные). Подбирать соответствующий режим термообработки (высокотемпературный гомогенизирующий отжиг). Избегать назначения технологических режимов термической обработки или сварки в опасном температурном интервале с точки зрения склонности к межкристаллитной коррозии. | ||||||||||||||||||||||||||||||||||
| Микробиологическая коррозия | |||||||||||||||||||||||||||||||||||
| Разрушение материалов, вызываемое как непосредственно, так и косвенно жизнедеятельностью бактерий, плесени или грибков. | |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| Микробы (бактерии, грибки, плесень) вызывают коррозию в результате: a) химического воздействия на металлы, бетон и другие материалы побочными продуктами жизнедеятельности микробов, а именно кислотами (например, серной, угольной и другими органическими кислотами), сероводородом или аммиаком; b) бактериального воздействия па органические материалы (например, органические лакокрасочные покрытия), некоторые природные неорганические вещества (например, серу) или ингибиторы; c) активации поверхности металла и образования коррозионных элементов; d) разрушения металла в результате процесса, при котором микробы и металл одновременно участвуют в коррозионной реакции: e) разъедания вследствие жизнедеятельности разных бактерии. | Тщательно анализировать возможность заражения среды микроорганизмами, вызывающими коррозию. Обеспечивать химический контроль состава среды. Производить ингибирование или добавлять гермициды. Поддерживать среду неагрессивной или обеспечивать контролируемое удаление из нее питательных для микробов веществ. Подбирать соответствующие стойкие материалы. Подбирать подходящие защитные покрытия. Применять катодную защиту. Предусматривать возможность частых очисток. | ||||||||||||||||||||||||||||||||||
| Питтинг (точечная коррозия) | |||||||||||||||||||||||||||||||||||
Самокатализируемая локализованная коррозия, при которой происходит прогрессирующее проникновение вглубь металла с образованием изъязвлений.

| |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| Локализованная коррозия в форме питтинга возникает при разрушении защитной пленки или слоев продуктов коррозии. По месту разрушения пленки образуется анод, а неразрушенная пленка (или продукты коррозии) становится катодом. Точечные разрушения образуют начальные точки концентрации напряжений, вследствие чего могут возникнуть или ускориться разрушения паза коррозионного растрескивания или коррозионной усталости. | Подбирать соответствующие стойкие материалы. Выбирать соответствующие геометрические формы для предотвращения условий, способствующих возникновению питтинга (увеличивать скорость потока). Устанавливать толщину стенки изделия с учетом глубины язвины. Обеспечивать контроль химического состава среды (не полагаться только на одни ингибиторы, если с их помощью разъедание по может быть полностью остановлено). Предусматривать защитные покрытия (улучшать текстуру поверхности). Обеспечивать образование непрерывной и прочной защитной пленки. | ||||||||||||||||||||||||||||||||||
| Селективная (избирательная) коррозия | |||||||||||||||||||||||||||||||||||
Процесс удаления растворимого компонента из сплава с нерастворимым компонентом при воздействии на сплав растворителя – обычно водной среды.

| |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| Один элемент из сплава выделяется в основном в результате коррозионного разъедания. Часто встречающимися видами селективной коррозии являются обесцинкование, обезалюминирование и графитизация. Например, когда медпоцинковые сплавы (латуни), содержащие менее 85% меди, подвергаются воздействию влажной среды в течение продолжительных периодов времени, цинк может перейти в раствор. Осаждающаяся на поверхность сплава медь имеет ничтожную механическую прочность. | Выбирать стойкие материалы. Снижать агрессивность среды. Использовать катодную защиту. | ||||||||||||||||||||||||||||||||||
| Коррозия блуждающими токами (электролиз) | |||||||||||||||||||||||||||||||||||
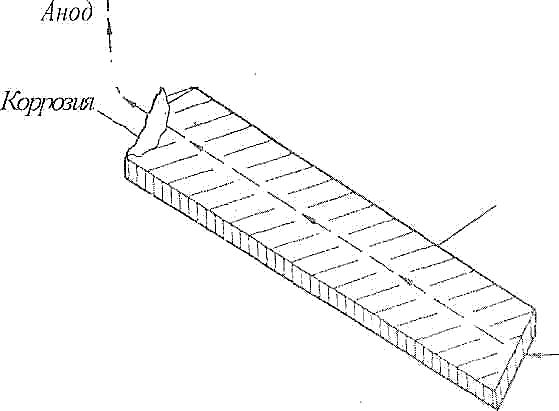 Коррозия этого типа обычно возникает при прохождении постоянного тока по путям, не предусмотренным спроектированной цепью. Коррозия этого типа обычно возникает при прохождении постоянного тока по путям, не предусмотренным спроектированной цепью.
| |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| Электролитическая коррозия обусловлена протеканием неконтролируемых электрических токов (большей частью постоянного тока высокого напряжения) от посторонних источников по непредусмотренным путям. Например, плохое заземление электрических машин, выпрямителей и т. п. приводит к утечкам тока через металлические конструкции и другие токопроводящие пути и вызывает коррозию электрически соединенных конструкций и оборудования. | При конструировании электрических цепей и оборудования предусматривать, чтобы все детали и приборные доски из электропроводных материалов постоянно имели потенциал земли. Изолировать электрические кабели и электрическое оборудование от элементов конструкций. Обеспечивать контролируемое оборудование заземление электрического оборудования. Применять неэлектропроводные среды. Отводить блуждающие токи с помощью другого проводника. При необходимости применять катодную защиту. Выбирать соответствующее расположение сооружений и деталей; устранять источники блуждающих токов. Окружать сооружения или детали инертной неэлектропроводной средой, предотвращая тем самым доступ блуждающим токам. | ||||||||||||||||||||||||||||||||||
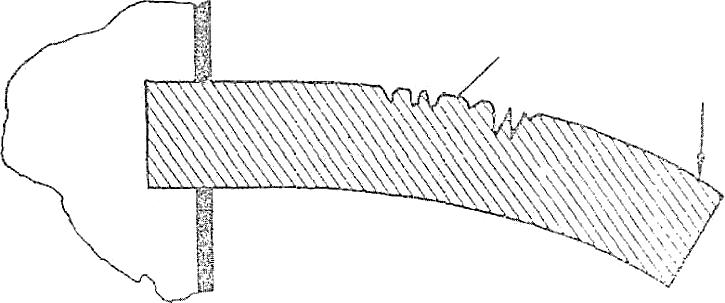
| Коррозионное растрескивание | |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| Причины | Мероприятия по защите | ||||||||||||||||||||||||||||||||||
| Коррозионное растрескивание происходит при одновременном воздействии значительных растягивающих напряжений и коррозионной среды (см. таблицу). Растягивающие напряжения возникают на поверхности металла при статической нагрузке. Коррозионное воздействие приводит к концентрированию напряжений и превышению ими предела текучести металла. При достаточно длительной выдержке сочетание коррозии металла с высокими локальными концентрациями напряжений приводит в конечном счете к потере прочности. Неметаллы также проявляют сходные особенности поведения. | Сводить к минимуму приложенные или остаточные растягивающие напряжения.
Обеспечивать достаточную эластичность.
Увеличивать размеры опасного сечения.
Снижать концентра
Воспользуйтесь поиском по сайту:  ©2015 - 2026 megalektsii.ru Все авторские права принадлежат авторам лекционных материалов. Обратная связь с нами...
|