 |
И при патологии (Владимиров Ю.Я., 1998)
|
|
|
|

Рис. 1.3.1.
Накопленные к настоящему времени данные литературы позволяют сделать вывод о том, что свободнорадикальное окисление липидов при сальмонеллезной инфекции играет определенную патогенетическую роль [25, 50].
Установлено, что при развитии ПОЛ в биомембранах понижается содержание легкоокисляемых полиненасыщенных жирных кислот и изменяются физико-химические свойства: микровязкость, текучесть, мембранный потенциал, полярность внутренних областей мембран. Таким образом, изменяются транспортные свойства мембраны и активность ферментов [26].
Регуляция свободнорадикального окисления обеспечивается в клетке системой антиоксидантной защиты. Так, накапливающаяся в процессе ПОЛ перекись водорода обезвреживается с помощью каталазы, присутствующей во всех тканях организма. Каталаза (КФ 1.11.1.6.) представляет собой гемсодержащий фермент с молекулярной массой около 250000 Д, локализованный в пероксисомах клеток [27].
Митохондриальная каталаза участвует в оксидазном пути окисления, сопровождающемся запасанием энергии в виде АТФ. Блокирование транспорта электронов в дыхательной цепи приводит к стимуляции пероксисомального окисления. При потологиях, связанных с нарушением энергетических процессов, каталаза пероксисом может выходить из них и участвовать в окислении на мембранах эндоплазматического ретикулума [28, 53].
В работе Л.Б. Оконенко с соавторами о состоянии антиоксидантной системы судили по активности СОД, глутатионпероксидазы и каталазы, анализ данных выявил дефицит антиоксидантов [29, 30].
При инфекционном токсикозе в мембранах эритроцитов резко снижается содержание общих фосфолипидов, но увеличивается количество НЭЖК и лизофосфотидилхолина, что косвенно указывает на повышение активности фосфолилаз, которые избирательно разрушают липиды мембран. Холестерин подвергается как активному, так и пассивному обмену в мембранах эритроцитов [29]. Фермент лецитинхолестеролацил трансфераза превращает эфиры холестерина в свободный холестерин и тем самым регулирует уровень свободного холестерина в плазме, что способствует проникновению его в мембраны. Следовательно, инактивация этого фермента в результате гипоксии при эндотоксикозе ведет к повышению уровня эфиров холестерина в мембранах эритроцитов [31,32].
|
|
|
Наряду с уровнем МДА, активности каталазы и уровня холестерина для диагностики заболевания и его прогноза имеют значение и другие неспецифические показатели – ЦИК, Ит, МСМ.
Синтезирующиеся при формировании иммунитета специфические антитела обладают способностью взаимодействовать с антигенами возбудителей и тем самым вызывать нейтрализацию патогенных микробов и их токсинов. Эта реакция сопровождается образованием иммунных комплексов антиген – антитело [33, 34, 54, 55]. При патологических состояниях образование ИК выходит из под контроля, в результате чего развивается та или иная болезнь ИК [рис. 1.3.2.].
Патогенетические механизмы болезней иммунных
Комплексов (Сура В.В., 1987)
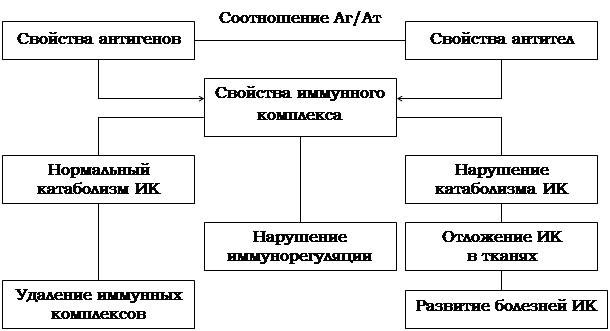 |
Рис. 1.3.2.
В результате развития эндотоксемии при сальмонеллезе организм длительное время контактирует с избытком АГ как экзогенного (компоненты микробных клеток), так и эндогенного (компоненты разрушенных клеток самого организма) происхождения. Вместе с тем наблюдается угнетение системы комплемента, ответственного за лизис микробных клеток. В этих условиях значительного избытка АГ и недостаточности выработки АТ может привести к образованию ИК, которые способны откладываться в определенных тканях и вызывать острые воспалительные реакции. При значительных отложениях наблюдаются функциональные и морфологические повреждения органов и тканей [35].
|
|
|
Связываясь с клеточной мембраной ЦИК вызывают выделение в окружающую среду протеолитических ферментов и основных пептидов. Эти вещества повреждают протеогликановые компоненты тканей, действуют на базальную мембрану и вызывают некроз эндотелиальных клеток [36].
ЦИК наряду с продуктами ПОЛ вызывают нарушение проницаемости мембран, вплоть до их разрыва, что в конечном итоге может привести к гибели клетки. В результате появляются различные вещества пентидной природы. Из них наибольший интерес представляют молекулы средней массы.
Являясь олигопептидами с молекулярной массой 300-5000 Дальтон, они расцениваются как универсальный критерий эндогенной интоксикации и влияют на ее уровень и прогноз [37, 38].
МСМ образуются в организме под воздействием повреждающих эндогенных или экзогенных факторов различного генеза, являются промежуточными продуктами протеолиза. [39, 57].
Пристальное внимание исследователей к МСМ объясняется высокой биологической активностью их отдельных фракций, которые ингибируют гликолиз, глюконеогенез, пентозный цикл, синтез гемоглабина, нуклеиновых кислот, мембранный транспорт, дагоцитов, эритропоэз, микроциркуляцию, обладают иммунодепрессивным, цитотоксическим, нейро- и психотропным свойствами. Сейчас, квалификационная оценка степени тяжести состояния больных при сальмонеллезе немыслима без определения МСМ [40].
Установлено, что значительная часть циркулирующих в крови СМ не только растворена в плазме крови, но и связана с альбумином.
Человеческий сывороточный альбулин (ЧСА) – важнейший транспортный белок, осуществляющий перенос эндогенных метаболитов и ксенобиотиков в плазме крови, межклеточной жидкости, в лимфе.
Универсальность транспортной функции ЧСА обеспечивается его уникальной способностью связывать лиганды различной химической природы. Интенсивная лигандная нагрузка молекул альбулина приводит к изменению их структуры и связывающей способности. Такие модификационные формы ЧСА обнаруживаются при патологии [41].
|
|
|
О величине токсического действия вредных веществ можно судить по ЭКА, которая снижается после того, как токсические вещества займут центры связывания в молекуле альбулина, что приводит к снижению детоксикационных свойств организма. Изучение свойств альбулина является важным с точки зрения как диагностики, так и лечения [42].
2. Материалы и методы исследований
2.1. Материал исследований
Уровень интоксикации оценивался по изменениям в крови больных эффективной и общей концентраций сывороточного альбулина, малонового диальдегида, как одного из продуктов ПОЛ, уровня холестерина, ЦИК, МСМ и активности каталазы.
Для всех исследований бралась сыворотка крови. Исследовано 30 больных сальмонеллезом в возрасте от 17 до 46 лет. Для контроля набиралась группа 51 человека разного пола в возрасте от 20 до 46 лет.
Кровь бралась из локтевой вены, преимущественно натощак в количестве не менее 5 мл. Центрифугируем 1500 об/мин 10 минут. Для выполнения анализов сыворотки необходимо использовать сразу или заморозить и хранить при t=-20 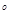 С.
С.
2.2. Методы исследований
2.2.1. Определение МДА с тиобарбитуровой кислотой
(Конюхова В.С., 1989)
Об изменении интенсивности ПОЛ судим по изменению уровня вторичного продукта ПОЛ – малонового диальдегида.
Метод основан на том, что при высокой температуре в кислой среде МДА реагирует с 2-ТБК, образуя окрашенный розовый триметиновый комплекс с максимумом поглощения при 535 им.
Ход работы: К 0,2 мл сыворотки крови добавить 0,2 мл дистиллированной воды, 1 мл 0,6 % ТБК в ледяной уксусной кислоте. Кипятить 30 минут, охладить и добавить 1 мл 5№ КОН и 2 мл изопропанола. Центрифугируют при 6000 об/мин 20 минут. Колориметрируют при 535 нм и 580 нм против контроля, содержащего вместо плазмы воду.
Расчет: 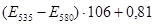 (мкМоль/л), где Е – оптическое поглащение изопропилового экстракта; 106 – коэффициент пересчета оптической плотности.
(мкМоль/л), где Е – оптическое поглащение изопропилового экстракта; 106 – коэффициент пересчета оптической плотности.
Пример расчета: больной Максимов С., 19 лет
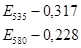
концентрация МДА = 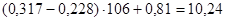 (мкМоль/л).
(мкМоль/л).
2.2.2. Определение активности каталазы
(Королюк М.А., 1988)
Метод основан на способности перекиси водорода образовывать с солями молибдена стойкий окрашенный комплекс.
|
|
|
Ход определения: Реакция запускается добавлением 0,1 мл сыворотки крови к 2 мл 0,03 % раствора перекиси водорода. В холостую пробу вместо сыворотки вносят 0,1 мл дистиллированной воды. Реакцию останавливают через 10 минут добавлением 1 мл 4% молибдата аммония. Интенсивность окраски измеряют на спектрофотометре при длине волны 410 нм против контрольной пробы, в которой вместо перекиси водорода вносят 2 мл воды.
Расчет:  (мкат/л), где
(мкат/л), где
Е – активность каталазы в мкат/л;
А – оптическая плотность холостой и опытной проб;
V – объем вносимой пробы, 0,1 мл;
t – время инкубации, 600 сек;
К – коэффициент миллимолярной экстинкции перекиси водорода, равный 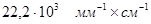 .
.
За единицу активности каталазы принимают то количество фермента, которое участвует в превращении 1 мкат перекиси водорода за 1 секунду при заданных условиях. Расчет активности каталазы ведут на 1 л сыворотки крови.
Пример расчета: больной Крайнов Т.В., 31 год.
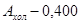
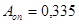
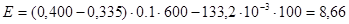 (мкат/л)
(мкат/л)
2.2.3. Определение общего холестерина в сыворотке крови ферментативным методом «Фотокол»
(Творогова М.Г., 1995)
Определение основано на сопряженных реакциях, которые катализирует холестеринэстераза, холесериноксидаза и пероксидаза:
Эфиры холестерина 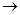 холестерин + Ж.К.;
холестерин + Ж.К.;
Холестерин + О2  холестинон + Н2О2;
холестинон + Н2О2;
Н2О2 + хромогены  Н2О + окрашенный продукт.
Н2О + окрашенный продукт.
Концентрация образующегося в ходе реакции окрашенного продукта пропорциональна концентрации холестерина в пробе.
Ход определения: Рабочий реагент обязательно вносить в пробирки после проб, содержащих холестерин. Пробирки встряхнуть и инкубировать при t = 37oС. Через 10 минут после начала инкубации пробирки повторно встряхнуть и инкубировать 20 минут при t = 37oС. Окрашенные пробы фотометрировать при 500 нм в кювете с длиной оптического пути 5 мм или 10 мм относительно холостой пробы. Окраска стабильна в течении двух часов при комнатной температуре.
Концентрацию холестерина в исследуемых пробах рассчитать по формуле:
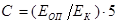 ммоль/л, где
ммоль/л, где
ЕОП и ЕК – оптические плотности исследуемой пробы и пробы с калибратором.
Норма: 3,62 – 5,2 ммоль/л.
2.2.4. Определение циркулирующих иммунных комплексов
в крови методом ПЭГ-теста (Гриневич Ю.А., 1988)
Метод основан на селективной преципитации комплексов АТ-АГ в 3,75 % ПЭГ (полиэтиленгликоля) с последующим определением плотности преципитата.
Реактивы:
1) 0,1 м боратный буфер (3,410 г борной кислоты, 4,275 г буры растворить в 1 л дистиллированной воды)
2) 10 г полиэтиленгликоль – 6000 ед. растворить в 240 мл буфера.
Ход определения: К 0,3 мл сыворотки крови добавить 0,6 мл реактива №1, перемешать и перенести по 0,3 мл в 2 пробирки. В I добавить 2,7 мл раствора №1 (контроль). Во II добавить 2,7 мл раствора №2 (опыт). Перемешать, инкубировать в течение 60 минут при комнатной температуре. На спектрофотометре (КФК-3) определяют оптическую плотность в кюветах 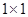 при 450 нм.
при 450 нм.
|
|
|
Расчет: Высчитывают разность показателей оптической плотности, результат умножают на 1000 и получают количество ИК в 100 мл сыворотки. Ответ выражают в единицах оптической плотности. 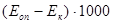 - количество ЦИК в 100 мл сыворотки.
- количество ЦИК в 100 мл сыворотки.
Норма: 54,24 + 2,03 усл. ед.
Пример расчета: больной Максимов С.И., 19 лет.
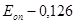
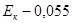
Количество ЦИК в 100 мл сыворотки:
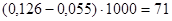 усл. ед.
усл. ед.
2.2.5. Определение уровня МСМ в крови (Габриэлен Н.И., 1984)
Метод основан на осаждении белков из исследуемой жидкости 10 % раствором ТХУ с последующем центрифугированием и определением абсорбции света супернатантом в 10 раз разведенным дистиллированной водой.
Ход работы: Сыворотку крови обрабатывают 10 % раствором ТХУ. В качестве контроля лучше использовать сам раствор ТХУ в 30 раз разведенный дистиллированной водой. Оптическая плотность его против воды составляет 0,123±0,012 усл. ед. на волне 254 нм при 23-25 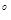 С. Центрифигируем 3000 об/мин в течение 30 минут. К 0,5 мл надосадочной жидкости +4,5 мл дистиллированной воды. Измерение проводим на спектрофотометре в УФ свете при 280 нм для определения ароматических аминокислот и при длине волны 254 нм для определения нуклеотидов. Уровень МСМ выражают в единицах, количественно равных показателям экстинции.
С. Центрифигируем 3000 об/мин в течение 30 минут. К 0,5 мл надосадочной жидкости +4,5 мл дистиллированной воды. Измерение проводим на спектрофотометре в УФ свете при 280 нм для определения ароматических аминокислот и при длине волны 254 нм для определения нуклеотидов. Уровень МСМ выражают в единицах, количественно равных показателям экстинции.
2.2.6. Определение показателей «эффективная концентрация
альбумина» и «общая концентрация альбумина» в сыворотке крови человека флуоресцентным методом
(Миллер Ю.И., 1994).
Принцип метода:
Метод основан на специфическом взаимодействии флуоресцентных органических соединений с альбумином в сыворотке крови. В зависимости от условий этого взаимодействия интенсивность флуоресценции красителя из альбумина отражает различные свойства белка. Индекс ЭКА/ОКА не зависит от числа молекул альбумина в пробе и характеризует физико-химические свойства молекулы альбумина.
Состав набора:
Реактив I (4 ампулы по 5 мл). Предназначен для приготовления раствора используемого при разбавлении сыворотки крови. Он содержит антикоагулянт ЭДТА.
Реактив II (4 ампулы по 0,7 мл). Основным компонентом является специальное флуоресцирующее соединение, интенсивность флуоресценции которого в сыворотке крови пропорциональна концентрации сывороточного альбумина.
Реактив III (4 ампулы по 0,7 мл). Взаимодействие реактивов №2 и №3 с сывороткой позволяет определить ОКА.
Определение показателя ЭКА:
К 2,0 мл надосадочной жидкости добавить 0,025 мл реактива 2. Перемешать. Измерить интенсивность флуоресценции при длине волны возбуждения 420 нм и длине волны испускания 515 нм.
Определение показателя ОКА:
В ту же пробу добавить 0,025 мл реактива 3. Перемешать. Измерить интенсивность флуоресценции. Нормальные величины показателя ЭКА лежат в интервале нормальных значений ОКА от 40 г/л – 55 г/л.
Подготовка образцов крови к измерениям:
Буферный раствор: Содержимое ампулы с реактивом 1 перенести в 100 мл дистиллированной воды. Перемешать. 0,025 мл сыворотки крови добавить в пробирку, содержащую 5 мл раствора для разбавления крови. Для анализа берут жидкость 2,0 мл полученного образца.
Используют специализированный анализатор АКЛ-0,1.
3. Результаты исследования и их обсуждение
3.1. Определение показателей уровня интоксикации
в сыворотке крови практически здоровых людей
Нами было произведено исследование биохимических показателей – МДА, активность каталазы, уровень холестерина, ЦИК, МСМ, Ит в сыворотке крови 51 донора в возрасте от 20 до 46 лет. Сыворотка крови доноров была получена на ОСПК (областная станция переливания крови) г. Пензы.
Полученные результаты биохимических анализов были подвергнуты статистической обработке, согласно методам и приемам статистического анализа.
По данным комитета экспертов Международной федерации клинической химии по референтным величинам рекомендуется верхняя и нижняя границы нормы на уровне М±1,96σ, состояние предболезни М±2σ, состояние острой формы М±3σ.
Об уровне процессов ПОЛ судили по концентрации вторичного продукта МДА. Содержание количества МДА составляет 3,61±0,07 мкМоль/л. Это значение близко к данным, найденным в литературе (табл. 3.1.1). У 48 человек значение содержания МДА входит в границы М±1,96σ. У 3 человек (5 %) содержание МДА соответствует значению М±2σ, что соответствует состоянию предболезни.
Активность каталазы у практически здоровых людей составила 16,7±0,15 мкат/л (табл. 3.1.1). При исследовании активности каталазы в группе доноров отклонений за пределы М±1,96σ мы не наблюдали.
Уровень холестерина, определяемый нами у практически здоровых людей составил 4,45±0,68 ммоль/л (табл. 3.3.1.), показатели уложились в границу референтной величины М±1,96σ.
Содержание ЦИК, определяемое нами в сыворотке крови практически здоровых людей составило 52,62±3,52 усл. ед. (табл. 3.1.1). 94 % людей по показателям ЦИК входит в границы нормы, а 6% находятся в состоянии предболезни.
Уровень МСМ у обследованных доноров в среднем составил 0,280±0,01 усл. ед. Это значение близко к данным, найденным в литературе (табл. 3.1.1). При исследовании МСМ отклонений за пределы М±1,96σ мы не наблюдаем.
У практически здоровых людей определена детоксикационная нагрузка сывороточного альбумина, т.е. определение общей и эффективной концентрации альбумина. Токсичность по альбумину составляет 0,13±0,01 усл. ед. (табл. 3.1.1). Все значения токсичности по альбумину вошли в границы М±1,96σ.
Полученные нами данные не имели существенных отличий от значений этих показателей, имеющихся в литературе в сравнении с приложением 2.
Таблица 3.1.1.
Содержание биохимических показателей в сыворотке крови практически здоровых людей
| Группа обследованных | n | МДА мкМоль/л | Активность каталазы мкат/л | ЦИК усл. ед. | МСМ усл. ед. | Ит усл. ед. | Холестерин ммоль/л |
| Практически здоровые | 51 | 3,61±0,07 | 16,7±0,15 | 52,62±3,52 | 0,28±0,01 | 0,13±0,01 | 4,45±0,68 |
3.2. Определение показателей уровня интоксикации
в сыворотке крови больных сальмонеллезом
Сыворотка крови больных исследовалась на базе центра госсанэпиднадзора г. Пензы. Исследования биохимических показателей велись в острую фазу заболевания и в период ранней реконвалесценции. Обследовано нами 30 больных сальмонеллезом в возрасте от 17 до 46 лет, с целью установления показателей, характеризующих эндотоксикоз: перекисное окисление липидов, уровень холестерина, Ит по сывороточному альбумину, циркулирующих иммунных комплексов, молекул средней массы и активности каталазы. Причем биохимические показатели крови в разгар заболевания отличались от показателей в период ранней реконвалесценции.
Таблица 3.2.1.
|
|
|


