 |
Получение N,N,N’N’-тетраметилдиаминометана
|
|
|
|
В работе [6] был предложен метод синтеза N,N,N’N’-тетраметилдиаминометана (или бис -(диметиламино)-метана) из формальдегида диметиламина. Для приготовления вещества реагенты смешивают в водном растворе при охлаждении в бане со льдом. После окончания реакции отделяют органический слой подщелачиванием гидроксидом калия. Этот слой далее отделяют, сушат над щелочью и перегоняют. Выход N,N,N’N’-тетраметилдиаминометана по данной методике составляет 77-85% от теоретического:
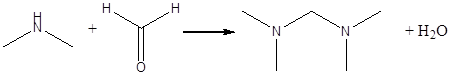
Также в работе [7] был описан метод получения бис -(диметиламино)-метана по следующей реакции с выходом 54% от теоретического:

N,N,N’N’-тетраметилдиаминометан можно получить по реакции, описанной Рудченко, Шевченко и Костяновским в [8], но с очень низким выходом (26%):

Ещё один синтез бис -(диметиламино)-метана из диметиламина был описан в работе [9]. Для получения этого вещества раствор диметиламина в дихлорметане нагревают до в водяной бане. После трёх часов реакции жидкую фазу выпаривают и далее разделяют при помощи фракционной перегонки.

Этот способ непрактичен, так как выход вещества небольшой (порядка 40-50%) в связи с протеканием побочных реакций.
2.5 Получение бис -(триметилсилил) фосфоната
В статье Воронкова, Колесовой и Згонник был описан простой метод получения триалкилсилиловых эфиров фосфористой кислоты [10]. По этому методу с выходом 57% от теоретического получается и бис -(триметилсилил) фосфонат (бис -(триметилсилил)-фосфит).

Для получения вещества избыток триметилхлорсилана и фосфористая кислота H3PO3 кипятились в колбе с обратным холодильником до прекращения выделения соляной кислоты. Далее полученный фосфонат отгонялся под вакуумом. Аналогичный способ был предложен в [11].
|
|
|
Также российскими учеными запатентован метод получения бис -(триметилсилил) фосфината из триметилхлорсилана и фосфина в третбутаноле с количественным выходом [12]:
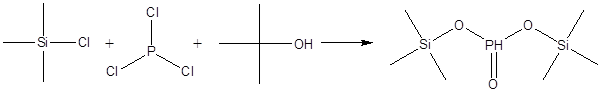
Экспериментальная часть
3.1 Синтез N,N,N’N’-тетраметилдиаминометана [6]
Поместили 30,5 г (0,38 моль) 37% раствора формальдегида в стакан на 600 мл, снабженный механической мешалкой и термометром. Стакан поместили в баню со льдом. К раствору медленно при сильном перемешивании прибавляли 135 г (0,75 моль) 25% водного раствора диметиламина так, чтобы температура реакционной смеси не поднималась выше 15 °С. После прибавления смесь перемешивали ещё 30 минут, после чего отдельными порциями прибавили 75 г гидроксида калия в гранулах до расслоения смеси. Верхний слой отделили, просушили над щелочью в течении 1 часа и перегнали. Получили 25 г (66% от расчета, 86% от методики) N,N,N’N’-тетраметилдиаминометана с температурой кипения 89 °С и 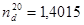 . (по литературным данным 82-84 °С и 1,4018 соответственно [13]).
. (по литературным данным 82-84 °С и 1,4018 соответственно [13]).
3.2 Синтез бис -(триметилсилил) фосфоната
48,9 г (0,45 моль) триметилхлорсилана, 12,3 г (0,15 моль) фосфористой кислоты H3PO3 кипятились с обратным холодильником до прекращения выделения хлороводорода. При фракционной перегонке реакционной смеси получено 16 г (51% от теории, 89% от методики) бис -(триметилсилил) фосфоната с температурой кипения 79 °С и  . (по литературным данным 74-75 °С и 1,4145 соответственно [10; 11]).
. (по литературным данным 74-75 °С и 1,4145 соответственно [10; 11]).
3.3 Синтез бис -(триметилсилил)-диметиламинометил фосфоната
Реакционную смесь, состоящую из 10 мл N,N,N’N’-тетраметилдиаминометана и 8 мл бис -(триметилсилил) фосфоната (двухкратный избыток N,N,N’N’-тетраметилдиаминометана), поместили в колбу Кляйзена, снабженную прямым холодильником, в которую предварительно положили кусочек безводного хлорида цинка, и кипятили до тех пор, пока температура смеси не поднялась до 160 °С. Перед помещением реагентов в колбу прибор продули в токе аргона во избежание гидролиза бис -(триметилсилил) фосфоната. Для предотвращения выпаривания реагентов прибор наклонили так, чтобы они свободно стекали из холодильника обратно в реакционную смесь.
|
|
|
После проведения реакции бис -(триметилсилил)-диметиламинометил фосфонат отгоняли под вакуумом (13 тор, температура кипения 112-114 °С). Получено 8,5 г конечного продукта (85% от теоретического выхода) с  .
.
Обсуждение результатов
Для получения бис -(триметилсилил)-диметиламинометил фосфоната мы провели следующий синтез, включающий синтез бис -(триметилсилил) фосфоната и диметиламина, по следующей схеме:

По приведенным в экспериментальной части работы методикам были синтезированы следующие вещества:
1. N,N,N’N’-тетраметилдиаминометан по реакции диметиламина с формальдегидом в водном растворе.
2. бис -(Триметилсилил) фосфонат при кипячении триметилхлорсилана с фосфористой кислотой.
3. Целевой бис -(триметилсилил)диметиламинометил фосфонат по реакции N,N,N’N’-тетраметилдиаминометана с бис -(триметилсилил) фосфонатом.
| Название и формула | Физические параметры | Выход | |||
| Полученные | Из литературных источников | В г. | В % | ||
| От методики | От теории | ||||
| N,N,N’N’-тетраметилдиаминометан | Ткип = 89 °С

| Ткип = 82-84 °С

| 25 | 86 | 66 |
| бис -(Триметилсилил) фосфонат | Ткип = 79 °С

| Ткип = 74-75 °С

| 16 | 89 | 51 |
| бис -(триметилсилил)-диметиламинометил фосфонат | Ткип = 112-114 °С (13 тор)

| - | 8,5 | - | 85 |
Для целевого продукта бис -(триметилсилил)-диметиламинометил фосфоната были зарегистрированы спектры 31P и 1H на приборе Brucker Avanse 400.
Спектр ЯМР 31P{1H} для бис -(триметилсилил)-диметиламинометил фосфоната (внутренний стандарт CD2Cl2): δP = … м. д. В спектре ЯМР 1H (внутренний стандарт CDCl3) целевого фосфоната имеется характеристичный дублет 2γPH = 12Гц, δ = 2,54 м. д. (область химических сдвигов, характерная для фосфонатов).
Выводы
1. Собрана и систематизирована литература по синтезу, физико-химическим и биологическим свойствам α-аминофосфоновых кислот и некоторых их производных
2. Осуществлен трехстадийный синтез бис -(триметилсилил)-диметиламинометил фосфоната. Его строение было подтверждено данными спектра ЯМР 31P и 1H.
|
|
|
Список литературы
1 Wozniak L., Chojnowski J. //Tetrahedron Lett., 1989 2465-2547.
2 Петров К. А., Чаузов В. А., Ерохина Т. С. //Успехи химии, 1974, Т. 43, 2046-2067.
3 Черкасов Р. А., Галкин В. И. //Успехи химии, 1998, Т. 67, 941-968.
4 Uziel J., Genet J. P. //Ж. орг. химии, 1997, Вып. 11, 1605-1617.
5 Кабачник М. М., Ливанцов М. В., Вейц Ю. А., Ливанцова Л. И. //Основы химии фосфорорганических соединений, ч. 2. Москва 2003, Хим. Фак. МГУ, 14-20.
6 … //Синтез органических препаратов, сб. 12. Москва 1964, 74.
7 Багдасарян Г. Б., Бадалян К. С., Шежранян М. А., Инджикян М. Г. //Арм. Хим. Ж., 1982, 35, Н. 6, 379-383.
8 Рудченко В.Ф., Шевченко В. И., Костяновский Р. Г. //Изв АН СССР Хим., 1986, Н. 3, 606-610.
9 … //Am. Soc., 47, 1351.
10 Воронков М. Г., Колесова В. А., Згонник В. Н. //Изв АН СССР Хим., 1957, Н. 11, 1364-1367.
11 Нифантеев Е. Е., Харшан М. А., Лысенко С. А. //Ж. Общей химии, 1993, Н. 4, 776-782.
12 Ближнюк Н. К., Бондарева Т. А., Протасова Л. Д., Емельянович А. М., Климова Т. А. //Патент № SU1578132.
13 Низамов И. С., Батиева Е. С., Альфонсов В. А., Мусин Р. З. Пудовик А. Н. //Phosph., Sulfur and Silicon and Relat. Elem., 55 (1991), N. 4, 229-237.
|
|
|
12 |


