 |
Подготовка энергии к использованию
|
|
|
|
(дыхание)
У растений источником энергии является солнечный свет, причем ответственными за производство АТФ являются хлоропласты. Энергия, которая оказывается запасенной в основном в углеводах, используется в дальнейшем клетками растений для обеспечения различных биологических реакций. Что же касается клеток животных, то энергия поступает к ним с пищей (сахарами и жирными кислотами). Чтобы эта энергия могла использоваться в процессе жизнедеятельности клеток, она должна быть подготовлена для использования. Каковы же механизмы, с помощью которых энергия, запасенная в глюкозе, трансформируется в клетках в доступную для использования форму АТФ?
Подготовка энергии к использованию, т. е. генерирование (извлечение) энергии из пищевых веществ осуществляется в процессе дыхания, под которым понимают окисление (расщепление) молекул-энергоносителей, т. е. «топливных» молекул, при котором роль конечного акцептора электронов выполняет О у а донором электронов является органическое или неорганическое соединение. Процесс подготовки энергии к использованию протекает в три последовательные стадии (рис. 71).
На первой стадии поступающие в клетки крупные молекулы полисахаридов гидролизуются до простых Сахаров. На этой стадии происходит разложение и других энергоносителей. В частности, жиры разлагаются на глицерол и жирные кислоты, белки гидро-лизуются до аминокислот. Однако на этой стадии высвобождение запасенной в пищевых веществах энергии все еще не происходит.
На второй стадии происходит распад малых молекул до еще более простых структур, играющих уже ключевую роль в метаболизме. Глюкоза превращается в ацетильную часть ацетил-КоА, являющегося производным кофермента А. В результате этих реакций образуются молекулы АТФ, но их еще мало. На уровне ацетил-КоА в метаболический путь могут вступать также жирные кислоты и аминокислоты.
|
|
|

Наконец, на третьей стадии происходит полное окисление ацетильного компонента ацетил-КоА до СОу На этой стадии образуется основная часть АТФ.
Процесс генерирования энергии в животных клетках (извлечения ее из субстрата) осуществляется с участием митохондрий и начинается с гликолиза (от греч. glycos — сахар и lysis — растворение), который представляет собой окисление глюкозы, заканчивающееся превращением этого углевода в пировиноградную кислоту и образованием АТФ. Уже давно установлено, что для дыхания в качестве акцептора электронов необходим кислород. Однако на первых этапах расщепления Сахаров кислорода не требуется. Окисление глюкозы начинается в анаэробных условиях дыхания (при отсутствии кислорода) с частичного расщепления ее шестиуглеродной молекулы и заканчивается образованием двух трехуглеродных молекул пировиноградной кислоты (рис. 72). Превращения глюкозы можно описать следующим уравнением:
C6H12O6 + 2Ф + 2АДФ ® 2СН3СНОНСООН + 2АТФ + 2Н2О
У большинства организмов гликолиз служит одним из центральных метаболических путей и состоит из десяти последовательных химических реакций, протекающих в цитоплазме (цитозол). Вначале глюкоза превращается через глюкозо-6-фосфат во фрукто-зо-1,6-дифосфат в результате фосфорилирования, катализируемого гексокиназой и фосфофруктозокиназой. Поскольку эти реакции еще сами нуждаются в АТФ, они являются подготовительными в образовании АТФ. В частности, на превращение каждой молекулы глюкозы в этих реакциях затрачивается по две молекулы АТФ.
На втором этапе фруктозо-1,6-дифосфат превращается с помощью альдолазы в дигидроксиацетонфосфат и глицераль-дегид-3-фосфат, которые взаимопревращаемы в реакциях, катализируемых триозофосфатизомеразой. Затем глицеральдегид-3-фосфат окисляется и фосфорилизуется, в результате чего превращается в высокоэнергетическое фосфатное соединение 1,3-дифосфоглицерат (1,3-БФГ). Это превращение катализируется глицеральдегид-3-фосфатдегидрогеназой.
|
|
|
 Поскольку 1,3-БФГ-ацилфосфат обладает высоким потенциалом переноса фосфатной группы, эта особенность используется для генерирования АТФ. Поэтому дальше происходит перенос фосфатной группы от ацилфосфатной группы 1,3-БФГ-ацилфосфата на АДФ, катализируемый фосфоглицераткиназой. В результате этого образуется молекула АТФ и 3-фосфоглицерат, т. е. на этом этапе происходит образование энергии.
Поскольку 1,3-БФГ-ацилфосфат обладает высоким потенциалом переноса фосфатной группы, эта особенность используется для генерирования АТФ. Поэтому дальше происходит перенос фосфатной группы от ацилфосфатной группы 1,3-БФГ-ацилфосфата на АДФ, катализируемый фосфоглицераткиназой. В результате этого образуется молекула АТФ и 3-фосфоглицерат, т. е. на этом этапе происходит образование энергии.
Последний этап гликолиза связан с превращением 3-фосфоглицерата в пируват и образованием второй молекулы АТФ. Этот этап осуществляется в реакциях трех типов. Первая реакция заключается во внутримолекулярной перестройке, связанной с превращением 3-фосфоглицера-та в 2-фосфоглицерат, катализируемым фосфоглицеромутазой.
В результате этой реакции происходит перемещение фосфатной группы. Во второй реакции происходит дегидратация 2-фосфоглицерата, катализируемая енолазой, в результате чего образуется фосфоенолпируват. При этом повышается потенциал переноса фосфатной группы енолфосфат обладает высоким потенциалом переноса фосфатной группы. В третьей (заключительной) реакции этого этапа гликолиза происходит перенос фосфатной группы, от фосфоенолпирувата к АДФ, катализируемый пируваткиназой. Это приводит к образованию пирувата и АТФ (второй молекулы).
При анаэробных условиях пировиноградная кислота превращается в молочную кислоту (лактат) или в этиловый спирт (этанол), или в пропионовую кислоту. Этот анаэробный процесс называют еще брожением. В данном случае речь идет о молочнокислом, спиртовом и пропионовом брожении (соответственно). Молочная кислота образуется из пирувата при метаболизме ряда микроорганизмов, а также в клетках мышц многоклеточных организмов. Суммарная реакция превращения глюкозы в лактат имеет следующий вид:
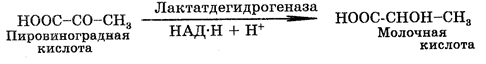
НАД×Н образуется в результате окисления глицеральдегид-3-фосфата, который используется при восстановлении пирувата.
|
|
|
В процессе превращения пировиноградной кислоты в лактат происходит регенерирование НАД+, что поддерживает непрерывность гликолиза в анаэробных условиях. Этиловый спирт образуется из пирувата при метаболизме дрожжей и некоторых других микроорганизмов спиртового брожения. Суммарная реакция превращения глюкозы в этанол имеет следующий вид:
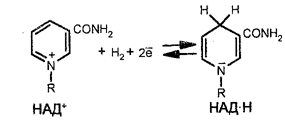
Глюкоза + 2Pi + 2АДФ + 2Н+ ® 2 этанол + 2СО2 + 2АТФ + 2Н20.
Восстановление ацетальдегида в этиловый спирт сопровождается регенерированием НАД+.
Анаэробное дыхание с точки зрения производительности не является эффективным процессом, т. к. при анаэробном превращении глюкозы в этанол или лактат освобождается лишь небольшое количество энергии. Большая часть энергии, запасенная в глюкозе, продолжает затем оставаться запасенной уже в молекулах этанола.
Как видно, последовательность реакций, в процессе которых глюкоза превращается в пируват, сходна в клетках всех видов у всех организмов. Биологическое значение гликолиза заключается в том, что он генерирует молекулы АТФ. В результате распада глюкозы образуются строительные блоки, используемые для синтеза клеточных структур. Оба эти процесса регулируются скоростью превращения глюкозы в пируват. Однако роль пирувата в генерировании энергии обмена веществ различна в разных клетках и разных организмах.
У аэробных организмов гликолиз, осуществляемый в цитозоле выполняет роль своего рода процесса-прелюдии к дальнейшему окислению, ибо при аэробном дыхании (в присутствии кислорода) окисление идет дальше и осуществляется уже в митохондриях в так называемом цикле Кребса (цикле трикарбоновых кислот или цикле лимонной кислоты) и в цепи переноса электронов, цикл Кребса является конечным путем окисления топливных молекул, причем не только глюкозы и других углеводов, но и жирных кислот и аминокислот (рис. 73). Следовательно, «топливом» для окисления в митохондриях являются пируват и жирные кислоты. Включение в этот окислительный путь осуществляется на уровне кофермента (ацетил-КоА), т. е. происходит с образования ацетил-КоА в митохондриаль-ном матриксе, в результате окислительного декарбоксилирования пирувата или распада жирных кислот до двухуглеродных групп. Ацетил-КоА обладает высоким потенциалом переноса ацетильных групп. Следовательно, топливные молекулы вступают в цикл Кребса в виде ацетил-КоА. Непрерывность же снабжения окислительных процессов «топливом» обеспечивается запасанием животными клетками липидов, являющихся главным ресурсом жирных кислот, а также гликогена, являющегося источником глюкозы.
|
|
|

Цикл Кребса действует только в аэробных условиях и начинается с конденсации ацетил-КоА (C2) и оксалоацетата (C4 с образованием цитрата (С6), изомеризация которого приводит к изоцитрату (C6). Затем следует окислительное декарбоксилирование изоцитрата и образование a-оксоглутарата (С5), после чего последний подвергается окислительному декарбоксилированию (выделяется вторая молекула CO2 в сукцинил-КоА (С4). В следующей реакции происходит расщепление тиоэфирной связи сукцинил-КоА в присутствии пирофосфата (Pi), в результате чего образуется сукцинат и генерируется высокоэнергетические фосфатные связи в форме ГТФ и АТФ.
Сукцинат потом окисляется в фумарат (С4), а последний гидратируется в малат. В последующей реакции происходит окисление малата, что приводит к регенерированию оксалоацетата (C4). Следовательно, в цикл Кребса вступают два атома углерода в виде ацетил-КоА и такое же количество атомов углерода покидают этот цикл уже в виде CO2 в последовательных реакциях декарбоксилирования, которые катализируются дегидрогеназами.


В результате четырех окислительно-восстановительных реакций цикла Кребса происходит перенос трех пар электронов над НАД и одной пары электронов на ФАД. Восстановленные этим путем переносчики электронов НАД и ФАД подвергаются затем окислению уже в цепи переноса электронов, в результате которого генерируется одиннадцать молекул АТФ. Одна высокоэнергетическая связь генерируется непосредственно в цикле Кребса. Таким образом, на каждый двухуглеродный фрагмент, полностью окисляемый до Н2О и СО2, генерируется двенадцать высокоэнергетических фосфатных связей.
Цикл Кребса подвержен регуляции; его скорость зависит от потребности в АТФ других метаболических реакций. Важное значение имеет регуляция синтеза цитратсинтазы, изоцитратдегидроге-назы и оксоглутаратдегидрогеназы.
Биологическое значение цикла Кребса заключается не только в том, что он является завершающим этапом в генерировании энергии, но и в том, что он «поставляет» промежуточные продукты для биосинтеза.
|
|
|
Цикл Кребса действует только в аэробных условиях по той причине, что для него необходимы НАД и ФАД, регенерирование которых происходит при переносе электронов НАД×Н и ФАД×H2 на О2 по цепи транспорта электронов, сопровождаемом одновременным образованием АТФ (рис. 74).
Поскольку у аэробных организмов единственным акцептором электронов является О2, а электроны не переносятся от топливных молекул и продуктов их реакций прямо на O2, топливные молекулы и продукты их распада переносят электроны к пиримидиннуклеотидам или флавинам, являющимся переносчиками.
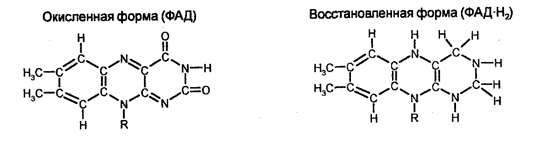
Главным акцептором электронов при окислении топливных молекул является никотинамидадениндинуклеотид (НАД+, реакционноспособной частью которого является никотинамидное кольцо. Последнее присоединяет ион водорода и два электрона. Восстановленной формой этого переносчика является НАД×Н. Окисление последнего дает три молекулы АТФ. Вторым акцептором электронов является ФАД (флавинадениндинуклеотид), ре-акционноспособной частью которого является изоаллоксазиновое кольцо, которое тоже присоединяет два электрона. Восстановленной формой ФАД является ФАД×H2. Окисление последнего дает две молекулы АТФ.
Таким образом, главными переносчиками являются НАД×Н и ФАД-Hg, которые содержат по паре электронов с высоким потенциалом и которые доставляют свои высокоэнергетические электроны к О3 по цепи транспорта электронов, также локализованной в митохондриях.
Этот перенос сопровождается образованием АТФ из АДФ и пи-рофосфата (Рi), происходит на митохондриальных мембранах и носит название окислительного фосфорилирования. Оно было открыто в 1931 г. В. А. Энгельгардтом (1894-1984). Следовательно, окислительное фосфорилирование — это процесс образования АТФ, сопряженного с переносом электронов по цепи транспорта (переносчиков) от НАД×Н или ФАД×H2 к O2 через многие другие переносчики, в частности питохромы. В процессе окислительного фосфорилирования генерируется 32 молекулы АТФ из всех 36 молекул АТФ, генерируемых в процессе окисления глюкозы до СО2 и Н2О.
Многоступенчатость транспорта электронов от НАД×Н или ФАД×Н2 к О2 по цепи многочисленных переносчиков сопровождается выбросом протонов из митохондриального матрикса и генерированием на внутренней митохондриальной мембране протон-движущей силы (мембранного потенциала), измеряемой в милливольтах. На внутренней поверхности митохондриальной мембраны протондвижущая сила равна 220 микровольтам.
В процессе обратного перехода протонов в митохондриальный матрикс происходит синтез АТФ.
Следовательно, окисление НАД×Н и ФАД×H2 и фосфорилирование АДФ в АТФ сопряжены по той причине, что они обеспечиваются протонным градиентом через внутреннюю мембрану митохондрий. Это сопряжение называют дыхательным контролем.
Потенциальные возможности окисления в митохондриях очень большие, т. к. последние обеспечивают производство почти всего АТФ в клетках млекопитающих.
|
|
|


