 |
Условия хранения препарата 5-Фторурацил-Эбеве
|
|
|
|
В защищенном от света месте, при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Азидотимидин
Показания
ВИЧ-инфекция у взрослых и детей (в комбинации с другими антиретровирусными препаратами).
Противопоказания
Гиперчувствительность, лейкопения (нейтрофилы < 750/мм3), анемия (гемоглобин < 7,5 г/дл), тромбоцитопения (уменьшение количества тромбоцитов до 25000/мкл), почечная и/или печеночная недостаточность.
Фармакологическое действие
Фармакологическое действие - противовирусное. Обладает высокой активностью в отношении ретровирусов (в т.ч. ВИЧ).
Действующее вещество
›› Зидовудин* (Zidovudine*)
Латинское название
Azidothymidin
АТХ:
›› J05AF01 Зидовудин
Фармакологическая группа
›› Средства для лечения ВИЧ-инфекции
Нозологическая классификация (МКБ-10)
›› B20-B24 Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ]
Состав и форма выпуска
1 капсула содержит зидовудина 0,1 г, а также сахар молочный, крахмал картофельный, МКЦ, магния стеарат или кальция стеарат; в пластиковых банках по 100 или 200 шт.
Характеристика
Твердые желатиновые капсулы, разъемные, с донышком белого цвета и желтой крышечкой, заполненные порошком белого или белого с желтоватым оттенком цвета, без запаха.
Фармакокинетика
Биодоступность — 60–70%. Проходит через ГЭБ, концентрация в спинно-мозговой жидкости составляет 50% от уровня в плазме. Метаболизируется в печени. Выводится почками около 30% в неизмененном виде, 50% и более — в виде глюкуронидов.
Фармакодинамика
В клетке при участии клеточных тимидинкиназы, тимидилаткиназы и неспецифической киназы фосфорилируется с образованием моно-, ди- и трифосфатного соединения. Зидовудин-трифосфат встраивается в провирус и блокирует дальнейшее наращивание цепи вирусной ДНК и делает невозможным синтез вирусной ДНК. Способствует увеличению количества T4 клеток.
|
|
|
Применение при беременности и кормлении грудью
Применение при беременности возможно, если ожидаемый эффект терапии превышает потенциальный риск для плода. На время лечения следует прекратить грудное вскармливание.
Побочные действия
Со стороны сердечно-сосудистой системы и крови (кроветворение, гемостаз): анемия, лейкопения, нейтропения.
Прочие: диспептические явления, повышение активности печеночных трансаминаз, сывороточной амилазы, гиперкреатининемия.
Способ применения и дозы
Внутрь, взрослым: начальная доза — по 200 мг 6 раз в сутки. Оптимальная доза подбирается индивидуально и может варьировать от 500 до 1500 мг/сут. Детям: средняя доза — из расчета 150–180 мг/м2 каждые 6 ч (4 раза в сутки). Пересчет дозы проводят по специальным таблицам с учетом роста и массы тела не реже 1 раза в 2 мес.
Особые указания
Необходимо прекратить лечение у взрослых при уровне гемоглобина < 7,5 г/дл или числе нейтрофилов < 750/мкл; у детей — при снижении уровня гемоглобина < 8 г/дл, количества нейтрофилов до 500 в мм3 в 2 анализах с интервалом в 24 ч, количества тромбоцитов до 25000 в мм3 или при прогрессирующей почечной недостаточности. Необходимо систематически проводить исследования периферической крови (в первые 3 мес лечения — каждые 2 нед, затем не реже 1 раза в месяц).
Срок годности
2 года
Условия хранения
Список Б.: В сухом, защищенном от света месте, при температуре не выше 25 °C.
Нуклеотиды. Отношение к гидролизу
Нуклеотиды гидролизуются нуклеотидазами, с образованием нуклеозидов и Фн.
Нуклеозиды, которые обычно рассматриваются как конечный продукт переваривания
нуклеиновых кислот в кишечнике, всасываются. В клетках некоторых тканей, в том числе
Рис 8.8. Схема катаболизма нуклеиновых кислот и нуклеотидов.и клетках кишечника, нуклеозиды подвергаются фосфоролизу нуклеозид фосфорилаза-
|
|
|
ми, с образованием оснований и рибозы 1-Ф (или дезоксирибозы 1-P). Рибоза 1-Ф и ри-
боза 5-Ф в цитозоле находятся в равновесии и могут быть вновь использованы для синте-
за нуклеотидов или вступают в неокислительную часть пенозофосфатного пути.
Пуриновые и пиримидиновые основания также или распадаются далее до конеч-
ных продуктов или используются повторно для синтеза нуклеотидов. В клетке существует
интенсивно обмениваемый пул рибонуклеотидов и РНК. Молекулы ДНК и пул дезокси-
рибонуклеотидов обменивается значительно медленнее.
Тканевые пурины и пиримидины, которые не попадают в пути повторного исполь-
зования, обычно распадаются и продукты их распада выделяются. Используется лишь
очень небольшое количество пищевых пуринов, а основная масса поступивших с пищей
пуринов распадается. Катаболизм пуринов и пиримидинов не сопровождается значитель-
ным высвобождением энергии в сравнении с обменом аминокислот, однако некоторые
продукты распада выполняют определенные физиологические функции, например, конеч-
ный продукт катаболизма пуринов у человека мочевая кислота, может служить антиок-
сидантом, продукт катаболизма пиримидина, β– аланин используется в синтезе активных
пептидов мозга и мышц. Парэнтеральное введение нуклеотидов и нуклеозидов нашло
применение в исследовательской практике. Меченый 3Н –тимидин включается в синтези-
руемую ДНК без изменений и используется для введения метки в ДНК различных биоло-
гических оъектов.
Конферменты АТФ, НАД+, НАДФ+.
Аденозинтрифосфорная кислота (АТФ) — универсальный источник и основной аккумулятор энергии в живых клетках. АТФ содержится во всех клетках растений и животных. Количество АТФ в среднем составляет 0,04% (от сырой массы клетки), наибольшее количество АТФ (0,2-0,5%) содержится в скелетных мышцах. В клетке молекула АТФ расходуется в течение одной минуты после ее образования. У человека количество АТФ, равное массе тела, образуется и разрушается каждые 24 часа.
АТФ – мононуклеотид, состоящий из остатков азотистого основания (аденина), рибозы и трех остатков фосфорной кислоты. Поскольку АТФ содержит не один, а три остатка фосфорной кислоты, она относится к рибонуклеозидтрифосфатам.
|
|
|
Для большинства видов работ, происходящих в клетках, используется энергия гидролиза АТФ. При этом при отщеплении концевого остатка фосфорной кислоты АТФ переходит в АДФ (аденозиндифосфорную кислоту), при отщеплении второго остатка фосфорной кислоты – в АМФ (аденозинмонофосфорную кислоту). Выход свободной энергии при отщеплении как концевого, так и второго остатков фосфорной кислоты составляет около 30,6 кДж/моль. Отщепление третьей фосфатной группы сопровождается выделением только 13,8 кДж/моль. Связи между концевым и вторым, вторым и первым остатками фосфорной кислоты называются макроэргическими (высокоэнергетическими).
Запасы АТФ постоянно пополняются. В клетках всех организмов синтез АТФ происходит в процессе фосфорилирования, т.е. присоединения фосфорной кислоты к АДФ. Фосфорилирование происходит с разной интенсивностью при дыхании (митохондрии), гликолизе (цитоплазма), фотосинтезе (хлоропласты).
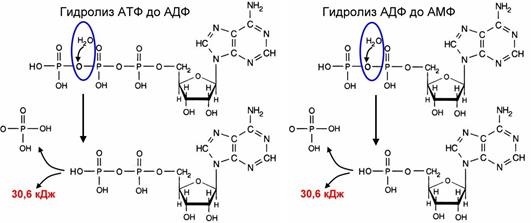
Рис. Гидролиз АТФ
АТФ является основным связующим звеном между процессами, сопровождающимися выделением и накоплением энергии, и процессами, протекающими с затратами энергии. Кроме этого, АТФ наряду с другими рибонуклеозидтрифосфатами (ГТФ, ЦТФ, УТФ) является субстратом для синтеза РНК.
Кроме АТФ есть и другие молекулы с макроэргическими связями – УТФ (уридинтрифосфорная кислота), ГТФ (гуанозинтрифосфорная кислота), ЦТФ (цитидинтрифосфорная кислота), энергия которых используются для биосинтеза белка (ГТФ), полисахаридов (УТФ), фосфолипидов (ЦТФ). Но все они образуются за счет энергии АТФ.
Помимо мононуклеотидов, важную роль в реакциях обмена веществ играют динуклеотиды (НАД+, НАДФ+, ФАД), относящиеся к группе коферментов (органические молекулы, сохраняющие связь с ферментом только в ходе реакции). НАД+ (никотинамидадениндинуклеотид), НАДФ+(никотинамидадениндинуклеотидфосфат) – динуклеотиды, имеющие в своем составе два азотистых основания – аденин и амид никотиновой кислоты – производное витамина РР), два остатка рибозы и два остатка фосфорной кислоты (рис..). Если АТФ – универсальный источник энергии, то НАД+ и НАДФ+– универсальные акцепторы, а их восстановленные формы – НАДН и НАДФН – универсальные доноры восстановительных эквивалентов (двух электронов и одного протона). Входящий в состав остатка амида никотиновой кислоты атом азота четырехвалентен и несет положительный заряд (НАД+). Это азотистое основание легко присоединяет два электрона и один протон (т.е. восстанавливается) в тех реакциях, в которых при участии ферментов дегидрогеназ от субстрата отрываются два атома водорода (второй протон уходит в раствор):
|
|
|
С  убстрат-Н2 + НАД+ субстрат + НАДН + Н+
убстрат-Н2 + НАД+ субстрат + НАДН + Н+
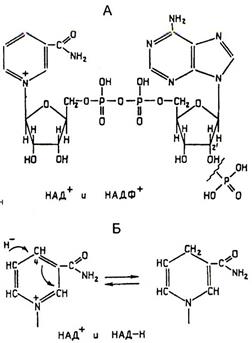
Рис.. Структура молекулы динуклеотидов НАД+ и НАДФ+.
А – присоединение фосфатной группы к остатку рибозы в молекуле НАД. Б – присоединение двух электронов и одного протона (аниона Н-) к НАД+.
В обратных реакциях ферменты, окисляя ^ НАДН или НАДФН, восстанавливают субстраты, присоединяя к ним атомы водорода (второй протон приходит из раствора).
ФАД – флавинадениндинуклеотид – производное витамина В2 (рибофлавина) также является кофактором дегидрогеназ, но ФАД присоединяет два протона и два электрона, восстанавливаясь до ФАДН2.
|
|
|


