 |
Вапиров В.В., Ханина Е.Я., Волкова Т.Я.
|
|
|
|
Вапиров В. В., Ханина Е. Я., Волкова Т. Я.
Основы электрохимии
Учебное пособие для студентов инженерно-технических специальностей университетов
1. Окислительно-восстановительные реакции
1. 1. Степень окисления
Каждый элемент в химическом соединении характеризуется определенной степенью окисления. Это связано с тем, что электроны, образующие химическую связь, могут быть по-разному распределены между элементами. Если химическая связь образована одинаковыми атомами, валентные электроны являются в равной степени общими и ни один из элементов не обладает эффективным электрическим зарядом. В ковалентной связи между различными атомами электроны смещены к более электроотрицательному элементу, в результате чего последний приобретает некоторую долю отрицательного заряда, а элемент, от которого смещены электроны – такую же долю положительного. В соединениях с ионной связью происходит почти полная передача электронов с образованием ионов. Для характеристики состояния элемента в молекуле и введено понятие степени окисления.
Степень окисления – условный электрический заряд, который может получить атом, если бы все электроны, образующие с ним химическую связь, были бы полностью смещены к более электроотрицательному элементу.
Обращает на себя внимание то, что степень окисления – величина формальная. Так, например, в молекуле HI ни атом водорода, ни атом йода не обладают целочисленными положительными или отрицательными зарядами, однако степень окисления водорода и йода в HI равны соответственно +1 и –1. Иными словами, степень окисления определяют исходя из предположения, что все связи в молекуле ионные и молекула состоит из ионов.
|
|
|
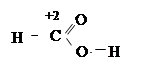
Не отражая истинного эффективного заряда атома в молекуле, степень окисления не всегда совпадает и с валентностью элемента. В молекуле муравьиной кислоты углерод является четырехвалентным, однако проявляет степень окисления +2.
 |
В результате многих химических реакций распределение электронов у одного и того же элемента, входящего в состав исходных веществ и продуктов реакции, может принципиально отличаться. При этом, несмотря на формальность, степень окисления отражает изменение электронного окружения элемента.
Химические реакции, в результате которых изменяется степень окисления элементов, называются окислительно-восстановительными.
В окислительно-восстановительной реакции один из элементов теряет электроны (окисляется), а другой их приобретает (восстанавливается). Однако не следует понимать, что при этом всегда происходит полная передача электронов от одного атома к другому. При окислении цинка кислородом
2Zn + O2 = 2ZnO
цинк только частично передает валентные электроны атому кислорода, но при этом меняет степень окисления от 0 до +2. При химическом взаимодействии натрия с хлором
2Na + Cl2 = 2NaCl
происходит почти полный перенос электрона от натрия к хлору и степени окисления элементов в молекуле NaCl совпадают с зарядами ионов.
При окислении элемента его степень окисления всегда увеличивается, а при восстановлении – уменьшается.
Элемент, восстанавливающийся в результате реакции, выступает в роли окислителя, а окисляющийся – в роли восстановителя. Процессы окисления и восстановления между собой тесно взаимосвязаны и один не возможен без другого.
В роли восстановителей в химической реакции могут выступать вещества, которые содержат элементы, способные отдавать электроны (окисляться), повышая при этом свою степень окисления. К типичным восстановителям относятся элементы главных подгрупп I и II группы периодической системы Д. И. Менделеева, водород и вещества, содержащие в своем составе атомы в состоянии низшей степени окисления – сероводород, аммиак, а также ионы, хлорид-анион, иодид-анион и т. д.
|
|
|
Роль окислителя могут выполнять вещества, содержащие элементы в высшей степени окисления, так как они способны только к восстановлению. К ним относятся азотная кислота, селеновая кислота, концентрированная серная кислота, бихромат калия и т. д. В роли окислителя могут выступать и элементы, способные к расширению своего электронного окружения (галогены, кислород, азот).
Вещества, образованные элементами в промежуточных степенях окисления, в зависимости от условий, могут выполнять функцию, как окислителя, так и восстановителя.
|
|
|


