 |
Назначение термостатирующего цилиндра? Какую функцию он выполняет при сжатии и расширении воздуха в бюретке?
|
|
|
|
Для исследования какого термодинамического процесса станет пригодной используемая установка, если выпустить воду из термостатирующего цилиндра и поддерживать в нем вакуум? Какой измерительный прибор при этом необходимо дополнительно установить на установке для исследования этого процесса?
4. Назначение измерительных приборов: барометра, вакуумметра, манометра и мановакуумметра?
5. Какое из ниже перечисленных давлений подставляется во все термодинамические соотношения? (избыточное, барометрическое, абсолютное или давление разрежения).
Какие элементы установки образуют дополнительный объём? Является ли он постоянным в опытах? Как он определяется, от чего он зависит?
Перечислите основные единицы измерения давления и запишите соотношения между ними. Единицы измерения давления в СИ.
8. Дайте определения понятиям вакуум, разрежение, избыточное, манометрическое, барометрическое и абсолютное давление. Запишите соотношения связывающие эти давления. Какое давление подставляется во все термодинамические соотношения?
9. Запишите уравнение состояния для 1 кг идеального газа. Объясните физический смысл и размерности входящих в него параметров.
10. Запишите уравнение состояния для 1 кмоля идеального газа. Объясните физический смысл и размерности входящих в него параметров.
11. Какими параметрами характеризуют (задают) состояние рабочего тела? Какие параметры входят в обобщающие понятия «термические и калорические параметры состояния рабочего тела»?
12. Изобразите на p-u и Т-s диаграммах изотермический и адиабатный процессы сжатия идеального газа, исходящие из общей точки. В каком из этих процессов затрачивается больше работы (какой?) при сжатии до одного и того же давления?
|
|
|
13. Изобразите на p-u и Т-s диаграммах изотермический и адиабатный процессы расширения идеального газа, исходящие из общей точки. В каком из этих процессов получается больше работы (какой?) при расширении до одного и того же объёма?
14. Какими единицами измерения может быть задано количество вещества, участвующего в процессе? Каковы соотношения между величинами, заданными этими единицами измерения?
Как соотносятся между собой теплота и работа в изотермическом процессе? Как на практике можно организовать изотермическое сжатие воздуха в судовом компрессоре? Что при этом мы выиграем и что потеряем? Ответ обосновать.
Какая разница между параметрами состояния и функциями процесса? Какими из этих величин может быть задано термодинамическое состояние рабочего тела?
Лабораторная работа №2 посвящена экспериментальному определению средней изобарной теплоемкости воздуха. Как известно, теплоемкость — это количество теплоты, необходимое для нагрева единицы количества вещества на один градус в данном термодинамическом процессе. В зависимости от метода определения различают истинную и среднюю теплоемкости.
Истинная теплоемкость вещества — это производная от количества теплоты δ q по температуре dT (dt) в данном термодинамическом процессе
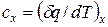
| (6.5) |
Истинная теплоемкость изображается на диаграмме T,s подкасательной (с) к кривой процесса в данной точке А (рис. 6.2).
Средняя теплоемкость – это количество теплоты q, которое необходимо подвести к единице количества вещества в данном термодинамическом процессе (либо отвести от вешщества), чтобы повысить (понизить) его температуру от t 1 до t 2. Этой формулировке соответствует математическая запись

| (6.6) |
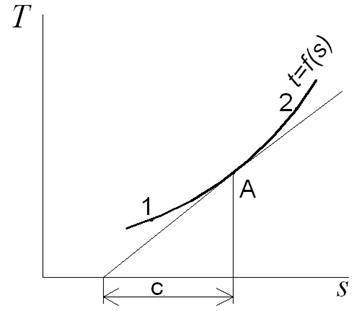
Рис 6.2. Определение истинной теплоемкости на диаграмме T,s
Как истинная, так и средняя теплоемкость в общем случае есть функция процесса. Однако они становятся функциями состояния, когда задан термодинамический процесс. Средняя теплоемкость в данном процессе может быть определена экспериментально, а истинная — рассчитана по (6.5).
|
|
|
Как известно, количество вещества, участвующего в процессе, может быть задано в килограммах, киломолях и нормальных кубических метрах. Поэтому различают массовую, мольную и объемную теплоемкости, имеющие соответственно размерности Дж/(кг·К), Дж/(кмоль·К) и Дж/(нм3·К).
Теплоемкость реального газа в заданном термодинамическом процессе зависти от двух параметров состояния. Чаще всего её представляют в табличном виде в зависимости от температуры и давления либо от температуры и удельного объема (реже). Теплоемкость идеального газа зависит только от температуры c = ƒ(T).
В рамках упрощенной молекулярно-кинетической теории (МКТ) зависимость теплоемкости от температуры не учитывают, а учитывают только её зависимость от строения молекулы вещества, а именно, от количества атомов в молекуле рассматриваемого газа. По этой концепции изохорная и изобарная теплоемкости вещества рассчитываются из соотношений
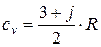 ,
, 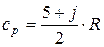
где j — количество вращательных внутримолекулярных степеней свободы,
R — удельная газовая постоянная рассматриваемого газа, Дж/(кг·К).
Для одноатомных молекул j = 0, двухатомных 2, трех- и многоатомных 3.
Количество теплоты, подводимое к рабочему телу массой М в заданном термодинамическом процессе (х = const) при изменении температуры от t 1 до t 2, может быть рассчитано из соотношения
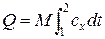
|
|
|


