 |
Химическое равновесие. Принцип Ле – Шателье
|
|
|
|
Химическое равновесие. Принцип Ле – Шателье
Реакции, которые протекают в одном направлении и идут до конца, называются необратимыми. Их не так много. Большинство реакций являются обратимыми, т. е. они протекают в противоположных направлениях и не идут до конца. Например, реакция J2 + H2 D 2HJ при 350°С является типичной обратимой реакцией. В этом случае устанавливается подвижное химическое равновесие и скорости прямого процесса и обратного делаются равными.
Химическое равновесие – такое состояние системы реагирующих веществ, при котором скорости прямой и обратной реакций равны между собой.
Химическое равновесие называют динамическим равновесием. При равновесии протекают и прямая, и обратная реакции, их скорости одинаковы, вследствие чего изменений в системе не заметно.
Концентрации реагирующих веществ, которые устанавливаются при химическом равновесии, называются равновесными концентрациями. Обычно их обозначают при помощи квадратных скобок, например, [J2], [H2], [HJ].
Количественной характеристикой химического равновесия служит величина, называемая константной химического равновесия. Для реакции в общем виде: mA + nB = pC + qD
Константа химического равновесия имеет вид:
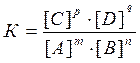
Она зависит от температуры и природы реагирующих веществ, но не зависит от их концентрации. Константа равновесия показывает, во сколько раз скорость прямой реакции больше скорости обратной реакции, если концентрации каждого из реагирующих веществ равна 1 моль/л. В этом физический смысл К.
Направление смещения химического равновесия при изменениях концентрации реагирующих веществ, температуры и давления (в случае газовых реакций) определяется общим положением, известным под названием принципа подвижного равновесия или принципа Ле Шателье: если на систему, находящуюся в равновесии, производится какое-либо внешнее воздействие (изменяется концентрация, температура, давление), то оно благоприятствует протеканию одной из двух противоположных реакций, которая ослабляет воздействие.
|
|
|
Следует отметить, что все катализаторы одинаково ускоряют как прямую, так и обратную реакции и поэтому на смещение равновесия влияние не оказывают, а только способствуют более быстрому его достижению.
Примеры решения задач
Пример 1.
Рассчитайте температурный коэффициент скорости реакции, зная, что с повышением температуры на 70 °С скорость возрастает в 128 раз.
Решение:
Для расчета используем правило Вант-Гоффа:
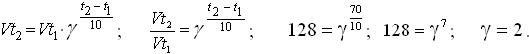
Ответ: 2
Пример 2.
При какой температуре закончится некоторая реакция за 0, 5 мин, если при 70°С она заканчивается за 40 мин? Температурный коэффициент реакции равен 2, 3.
Решение:
Для расчета используем правило Вант-Гоффа. Находим t2:
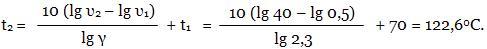
Ответ: 122, 6 0С
Пример 3.
Во сколько раз изменится скорость прямой реакции N2(г)+3Н2(г)=NH3(г), если давление в системе увеличить в 2 раза?
Решение:
Увеличение давления в системе в 2 раза равносильно уменьшению объема системы в 2 раза. При этом концентрации реагирующих веществ возрастут в 2 раза. Согласно закону действия масс, начальная скорость реакции равна Vн = k·[N2]·[H2]3.
После увеличения давления в 2 раза концентрации азота и водорода увеличатся в 2 раза, и скорость реакции станет равна Vк = k·2[N2]·23[H2]3 = k·32[N2]·[H2]3. Отношение Vк/Vн показывает, как изменится скорость реакции после изменения давления. Следовательно, Vк/Vн = k·32[N2]·[H2]3/(k·[N2]·[H2]3) = 32.
Ответ: скорость реакции увеличится в 32 раза.
|
|
|


