 |
2.3. ВОЛЬТАМПЕРОМЕТРІЯ. Теоретичні основи методу. І. Визначення концентрації іонів металів за рівнянням Ільковича
|
|
|
|
2. 3. ВОЛЬТАМПЕРОМЕТРІЯ
Теоретичні основи методу
Вольтамперометрія об'єднує групу електрохімічних методів аналізу, які базуються на вивченні поляризаційних кривих.
У вольтамперометрії застосовують електролітичні комірки, які містять електрод малої площі, що легко поляризуються, та електрод порівняння. У випадку, коли використовують ртутний краплинний електрод, метод називають полярографією. Вольтамперометричні данні одержують шляхом вимірювання сили струму, який тече через електролітичну комірку і є функцією потенціалу, поданого на індикаторний електрод. Графічну залежність сили струму від потенціалу називають вольтамперною кривою або полярограмою.
На початку електролізу, коли значення поданого потенціалу є незначним, сила струму збільшується дуже повільно. Такий струм називають залишковим. Як тільки потенціал катода досягає значення, необхідного для відновлення іонів, починається їх розрядження на краплині ртуті:

На катоді утворюється розбавлена амальгама металу Me(Hg), яка розкладається на складові, як тільки краплина попадає на анод:
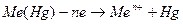
Після досягнення значення потенціалу, при якому відбувається відновлення іону металу, сила струму стрімко зростає, але після досягнення певного значення вона залишається постійною, незважаючи на збільшення потенціалу, що подається. Цей струм має назву граничного, зазвичай його величина пропорційна концентрації визначуваної речовини.
Під час одержання вольтамперної кривої до досліджуваного розчину додають певний індиферентний електроліт з катіонами, які відновлюються значно важче за визначуваний катіон, наприклад KCl, KNO3, NH4Cl, з концентрацією в 100 – 1000 разів вищою від концентрації визначуваної речовини. Такий електроліт називають фоном. Його додають до досліджуваного розчину для збільшення електропровідності та для екранування електричного поля індикаторного електрода (катода). Тому катіони визначуваної речовини не притягаються електричним полем катода, а рухаються до нього за рахунок дифузії.
|
|
|
Найважливішими характеристиками полярограми є потенціал на півхвилі  та висота полярографічної хвилі
та висота полярографічної хвилі 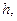 яка відповідає дифузійному струму.
яка відповідає дифузійному струму.
Величину „потенціалу напівхвилі” використовують в якісному полярографічному аналізі. Потенціали напівхвиль різних речовин, розташовані в порядку збільшення їх негативних значень, утворюють так званий полярографічний спектр (таблиці значень  ). Оскільки потенціал на півхвилі суттєво залежить від складу розчину (середовища), у полярографічних таблицях вказують фон. У кількісному полярографічному аналізі використовують наступні методи:
). Оскільки потенціал на півхвилі суттєво залежить від складу розчину (середовища), у полярографічних таблицях вказують фон. У кількісному полярографічному аналізі використовують наступні методи:
І. Визначення концентрації іонів металів за рівнянням Ільковича
Класичним методом визначення концентрації електровідновної речовини є розрахунок її з дослідних даних за рівнянням Ільковича. Рівняння Ільковича дає залежність між величинами граничного дифузійного струму i концентрацією:
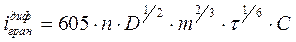
де  - кількість електронів, які беруть участь в електрохімічній реакції;
- кількість електронів, які беруть участь в електрохімічній реакції;  коефіцієнт дифузії іона
коефіцієнт дифузії іона 
 швидкість витікання ртуті з капіляра, мг/с;
швидкість витікання ртуті з капіляра, мг/с; 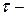 час утворення краплини, с;
час утворення краплини, с;  концентрація визначуваної речовини, ммоль/л.
концентрація визначуваної речовини, ммоль/л.
Для того, щоб розрахувати концентрацію (С), попередньо потрібно визначити три експериментальні величини  ., m2/3 i
., m2/3 i  . Визначення
. Визначення  здійснюють при потенціалі початку граничного струму. Значення коефіцієнта дифузії знаходять з таблиць. Після чого розраховують концентрацію. Тривалість визначення m, необхідно вести виміри при постійній температурі, а головне – неточне значення величини D робить цей метод цікавим тільки з теоретичної точки зору.
здійснюють при потенціалі початку граничного струму. Значення коефіцієнта дифузії знаходять з таблиць. Після чого розраховують концентрацію. Тривалість визначення m, необхідно вести виміри при постійній температурі, а головне – неточне значення величини D робить цей метод цікавим тільки з теоретичної точки зору.
|
|
|
|
|
|


