 |
ЗАДАЧА 2. (Автор - доцент А.И. Курамшин)
|
|
|
|
Можно записать следующие уравнения реакций:
1. KOH + HI à KI + H2O
2. 6КОН + ЗВг2 à 5КВг + КВЮз + ЗН2О
3. 2HI + Вг2 à НВг + 2I2
4. Н2О2 + Вг2 à О2 + 2НВг
5. Н2О2 + 2HI à I2 + 2Н2О
Также можно записать по 2 реакции аминокислот соответственно с щелочью и иодоводородной кислотой, реакцию образования дипептида между двумя аминокислотами. Возможный вариант реакции - З-тиол-2-аминопропановая кислота реагирует с перекисью водорода, образуя мостик -S-S- (этот принцип сшивки серных мостиков используется при химической завивке пергидролем).
ЗАДАЧА 3. (Автор - доцент А.И. Курамшин)
В соответствии с содержанием водорода в С найдем, что С - хлороводород, в соответствии с содержанием олова в "оловянном масле", его фическими и рядом химических свойств определяем, что "оловянное масло" - хлорид олова(1V) SnСl4 Уравнения реакций:
• SnCl4+ С12О à 2С12 + SnOCl2
• SnCl4 + 2H2O à SnO2 + 4HC1
• SnCL» +'4HF à SnF4 + 4HC1
• SnCl4 + 2НС1(конц.) à H2[SnCl6]
Другое вещество с тем же качественным составом, что и хлорид олова(1V) - хлорид олова(II) SnCl2. Более высокие температуры кипения и плавления этого соединения обусловлены тем, что хлорид олова(II) в отличие от тетрахлорида олова имеет ионную кристаллическую решетку. Уравнения реакций, которые можно предложить:
SnCl2 + 2AgNO3 à Sn(NO3)2 + 2AgCl
SnCl2 + 2KOH à Sn(OH)2 + 2KC1
SnCl2 + C12 à SnCl4,
SnCl2 + Zn à ZnCl2 + Sn
ЗАДАЧА 4. (Автор - старший преподаватель М.А. Зиганшин)
Чилийская селитра - это одно из названий нитрата натрия (NaNO3).
При нагревании селитры происходит образование нитрита натрия:
В соответсвии с логикой первой реакции одно из веществ А или В должно содержать
в своем составе элемент Na. Тогда можно предположить, что В - это нитрит натрия, а
|
|
|
вещество А - ароматический углеводород.
Получим цепочку:
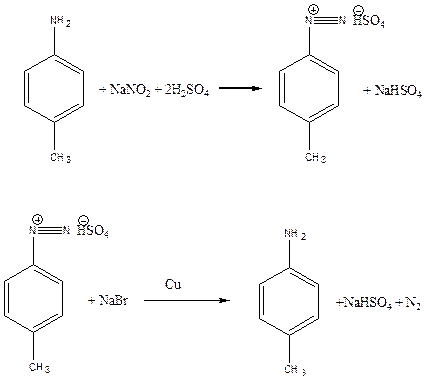
А - п-метиланилин, С - сульфат п-диазотолила, D - азот. Реакция образования диазосоединений протекает при 0°С
Альтернативной одностадийной реакцией может быть бромирование толуола в присутствии солей трехвалентного железа:
Вг2 + С6Н5-СН3 à р-Вr-С6Н5-СН3 + НВr Норвежская селитра - это нитрат кальция Ca(NO3)2
ЗАДАЧА 5. (Автор - старший преподаватель М.А. Зиганшин)
1. Определим состав веществ А, В, С
Вещество А:
C:Н:О= 6.43:11.43:0.714 = 9:16:1
Получаем формулу С9Н16О
Вещество В:
С:Н:О=6,38:6,38:1,064=6:6:1
Получаем формулу С6Н6О
Вещество С:
С:Н:О= 6,77:8,39:0,645=10,5:13:1
Получаем формулу С2|Н26О2
Вещество В – фенол (циклическое соединение с выраженными кислотными свойствами с общей формулой С6Н5ЩР)
Вещество А - 3,3,5-триметилциклогексанон-1
2. Запишем уравнение реакции (возможно присоединение в орто положение, однако, в основном замещение пройдет по пара-положению). Видно, что состав С соответствует А + 2В – Н2О. Так как С обладает кислотными свойствами, значит фенольные ОН-группы сохранились.
3. HCI является в данной реакции катализатором.
ЗАДАНИЯ РАЙОННЫХ ОЛИМПИАД ПО ХИМИИ
Республика Татарстан, 2005-2006 учебный год
Задачи для 11 класса
ЗАДАЧА 1.
Расшифруйте цепочку превращений:
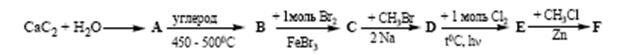
?1. Напишите уравнения всех реакций. Расставьте коэффициенты.
?2. Назовите соединения A, B, C, D, E, F.
ЗАДАЧА 2.
d -Элемент периодической таблицы Менделеева (X), находящийся в 6 периоде, при
хранении окисляется кислородом воздуха до высшего оксида, обладающего резким
запахом. При взаимодействии оксида X с концентрированной соляной кислотой выделяется хлор и образуется хлорид X, в котором валентность X вдвое меньше, чем в высшем оксиде.
?1. Определите элемент X.
?2. Напишите уравнения всех реакций, упомянутых в задаче. Расставьте коэффициенты.
ЗАДАЧА 3.
Имеется раствор смеси муравьиной, уксусной и пропионовой кислот. При проведении реакции “серебряного зеркала” с 25 г. этого раствора выделилось 3.5208 г. металла. На нейтрализацию другой порции в 25 г. раствора смеси кислот израсходовано 12.556 г. 10 %-ного раствора гидроксида натрия.
|
|
|
?1. Напишите уравнения всех реакций.
?2. Определите весовое %-ное содержание каждой кислоты в исходном растворе, если
известно, что %-ные концентрации уксусной и пропионовой кислот равны.
?3. Определите объем газа, выделившегося в реакции “серебряного зеркала” при нор-
мальных условиях.
ЗАДАЧА 4.
Неизвестный углеводород не реагирует с бромной водой и перманганатом калия.
1.0000 г. этого углеводорода было сожжено, продукты сгорания были поглощены
концентрированным раствором щелочи. Масса раствора при этом возросла на 4.556 г.
Также этот углеводород был прохлорирован эквимолярным количеством хлора. Продукты хлорирования были обработаны спиртовым раствором щелочи, а далее подвергнуты озонолизу. В результате были получены три альдегида и два кетона.
?1. Определите структурную формулу неизвестного углеводорода.
?2. Изобразите структуры полученных кетонов и альдегидов.
ЗАДАЧА 5.
Когда во взаимодействие вступают органические вещества, то далеко не всегда
удается предсказать возможные направления процесса. Рассмотрим, например, такую
реакцию: окисление пропилена перманганатом калия в кислой среде. Анализ продуктов реакции показал, что процесс одновременно протекает по трем направлениям: в
среднем одна треть молекул пропилена окисляется до уксусной кислоты, одна шестая
часть — до щавелевой, а остальные молекулы полностью превращаются в углекислый газ. Но каков механизм окисления, какие именно связи в углеродной цепи пропилена разрываются в каждом из трех случаев? Чтобы узнать это, синтезировали пропилен, содержащий в метиленовой группе меченый атом углерода (это может быть либо стабильный изотоп 13С, либо радиоактивный изотоп 14С). Изучение изотопного состава продуктов реакции показало, что чуть более 40 % всего углекислого газа содержит изотопную метку.
Теперь вы получили достаточно полную информацию для того, чтобы ответить на
следующие вопросы.
1?. Была ли обнаружена изотопная метка в молекулах уксусной и щавелевой кислот?
|
|
|
2?. В каком месте разрывается углеродная цепь молекулы пропилена в каждом из
трех случаев?
3?. Напишите уравнения реакций окисления пропилена в каждом из трех случаев и суммарной уравнение процесса
4?. Как получить пропилен с нужной изотопной меткой? (Обычно для синтеза подобных препаратов используют карбонат бария, содержащий меченый углерод.)
|
|
|


