 |
Определение условной температуры замерзания раствора неизвестного вещества и расчет его молярной массы.
|
|
|
|
Цель работы: Научиться криометрически определять молярную массу вещества.
Задание: Определить молярную массу вещества, сравнить полученный результат с табличным.
Приборы, оборудование и реактивы: макет криометра, термометр Бекмана, термометр химический, лёд колотый, хлорид натрия, исследуемые растворы сахарозы, мочевины, 0,9% раствор хлорида натрия.
Сущность работы:
Молярная масса неэлектролита определяется по измеренному относительному понижению температуры замерзания раствора по сравнению с чистым растворителем.
Проводится охлаждение заданных растворов до начала образования кристаллов льда. Измерение проводится с помощью термометра Бекмана в условных единицах. По полученным данным вычисляется понижение температуры замерзания раствора:
DТз=Тз (Н2О) – Тз(р-р),
где Тз – точка замерзания при данной настройке термометра. Рассчитывают молярную массу неэлектролита по формуле:
Выполнение эксперимента:
1. Подготовка макета криометра к работе (рис.2.2)
2. Определение температуры замерзания растворителя.
3. Определение температуры замерзания раствора.
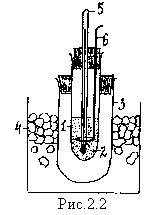
1 – внутренний сосуд;
2 - анализируемый раствор или дистиллированная вода;
4 – внешний сосуд;
5 - термометр Бекмана;
6 – мешалка
Экспериментальные данные
| Измерения | Температура замерзания (по шкале термометра Бекмана) | |
| Вода | Анализируемый раствор | |
| 1 | ||
| 2 | ||
| 3 | ||
| Среднее значение | ||
Справочные величины ___________________________________
Обработка результатов эксперимента
1. Вычисляют значение DТз. По полученным данным вычисляется понижение температуры замерзания раствора:
|
|
|
DТз=Тз (Н2О) – Тз(р-р),
где Тз – точка замерзания при данной настройке термометра.
2.Рассчитывают молярную массу неэлектролита по формуле:
1000 m(x) K(H2O)
М(Х) = --------------------------
m(S) DТз
m(x) – масса растворенного вещества;
K(H2O) – криометрическая постоянная (табулированная величина);
m(S) – масса растворителя;
DТз – разность температур замерзания воды и анализируемого раствора;
1000 – переводной коэффициент [ г/кг].
4. Вычисляют относительную ошибку опыта:
Расчеты:
* В выводах указывают вещество, содержащееся в исследуемом растворе, относительную ошибку эксперимента.
Выводы:
Если было проведено определение DТз раствора электролита (хлорида натрия) с известной массовой долей, то DТз = i сmКТ, где
i –изотонический коэффициент Вант-Гоффа,
сm – моляльная концентрация.
В результате эксперимента можно рассчитать значение изотонического коэффициента хлорида натрия и сравнить с теоретическим.
Дата _______
Лабораторная работа 5.2
Наблюдение явлений плазмолиза и гемолиза эритроцитов
Цель: Изучение влияние концентрации веществ в окружающем растворе на состояние эритроцитов и объяснить на основе осмотического давления.
Задание: Изучить состояние эритроцитов в разбавленном растворе (воде), изотоническом растворе и 10% растворе NaCl.
Оборудование и реактивы: Микроскоп с подсветкой, штатив с пробирками, пипетки, предметные и покровные стекла. Донорская кровь, водные растворы хлорида натрия с массовыми долями 0,9 и 10%, дистиллировнная вода.
Сущность работы:В солевых растворах мембрана эритроцита проницаема для молекул воды. При помещении эритроцита в р-р соли с меньшей концентрацией (по сравнению с содержимым эритроцита) наблюдается гемолиз(разорванные клетки, мутная кровь). В гипертоническом р-ре происходит обратный процесс – плазмолиз(сжатие эритроцитов за счет потери воды, прозрачная кровь). В изотоническом растворе эритроциты без изменений.
|
|
|
Выполнение эксперимента:
Росм(плазмы):
 |
Рис. 1 ______________________________________
 |
Рис.2 _______________________________________

Рис.3 _____________________________________
Обработка результатов эксперимента: Расчет осмотического давления примененных в работе растворов.
* В выводах указывают значение явления осмоса для состояния клеток.
Вывод: 
Дата _________ Занятие ________
|
|
|


