 |
15. Диаграмма состояния для двухкомпонентной системы, образующие неограниченные твердые растворы.
|
|
|
|
15. Диаграмма состояния для двухкомпонентной системы, образующие неограниченные твердые растворы.
Два компонента: компонент А и компонент В.
АаВ - линия ликвидус.
 АвВ – линия солидус.
АвВ – линия солидус.
 Выше линии ликвидус сплав находится в жидком состоянии, ниже линии солидус – в твердом. При кристаллизации сплавов по диаграмме этого типа из жидкости будут выделятся не жидкие компоненты, а твердые растворы. Это обусловлено тем, что при сплавлении компонентов А и В образуется непрерывный ряд твердых растворов, т. е. растворов неограниченной растворимости. Отсюда a- твердый раствор компонента В в компоненте А.
Выше линии ликвидус сплав находится в жидком состоянии, ниже линии солидус – в твердом. При кристаллизации сплавов по диаграмме этого типа из жидкости будут выделятся не жидкие компоненты, а твердые растворы. Это обусловлено тем, что при сплавлении компонентов А и В образуется непрерывный ряд твердых растворов, т. е. растворов неограниченной растворимости. Отсюда a- твердый раствор компонента В в компоненте А.
16. Диаграмма состояния для двухкомпонентной системы
Диаграмма состояния для двухкомпонентной системы, компоненты в которой образуют ограниченные твердые растворы, при этом в зависимости от типа диаграммы, диаграммы подразделяются на диаграммы с эвтептикой и диаграммы с перетептикой.
Диаграммы с эвтептикой: компоненты А и В. Фазы: жидкость a, b; a- твердый раствор компонента В в компоненте А; b - твердый раствор компонента А в компоненте В.
Линия АВС – ликвидус. ADCFB – солидус, т. к. компоненты вступают во взаимодействие в твердом состоянии с правой и с левой стороны диаграммы будут находиться так называемые области ограниченной растворимости.
Линия ДК- указывает на то, что растворимость компонента В в А увеличивается с повышением температуры. Растворимость В в А при комп. Температуре будет соответственна на диаграммы. При температуре плавления эвтевтики точка Д на диаграмме. Противоположность растворимость компонента А в В не изменяется (линия FL) при комнатной температуре растворимость компонента А в В соответственна точке L при температуре плавления эвтевтики в точке L. Горизонтальная линия DCF соответствует температуре, при которой происходит эвтевтическая реакция.
|
|
|
Эвтевтика – это механическая смесь двух или более фаз одновременно кристаллизующихся из жидкости. В точке С происходит чисто эвтевтическая реакция, которая записывается как жидкость точки С распадается на a - твердый раствор точки Д и b - в точке F.
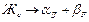
Кривые охлаждения.
С=К-Ф+1
С0-1=2-1+1=2 С1-2=2-2+1=1
Диаграмма с перлитом.
Компоненты А, В, жидкост, a, b.
В отличие от эвтевтической реакции при перетептичекой реакции жидкость взаимодействует с кристаллами выпавшей фазы с образованием кристаллов новой фазы.
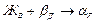
17. Диаграмма состояния с устойчивым химическим соединением
 Химическое соединение считается устойчивых, если оно плавится без разложения (предварительного).
Химическое соединение считается устойчивых, если оно плавится без разложения (предварительного).
18 Диаграмма состояния с неустойчивым химическим соединением

Характерным для неустойчивого химического соединения является то, что разлогается с повышением температуры.
19. Диаграмма состояния железо-цементит.
 Ж+F – ферритная область.
Ж+F – ферритная область.
F+A – ферритная + аустенитная.
Л – ледебурит
ЦI – цементит первичный.
Железо – металл, плавящийчя при температуре 1539оС и относящийся к полиморфным.
Полиморфизм – это возможность существования металлов в различных кристаллических модификациях.
В интервале 1539 оС – 1392 оС железо имеет ОЦК решетку.
В интервале 1392 оС – 911 оС железо имеет ГЦК решетку.
При температуре менее 911 оС железо имеет ОЦК решетку.
При температуре 768 оС железо из ферромагнитного переходит в паромагнитном состояние, т. е. становится немагнитным. Это т. н. точка Кюри.
Железо сравнительно мягкий металл: sв=250 МПа, НВ 80.
Цементит – химическое соединение, отвечающее формуле Fe3C. Образуется при строго определенном количестве атомов Fe и C, причем доля C составляет 6, 67%. Цементит является наиболее твердой фазой железоуглеродистых сплавов (НВ 800). При нагреве в определенных условиях цементит может распадаться с образованием железа и углерода в свободном состоянии в виде графита. Способность цементита к разложению положена в основу получения чугунов.
|
|
|
На диаграмме состояния железа-цементит линия ABCD – линия липидус, а AHIECF – солидус.
На диаграмме состояния есть две области, прилегающие к ординате, на которых откладывают температуру компонента железа, область феррита и область аустенита. Вообще на диаграмме можно выделить 4 фазы: жидкость, феррит, аустенит и цементит.
Ферит – твердый раствор углерода в a-железе. Феррит имеет ОКЦ решетку. Чисто ферритные области: AHN (1539 оС – 1392 оС) (высоко температурный феррит) и AGPQ (911 оС и до комнатной).
Аустенит – твердый раствор углерода в g-железе. Имеет ГЦК решетку. Область чистого аустенита MIESG.
На диаграмме видно три горизонтальных линии, при температуре которых протекают нонвариантные рекации (С=0).
По линии HIB при Т=1499 оС протекает перетектическая реакция, в результате которой жидкость состава точки B взаимодействует с кристаллами феррита в точке Н с образованием кристаллов аустенита в точке I.
По линии ECF при Т=1147 оС протекает эвтектическая реакция, в результате которой жидкость в точке C распадается на аустенит в точке E и цементит. Механическая смесь аустенита и цементита в интервале T=1147 оС – 727 оС получила название ледебурит.
По линии PSK при Т=727 оС протекает эвтектоидная реакция, в результате которой аустенит в точке S распадается на феррит в точке P и цементит. Механическая смесь феррита и цементита получила называние перлит.
Эвтектика отличается от эвтектоида тем, что первая протекает с участием жидкой фазы. Вторая является результатом распада твердого раствора. В связи с тем, что при температуре меньше 727 оС аустенита быть не может, ледебурит видоизменяется и в интервале T=727 оС – 20 оС ледебурит – механическая смесь из перлита и цементита.
На диаграмме видны линии ограниченной растворимости (PQ и SE).
При Т=20 оС количество углерода, способного раствориться в ОЦК решетке феррита составляет 0, 01% (в точке Q). При Т=727 оС количество углерода, способного раствориться в ОЦК решетке феррита составляет 0, 02% (в точке P). Следовательно, при охлаждении избыток атомов углерода должен выделиться из ОЦК решетки, но не в чистом виде, а в виде цементита третичного. Аналогичное наблюдается и при растворении углерода в ГЦК решетке, если при Т=727 оС (точка S) углерод составляет 0, 8%, то при Т=1147 оС (точка Е) – 2, 14%. При охлаждении избыток атомов углерода должен выделиться из ГЦК решетки, но не в чистом виде, а в виде цементита вторичного. По химическому составу цементит первичный, вторичный и третичный не отличаются. Это для того, чтобы отличить цементит, выделившийся из жидкости, из аустенита и из феррита.
|
|
|
Сплавы железа с углеродом с содержанием углерода до 2, 14% называют сталь. Стали подразделяются на доэвтектоидные, с содержанием углерода до 0, 8% (феррит + перлит), эвтектоидные – 0, 8% (перлит), заэвтектоидные –от 0, 8% до 2, 14% (перлит + цементит II). Сплавы железа с углеродом с содержанием углерода более 2, 14% называют чугунами: доэвтектоидные –от 2, 14% до 4, 3% (перлит + ледебурит + цементит), эвтектический –4, 3% (ледебурит), заэвтектический – от 4, 3% до 6, 67% (ледебурит + цементит I).
|
|
|


