 |
Методы проведения гравиметрического анализа.
|
|
|
|
Лапина С.Ф.
ГРАВИМЕТРИЧЕСКИЙ (ВЕСОВОЙ)
АНАЛИЗ
Методические указания для выполнения лабораторных работ
По дисциплине «Аналитическая химия».
Содержат теоретические основы гравиметрического (весового) анализа, технику выполнения основных операций гравиметрического анализа, примеры определений веществ гравиметрическим (весовым) методом, примеры расчета, вопросы для контроля знаний студентов.
Предназначены для выполнения лабораторных работ студентами специальности 013100 «Экология», по дисциплине «Аналитическая химия».
Рецензент: Заведующий кафедрой химии БрГТУ, к.х.н А.Д. Синегибская.
Содержание
1. Теоретические основы гравиметрического (весового) анализа.
1.1. Общая характеристика гравиметрического (весового) анализа.
1.2. Вычисления в гравиметрическом (весовом) анализе.
2. Методические указания к выполнению лабораторных работ.
2.1. Подготовка посуды для анализа.
2.2. Аналитические весы и правила взвешивания на них.
2.3. Техника общих операций в гравиметрическом (весовом) анализе.
2.4. Примеры количественного определения веществ гравиметрическим (весовым) методом.
2.4.1. Определение серы в растворимых сульфатах.
2.4.2. Определение кристаллизационной воды в хлориде бария.

Теоретические основы гравиметрического (весового) анализа.
Аналитическая химия – это экспериментальная наука. Однако для того, чтобы самостоятельно решать практические задачи, необходимо глубоко усвоить теоретические основы метода.
Общая характеристика гравиметрического (весового) анализа.
Количественное определение вещества, основанное на точном измерении массы определяемого компонента пробы, выделенного либо в виде соединения определенного состава, называется гравиметрическим (весовым) методом анализа. В основе метода лежат законы сохранения массы и постоянства состава вещества.
|
|
|
Неоспоримыми достоинствами гравиметрического анализа являются; высокая точность (десятые доли процента) и надежность, что позволяет использовать его в качестве арбитражного метода при получении сомнительных результатов другими методами анализа, особенно при определении состава вещества. Существенным недостаток является длительность анализа.
Методы проведения гравиметрического анализа.
Различают две группы методов проведения гравиметрического анализа - методы отгонки и методы осаждения.
Методы отгонки. Эти методы применяются в нескольких вариантах: а) определяемое вещество отгоняют из точной навески исследуемого образца и по уменьшению ее массы судят о содержании летучего компонента, например, таким способом определяют количество гигроскопической влаги в веществе и кристаллизационной воды в солях, высушивая навеску образца при определенной температуре до постоянной массы; б) определяемое вещество переводят химическим путем в летучее состояние и отгоняют, например, при анализе силикатов, содержащуюся в них двуокись кремния (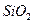 ) действием плавиковой кислоты переводят в летучий продукт - тетрафторид кремния(
) действием плавиковой кислоты переводят в летучий продукт - тетрафторид кремния( ), который отгоняют из образца и по убыли массы навески рассчитывают содержание кремния; в) определяемое вещество отгоняют и поглощают каким либо поглотителем, по увеличению массы которого рассчитывают содержание компонента, например, при определении двуокиси углерода в карбонатных породах выделяют углекислый газ (действием кислоты или прокаливанием), который поглощают известью или аскаритом.
), который отгоняют из образца и по убыли массы навески рассчитывают содержание кремния; в) определяемое вещество отгоняют и поглощают каким либо поглотителем, по увеличению массы которого рассчитывают содержание компонента, например, при определении двуокиси углерода в карбонатных породах выделяют углекислый газ (действием кислоты или прокаливанием), который поглощают известью или аскаритом.
Методы осаждения. Эти методы основываются на простой общей схеме определения. Навеску исследуемого образца, содержащего определяемое вещество, переводят в раствор и добавляют избыток реагента-осадителя. Образовавшийся осадок отфильтровывают, промывают, затем высушивают (прокаливают) и взвешивают. Зная массу и состав осадка можно вычислить количество определяемого компонента.
|
|
|
Форма осаждения.
Форма осаждения - соединение, в виде которого производят осаждение определяемого компонента. Форма осаждения должна удовлетворять ряду требований.
1. Анализируемое вещество должно осаждаться практически полностью - при этом потеря вещества за счет неполноты осаждения (растворимости) не должна превышать 10-4 г. т.е чувствительности аналитических весов. В гравиметрическом анализе в качестве осаждаемой формы используются соединения с малой величиной Ks0 (Ks0 - это величина произведения растворимости, например для хлорида серебра  . Чтобы вещество можно было использовать в качестве осаждаемой формы, Ks0, для бинарных соединений, должно быть не более 10-8, для соединений состава 2:1 не более 10-12). Одноименный ион, добавленный с избытком реагента-осадителя, понижает растворимость осадка (S). Например, используемый в качестве формы осаждения при определении хлоридов осадок
. Чтобы вещество можно было использовать в качестве осаждаемой формы, Ks0, для бинарных соединений, должно быть не более 10-8, для соединений состава 2:1 не более 10-12). Одноименный ион, добавленный с избытком реагента-осадителя, понижает растворимость осадка (S). Например, используемый в качестве формы осаждения при определении хлоридов осадок  в воде обладает некоторой растворимостью –
в воде обладает некоторой растворимостью –
 и
и 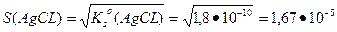 моль/л,
моль/л,
но при добавлении избытка нитрата серебра приводит к сдвигу гетерогенного равновесия в системе и уменьшает растворимость осадка:
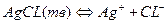
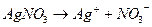
Если [Ag +]=0,1 моль/л, то
 моль/л,
моль/л,
т.е растворимость уменьшается на четыре порядка.
Однако к максимальной концентрации осадителя стремится не следует, т.е. более чем полуторный избыток может вызвать увеличение растворимости осадка вследствие «солевого эффекта», комплексообразования, амфотерности и т.д.
2. Осадок должен быть легко фильтрующимся (крупнокристаллическим) и химически чистым.
В процессе осаждения размер частиц осадка обратно пропорционален относительному пересыщению раствора (ОП), которое определяется по формуле:

где С – молярная концентрация смешиваемых реагентов до начала осаждения, моль/л;
S – молярная растворимость осадка после установления равновесия, моль/л.
Таким образом, для получения крупнокристаллического осадка следует подобрать такие условия, при которых С было бы наименьшим, а S относительно большим. Для этого обычно проводят осаждение из горячих (S велико) и разбавленных (С мало) растворов, медленно при перемешивании добавляя осадитель – во избежание местных пересыщений, а также выстаивают осадок в соприкосновении с маточным раствором в течение некоторого времени («старение осадка»), что приводит к росту относительно крупных кристаллов за счет растворения более мелких.
|
|
|
В тоже время растворимость (S) многих осадков столь незначительна, что не удается получить достаточно малую разность С- S, т.е. величина ОП велика, а в растворе появляется много центров кристаллизации, осадок образуется быстро и получается аморфным. В этом случае осаждение производят при энергичном перемешивании и нагревании, из концентрированных растворов, концентрированным раствором осадителя, с добавлением электролита (обычно соли аммония), что вызывает коагуляцию первоначально образующегося коллоидного раствора и, следовательно, уплотнение осадка. Аморфные осадки немедленно фильтруют.
Образование осадков сопровождается соосаждением, т.е. выпадением в осадок примесей растворимых в условиях осаждения.
Основными видами соосаждения являются:
1. Адсорбция ионов на поверхности осадка – особенно значительна для аморфных осадков, имеющих большую поверхность;
2. Окклюзия – захват примесей внутрь кристалла во время его роста и формирования за счет дефектов в кристаллической решетке;
3. Изоморфные включения (инклюзия) – совместная кристаллизация соединений, имеющих однотипные формулы и кристаллизующихся в одинаковых геометрических формах.
Чтобы свести к минимуму явления соосаждения, осаждение необходимо проводить в условиях получения крупных кристаллов, имеющих малую поверхность.
В случае очень загрязненных осадков их переосаждают, а затем тщательно промывают.
|
|
|


