 |
Главные основания нуклеиновых кислот
|
|
|
|
Главными пиримидиновыми основаниями и у прокариот, и у эукариот являются цитозин (Cyt), тимин (Thy) и урацил (Ura). Пуриновые основания представлены аденином (Ade) и гуанином (Gua). ДНК содержит два пиримидиновых основания (цитозин и тимин) и два пуриновых основания (аденин и гуанин). В состав РНК также входят два пиримидина – цитозин и урацил и два пурина – аденин и гуанин (рис. 12.2).
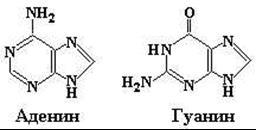
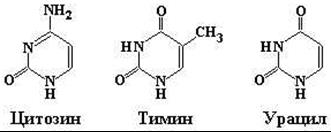
Пуриновые Пиримидиновые
Рис. 12.2. Структурные формулы главных пуриновых и пиримидиновых оснований нуклеиновых кислот
Кроме аденина и гуанина известны два других пуриновых основания – ксантин (Xan) и гипоксантин (Hyp), которые выступают в роли интермедиатов в процессах метаболизма пуринов, – в частности, ксантин и гипоксантин являются продуктами окислительного дезаминирования гуанина и аденина соответственно. Гипоксантин выполняет важную функцию в качестве одного из оснований, входящих в состав антикодона в транспортных РНК (рис. 12.3). У человека в роли конечного продукта катаболизма пуринов выступает окисленное пуриновое основание – мочевая кислота (UA).
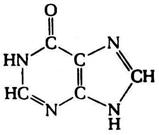
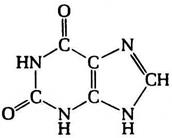
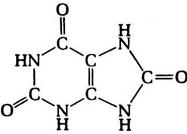
Гипоксантин Ксантин Мочевая кислота
Рис. 12.3. Структурные формулы минорных пуриновых оснований нуклеиновых кислот
Физико-химические свойства пуриновых
и пиримидиновых оснований
Явление таутомерии
Благодаря феномену кето-енольной таутомерии азотистые основания в нуклеотидах могут существовать либо в лактимной, либо в лактамной формах. В физиологических условиях преобладает лактамная форма гуанина тимина и урацила, но лактимные формы аденина и цитозина.
Для осуществления специфического спаривания основания должны находиться в соответствующей таутомерной форме. Миграция водородного атома позволяет каждому основанию существовать в различных таутомерных формах. Основания в составе двойной спирали ДНК, образующие канонические пары, должны иметь аминогруппы (-NH2) и кетогруппы (>С=О), в отличие от таутомеров, имеющих иминогруппы (=NH) и енольные группы (-ОН) и способных к неканоническому спариванию, как, например, пуриновое основание Ade, который может образовать пару с таутомерной формой Cyt (рис. 12.4).
|
|
|
А 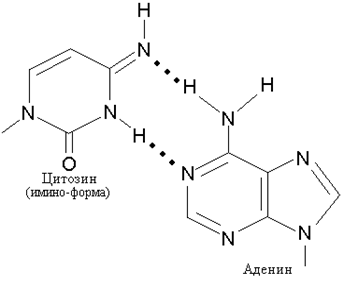
В 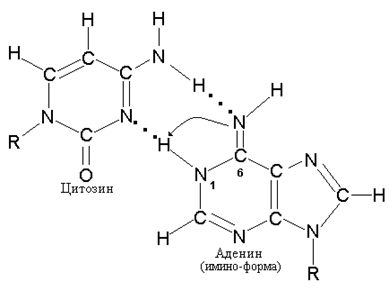
Рис. 12.4. Образование неканонических пар с участием иминоформы цитозина и аденина (А) и иминоформы аденина с нормальным цитозином (В)
Как известно, точность копирования в процессе репликации ДНК настолько велика, что в среднем на каждые 1·109 пар нуклеотидов приходится всего одна ошибка. Такую высокую точность репликации обеспечивает корректирующая (3/®5/)-экзонуклеазная активность ДНК-полимеразы. Тем не менее в ряде случаев ДНК-полимераза может ошибаться. Как раз одной из причин таких ошибок является способность всех азотистых оснований образовывать термодинамически невыгодные таутомерные формы за счет миграции атома водорода. При этом, как указывалось выше, амино- и оксогруппы превращаются в имино- и енольные группы соответственно. Такие редкие таутомерные формы, как правило, образуют неправильные, неканонические пары с другими основаниями. Примеры такого спаривания показаны на рис. 12.4.
Так, иминоформа Cyt образует пару не с Gua, а с Ade. В результате в процессе последующей репликации может произойти замена пары A-T на G-C. Точно так же Ade способен образовывать редкую таутомерную иминоформу, которая приобретает способность комплементарно спариваться с неканоническим для него Cyt.
В норме образование пар между двумя пуринами, а между двумя пиримидинами или некомплементарными основаниями A-C или G-T стерически затруднено, поскольку при этом не могут образовываться подходящие водородные связи и, следовательно, нарушается геометрия спирали. Модифицированные пурины и пиримидины, с небольшой частотой встречающиеся в ДНК, образуют такие же водородные связи, что и их немодифицированные аналоги. В этом случае правила спаривания не нарушаются.
|
|
|
Растворимость
При значениях рН, близких к нейтральным, наименьшей растворимостью в водной среде обладает гуанин. Следующим в этом ряду стоит ксантин. Мочевая кислота в форме уратов сравнительно неплохо растворяется при нейтральном рН, но очень плохо растворима в жидкостях с более низкими значениями рН, например в моче. Гуанин в моче человека в норме отсутствует, а ксантин и мочевая кислота являются ее обычными компонентами. Последние два пурина часто входят в состав камней мочевого тракта.
Нуклеозиды и нуклеотиды
Свободные основания значительно менее распространены в природе, чем соответствующие нуклеозиды и нуклеотиды. Молекулы нуклеозидов построены из пуринового или пиримидинового основания, к которому b-N-гликозидной связью присоединен углевод
(D-рибоза или 2/-дезокси-D-рибоза) по N9 или N1-положению соответственно.
Таким образом, адениновый рибонуклеозид (аденозин, Ado) состоит из аденина и D-рибозы, присоединенной по N9 атому пуринового цикла; гуанозин (Guo) – из гуанина и D-рибозы также в положении N9 пуринового цикла; цитидин (Cyd) состоит из цитозина и рибозы, присоединенной по N1 атому пиримидинового цикла, а уридин (Urd) построен из урацила и рибозы в положении N1 пиримидина (рис. 12.5).
Пуриновый нуклеозид Пиримидиновый нуклеозид


Рис. 12.5. Структурные формулы пуринового (аденозина) и пиримидинового (уридина) нуклеозидов. Природные нуклеозиды являются β‑аномерами, в которых азотистые основания присоединяются к углеводам β-N-гликозидными связями, причем в образовании этой связи принимают участие N9 атом пурина или N1 атом пиримидина и в любом случае С1 атом D-рибозы или 2/-дезокси-D-рибозы
В состав 2/-дезоксирибонуклеозидов входят пуриновые или пиримидиновые основания и 2/-дезоксирибоза, присоединенная по тем же атомам N9 и N1 в пуринах и пиримидинах соответственно. В целом присоединение рибозы или 2/-дезоксирибозы к кольцевой структуре основания происходит за счет относительно кислотолабильной N‑гликозидной связи.
|
|
|
Нуклеотиды – это производные нуклеозидов, фосфорилированные по одной или более гидроксильным группам углеводного остатка (D-рибозы или 2/-дезоксирибозы). Так, аденозинмонофосфат (АМР или адениловая кислота) построен из аденина, рибозы и остатка фосфорной кислоты. 2/-дезоксиаденозинмонофосфат (dАМР или дезоксиадениловая кислота) представляет собой молекулу, состоящую из аденина, 2/-дезоксирибозы и остатка фосфорной кислоты. Обычно к урацилу присоединена рибоза, а к тимину – 2/-дезоксирибоза. Таким образом, тимидиловая кислота (ТМР) состоит из тимина, 2/‑дезоксирибозы и фосфата, а в состав уридиловой кислоты (UМР) входят урацил, рибоза и фосфат.
Молекулы ДНК представляют собой полимеры тимидиловой, 2/‑дезоксицитидиловой, 2/-дезоксиадениловой и 2/-дезоксигуаниловой кислот. В то же время РНК образуется в результате сополимеризации уридиловой, цитидиловой, адениловой и гуаниловой кислот.
Номенклатура нуклеозидов и нуклеотидов
Таблица 12.1
Номенклатура нуклеозидов и нуклеотидов рибо-ряда
| Азотистое основание | Нуклеозид | Нуклеотиды |
| Аденин (Ade) | Аденозин (Ado) | Аденозинмонофосфат (AMP) Аденозиндифосфат (ADP) Аденозинтрифосфат (ATP) |
| Гуанин (Gue) | Гуанозин (Guo) | Гуанозинмонофосфат (GMP) Гуанозиндифосфат (GDP) Гуанозинтрифосфат (GTP) |
| Цитозин (Cyt) | Цитидин (Cyd) | Цитидинмонофосфат (CMP) Цитидиндифосфат (CDP) Цитидинтрифосфат (CTP) |
| Урацил (Ura) | Уридин (Urd) | Уридинмонофосфат (UMP) Уридиндифосфат (UDP) Уридинтрифосфат (UTP) |
Положение фосфатной группы в молекуле нуклеотида указывается цифрой. Например, аденозин с фосфатной группой, присоединенной сложноэфирной связью к 3-му атому углерода рибозы, обозначается как 3/-монофосфат. Штрих после цифры ставят для того, чтобы отличать номер углерода в пуриновом или пиримидиновом основании от положения атома углерода в углеводном остатке. При нумерации атомов углерода в азотистых основаниях штрих не ставится. Нуклеотид, состоящий из 2/-дезоксиаденозина (dAdo) с фосфатным остатком по С5 атому, в молекуле сахара обозначается как 2/‑дезоксиаденозин-5/-монофосфат.
|
|
|

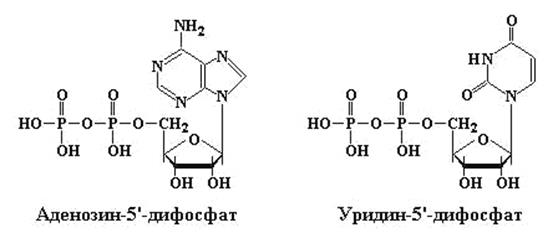
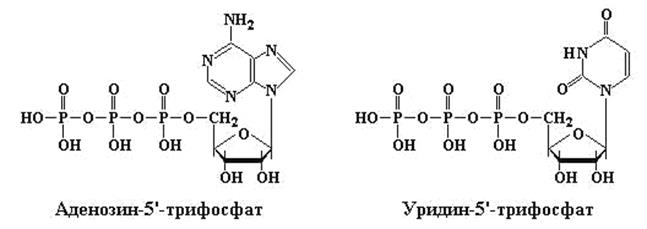
Рис. 12.6. Структурные формулы моно-, ди-, и трифосфатов аденозина и уридина
Нуклеозиды, содержащие аденин, гуанин, цитозин, тимин и урацил, принято обозначать буквами A, G, C, T, U или общепринятыми аббревиатурами Ado (dAdo), Guo (dGuo), Cyd (dCyd), Thd, Urd соответственно.
В таблице 12.1 приведены примеры только рибонуклеотидов и рибонуклеозидов. Наличие буквы d перед соответствующим сокращением означает, что углеводным компонентом такого нуклеозида является 2/-дезоксирибоза. Например, гуанозин, содержащий 2/-дезоксирибозу, может быть обозначен dG (dGuo, дезоксигуанозин), а соответствующий ему монофосфат с фосфатной группой, присоединенный к третьему атому углерода дезоксирибозы, – 2/‑дезоксигуанозин-5/‑монофосфат (dGuo-3/-MP). Часто в тех случаях, когда фосфат присоединен к С5 атому рибозы или 2/-дезоксирибозы, символ 5/ опускается. Так, гуанозин 5/-монофосфат принято обозначать GMP, а 5/‑монофосфат дезоксигуанозина сокращают как dGMP. Если к углеводному остатку нуклеозида присоединены 2 или 3 остатка фосфорной кислоты, используются аббревиатуры DP (дифосфат) и TP (трифосфат). Таким образом, аденозин с тремя фосфатными группами в 5/-положении углевода будет обозначаться как АТР. Примеры моно-, ди-, и трифосфатов Ado и Urd приведены на рис. 12.6.
Структура и информационные свойства
нуклеиновых кислот
Структура дезоксирибонуклеиновой кислоты (ДНК)
К числу важнейших научных событий второй половины ХХ в. следует отнести открытие того факта, что генетическая информация кодируется полимерной молекулой ДНК, образованной лишь четырьмя типами мономерных единиц. Именно ДНК служит химической основой наследственности. Молекула ДНК содержит в своей структуре множество генов. Гены функционируют не автономно: их репликация и транскрипция строго контролируются по принципу обратной связи, в которой ключевую роль играют продукты экспрессии. Знание структуры и функции нуклеиновых кислот необходимо для понимания сути генетических процессов, происходящих в клетке.
При рассмотрении структуры ДНК принято различать четыре уровня организации этой макромолекулы: первичную, вторичную, третичную и четвертичную структуры. Под первичной структурой ДНК (как и любой другой нуклеиновой кислоты) понимают последовательность расположения нуклеотидов в полинуклеотидных цепях.
Вторичная структура, согласно модели Уотсона и Крика, предложенной в 1953 г., – это двойная спираль ДНК, состоящая из двух правозакрученных вокруг общей оси полинуклеотидных цепей. Уотсон и Крик предположили, что две полинуклеотидные цепи в молекуле ДНК не связаны ковалентно, а соединяются водородными связями, возникающими между азотистыми основаниями, направленными внутрь двойной спирали. Реакции взаимодействия G с C и A с T получили название спаривания оснований, а основания, способные образовывать пары, получили название комплементарных.
|
|
|
Согласно модели двойной спирали две полинуклеотидные цепи в молекуле ДНК – антипараллельны, т.е. идут в противоположных направлениях. Поэтому, рассматривая спираль вдоль оси, можно видеть, что одна цепь идет в направлении 5/®3/, а другая – в направлении 3/ ® 5/ (рис. 12.7).
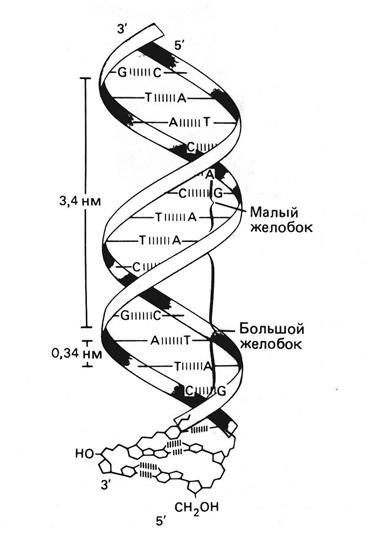
Рис. 12.7. Модель двойной спирали ДНК
Вдоль спирали основания уложены стопками друг на друга, и стабилизация спиральной структуры дополнительно обеспечивается межплоскостными взаимодействиями между ароматическими кольцами соседних оснований. Эти специфические контакты получили название стэкинг-взаимодействий, которые являются результатом реализации вандерваальсовых сил, возникающих за счет перекрывания p-облаков над и под двойными связями ненасыщенных колец пуринов и пиримидинов, с одной стороны, и гидрофобных взаимодействий – с другой.
Две соседние пары оснований в молекуле ДНК, расположенные вдоль оси спирали, образуют угол в 36°. Таким образом, 10 пар оснований составляют один полный оборот спирали в 360°. Две цепи, образующие двойную спираль, уложены таким способом, что наблюдаемая структура характеризуется наличием малой бороздки, шириной 12Å (1,2 нм), и большой бороздки, шириной 22Å (2,2 нм). Двойная спираль правосторонняя: если смотреть вдоль оси спирали – повороты следуют по часовой стрелке. Данное описание соответствует модели ДНК, известной как B-форма.
ДНК может формировать несколько типов двойных спиралей. В настоящее время описано, по крайней мере, шесть форм (от А до Е и Z-форма). Большая часть структурных вариантов ДНК может существовать только в строго контролируемых условиях. Эти варианты различаются: 1) числом пар оснований, приходящихся на один виток двойной спирали; 2) расстоянием между плоскостями пар оснований и углом, который они образуют с осью спирали; 3) диаметром спирали; 4) направленностью (правая, левая) двойной спирали.
При физиологических условиях (низкая концентрация соли, высокая степень гидратации) доминирующим структурным типом ДНК является В-форма (правоспирализованная). Шаг спирали такой молекулы равен 34 Å (3,4 нм). На один виток ДНК приходится 10 пар оснований, удерживаемых водородными связями и стэкинг-взаимодействиями.
А-форма отличается от В-формы тем, что плоскости оснований составляют с перпендикуляром к оси спирали угол, равный 20°. Поэтому расстояние между парами оснований по вертикали уменьшается до 2,9 Å (0,29 нм), а число пар на виток увеличивается до 11–12. А‑форма интересна еще и тем, что ее конформация близка к структуре гибридов ДНК-РНК и структуре двухспиральных РНК.
Z-форма представляет собой наиболее резкий контраст с классическими формами ДНК. Особенностью В- и А-форм ДНК является то, что сахарофосфатные остовы обеих цепей этих ДНК образуют правую спираль. При определенных условиях отдельные участки ДНК принимают форму левой спирали. В этом случае расстояние между соседними парами оснований увеличивается до 7,7 Å (0,77 нм), а число пар на один виток возрастает до 12. Свое название Z-форма получила из-за зигзагообразной (zigzag) линии, которую образует сахарофосфатный остов вдоль спирали.
Двухцепочечные кольцевые молекулы ДНК, за крайне редким исключением, обладают уникальными топологическими характеристиками. Кольцевые молекулы имеют в структуре соответствующие изгибы и петли, которые получили название супервитков и которые хорошо различимы при использовании электронной микроскопии (рис. 12.8).

Рис. 12.8. Электронные микрофотографии суперспирализованных молекул ДНК: А – суперспирализованная митохондриальная ДНК;
В – релаксированная форма митохондриальной ДНК; С – двухцепочечная кольцевая ДНК фага М13 с разной степенью сверхспиральности. На последней микрофотографии цифрами указано число супервитков в каждой молекуле
Если двойную спираль повернуть на один или несколько полных оборотов в направлении ее раскручивания, то в результате получим напряженную структуру. Такая напряженная структура, которая характеризуется недостатком оборотов, получила название отрицательносуперспирализованной ДНК. Возникшие отрицательные супервитки закручивают ДНК против часовой стрелки, т.е. в направлении, противоположном ходу обычной правосторонней двойной спирали. Такую спираль называют недокрученной. Напряжение, возникающее вследствие дефицита витков, может быть компенсировано либо разрушением водородных связей между комплементарными парами оснований и раскрытием двойной спирали на небольшом участке макромолекулы, либо путем сворачивания в направлении, противоположном тому, в котором она была повернута. Таким образом, напряжение вращения, которое было внесено в молекулу, может быть смягчено за счет образования третичной структуры с хорошо различимыми супервитками (см. рис. 12.8).
Наконец, под четвертичной структурой ДНК понимают образование нуклеопротеидных комплексов (нуклеосом – комплексов гистонов с ДНК у эукариот или комплексов гистоноподобных белков с ДНК у прокариот), которые принимают участие в компактизации ДНК с образованием хромосом (у эукариот) или нуклеоидов (у прокариот).
Структура рибонуклеиновых кислот (РНК)
РНК представляет собой сополимер пуриновых и пиримидиновых рибонуклеотидов, соединенных друг с другом, как и в ДНК, 3/,5/‑фосфодиэфирными мостиками. По ряду признаков ДНК и РНК отличаются друг от друга. У РНК углеводным остатком, к которому присоединены пуриновые или пиримидиновые основания и фосфатные группы, является рибоза, а не 2/-дезоксирибоза (как у ДНК). Пиримидиновые компоненты РНК отличаются от таковых у ДНК. РНК не содержит тимина, а его место в молекуле РНК занимает урацил. РНК – одноцепочечная молекула, которая способна сворачиваться с образованием «шпилек» – особых структур, имеющих двухспиральные характеристики.
При описании строения рибонуклеиновых кислот, как правило, упоминают три вида молекул РНК: информационные (иРНК), рибосомальные (рРНК) и транспортные РНК (тРНК). Информационные РНК выполняют функцию молекул-посредников и служат переносчиками информации от гена к белок-синтезирующей системе клетки. Они выполняют роль матриц для синтезируемого полипептида, т.е. определяют аминокислотную последовательность белка. Рибосомные РНК выполняют роль структурных компонентов рибосом, которые обеспечивают специфический контакт иРНК и тРНК, в результате которого происходит трансляция нуклеотидной последовательности, считанной с определенного гена, в аминокислотную последовательность соответствующего белка. Транспортные РНК – это адапторные молекулы, участвующие в трансляции информации иРНК в последовательность аминокислот в белках.
Кроме упомянутых трех видов РНК, в настоящее время открыты и интенсивно изучаются так называемые малые ядерные РНК (мяРНК), обозначаемые U1, U2, U4, U5 и U6, которые принимают участие в формировании сплайсисом – организованных структур обеспечивающих сплайсинг иРНК эукариот. Более того, в 2000 г. был открыт неизвестный ранее вид двухцепочечных молекул РНК, которые получили название малых интерферирующих РНК (миРНК), принимающих участие в защите эукариотических клеток от вирусных инфекций.
Химические свойства нуклеиновых кислот
Качественные реакции на компоненты
нуклеопротеинов
Обнаружение полипептидов. Для этого в составе нуклеопротеидов используют биуретовую реакцию. В щелочной среде белки, а также продукты их гидролиза – полипептиды – дают фиолетовое окрашивание с солями меди. Положительная биуретовая реакция проявляется у соединений, содержащих не менее двух пептидных групп (т.е. у трипептидов, тетрапептидов и т.д.). Интенсивность окраски зависит от длины пептида и варьирует от сине-фиолетовой до красно-фиолетовой и красной. Биуретовый медный комплекс имеет следующее строение:
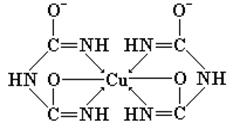
Аналогично построено комплексное соединение меди с енолизированными пептидными группами любого другого полипептида:
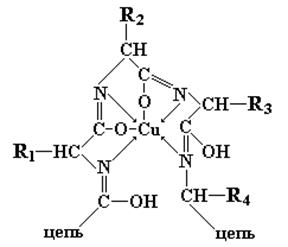
Обнаружение пуриновых оснований. При добавлении аммиачного раствора оксида серебра выпадает небольшой хлопьевидный осадок серебряных соединений пуриновых оснований. Данная реакция может быть применена при синтезе нуклеозидов.
Обнаружение пентоз. При нагревании с концентрированными серной или соляной кислотами пентозы теряют три молекулы воды и превращаются в фурфурол. Последний способен конденсироваться с анилином, тимолом или орцином (в присутствии хлорида железа III) с образованием характерных продуктов вишнево-красного, красного и зеленого цвета соответственно.
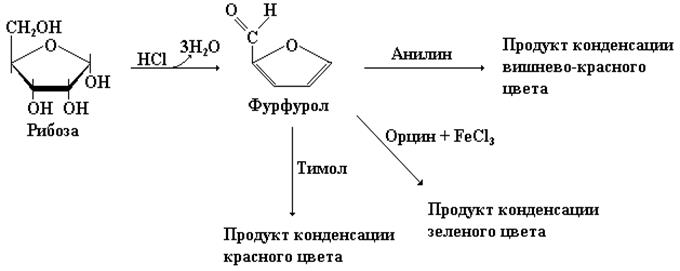
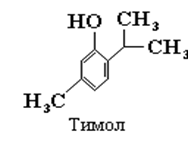
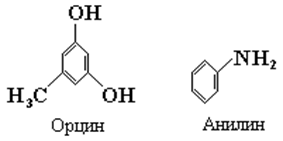
Обнаружение фосфорной кислоты в образце можно осуществить с использованием молибдата аммония. Фосфорная кислота образует с молибденовым реактивом желтый кристаллический осадок фосфорномолибденовокислого аммония:
H3PO4 + 12 (NH4)2MoO4 + 21 HNO3 →
(NH4)3PO4 × 12 MoO3 + 21 NH4NO3 + 12 H2O.
Количественное определение нуклеиновых кислот
Орциновый метод определения РНК. Рибоза, входящая в состав РНК, при взаимодействии с сильными неорганическими кислотами (в частности с HCl) образует фурфурол, который конденсируется с орцином в присутствии следов хлорида железа III. В результате образуется соединение синего цвета, интенсивность окраски которого пропорциональна концентрации РНК в растворе.
Дифениламиновый метод определения ДНК. Дезоксирибоза, входящая в состав ДНК, при нагревании с кислотой в мягких условиях образует фурфуриловый спирт, который конденсируется с дифениламином, образуя соединение синего цвета. Интенсивность окраски полученного раствора пропорциональна концентрации ДНК в растворе.

Контрольные вопросы
1. История исследования структуры нуклеиновых кислот.
2. Строение пуриновых и пиримидиновых азотистых оснований.
3. Физико-химические свойства пуриновых и пиримидиновых азотистых оснований.
4. Принципы образования канонических пар азотистых оснований в нуклеиновых кислотах.
5. Строение нуклеозидов. Характеристика моносахаридов, входящих в состав нуклеозидов.
6. Строение и роль нуклеотидов.
7. Основные принципы структурной организации дезоксирибонуклеиновых кислот.
8. Информационные свойства ДНК.
9. Структура рибонуклеиновых кислот.
10. Химические свойства нуклеиновых кислот. Качественные реакции на обнаружение компонентов нуклеопротеинов.
11. Сущность методов количественного определения ДНК и РНК.
Литература
1. Страйер Л. Биохимия, т. 1, 2, 3. – М.: Мир, 1985.
2. Овчинников Ю.А. Биоорганическая химия. – М.: Просвещение, 1987.
3. Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия человека, т. 1, 2. – М.: Мир, 1993.
4. Горячковский А.М. Справочное пособие по клинической биохимии. – Одесса: ОКФА, 1994.
5. Евстигнеева Р.П., Серебренникова Г.А., Звонкова Е.Н., Филиппович Е.И., Митрофанова Т.К., Мягкова Г.И., Скляр Ю.Е. Химия биологически активных природных соединений / Под ред. Преображенского Н.А. – М.: Химия, 1976.
6. Кнорре Д.Г., Мызина С.Д. Биологическая химия. – М.: Высшая школа, 1998.
7. Кольман Я., Рем К.-Г. Наглядная биохимия. – М.: Мир, 2000.
8. Зайчик А.Щ., Чурилов Л.П. Основы патохимии. – СПб.: ЭЛБИ-СПб, 2000.
9. Чиркин А.А. Практикум по биохимии. – Мн.: Новое знание, 2002.
Ход работы
Тема: Выделение нуклеопротеидов
w Выделение нуклеопротеидов из дрожжей
1. 5 г дрожжей увлажняют в ступке добавлением 1 мл эфира и 1 мл воды.
2. Добавляют немного песка и растирают с 0,4%-ным раствором NaOH, приливая его небольшими порциями по 5–10 мл (всего расходуют 50 мл раствора щелочи). Растирание продолжают в течение 15-20 мин.
3. Содержимое ступки центрифугируют 10 мин. при 2500 об/мин.
4. Супернатант переливают в стакан и к нему по каплям добавляют 5%-ный раствор уксусной кислоты до полного осаждения нуклеопротеида (обычно расходуют 10–15 мл раствора).
5. Осадок отделяют центрифугированием (8000g в течение 5 мин.).
6. Проводят гидролиз нуклеопротеидов кипячением с разбавленной серной кислотой. Для этого:
Ÿ Осадок нуклеопротеидов переносят в круглодонную колбу, смывая его 5%‑ной серной кислотой. Остаток кислоты вливают в колбу с осадком (всего расходуют не более 25 мл раствора).
Ÿ Колбу закрывают пробкой с обратным холодильником, ставят на асбестовую сетку, нагревают на малом огне до кипения и кипятят 1 ч.
Ÿ После этого колбу охлаждают и гидролизат фильтруют через бумажный фильтр.
Тема: Качественные реакции на присутствие нуклеопротеидов в растворе
КАЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ КОМПОНЕНТОВ НУКЛЕОПРОТЕИНОВ
w Открытие полипептидов
1. В одну пробирку наливают 2 мл фильтрата, а в другую – столько же дистиллированной воды.
2. Затем в каждую из них прибавляют 2 мл 10-ного раствора NaOH, хорошо перемешивают и добавляют 2–3 капли 2%-ного раствора CuSO4.
3. Пробирки встряхивают, полученные результаты описывают и делают выводы.
w Открытие пуриновых оснований
1. К 2 мл фильтрата добавляют концентрированный раствор аммиака до щелочной реакции на лакмус. Затем приливают 1 мл аммиачного раствора окиси серебра.
2. Через несколько минут наблюдают выпадение хлопьев осадка серебряных солей пуриновых оснований. Объясняют получаемые результаты и делают выводы.
w Открытие пентоз
1. К 1 мл фильтрата добавляют 2–3 капли 1%-ного спиртового раствора тимола.
2. Затем по стенке осторожно наслаивают 1 мл концентрированной серной кислоты.
3. Объясняют получаемые результаты и делают выводы.
w Открытие фосфорной кислоты
1. К 1 мл фильтрата добавляют равный объем молибденового
реактива.
2. Нагревают до кипения и кипятят 2–3 мин.
3. Наблюдают появление желтого окрашивания. При стоянии выпадает желтый осадок.
4. Объясняют получаемые результаты и делают выводы.
Тема: Количественное определение нуклеиновых кислот
w Орциновый метод количественного определения РНК
1. Непосредственно перед использованием смешивают 5 мл раствора А, 20 мл раствора Б и 0,5 мл раствора В.
2. К 0,5 мл фильтрата и стандартного раствора добавляют по 3 мл полученного реактива.
3. Пробы нагревают на кипящей водяной бане в течение 25 мин., затем охлаждают.
4. Измеряют оптическую плотность растворов при 660 нм относительно чистого реагента.
5. Рассчитывают концентрацию РНК в исследуемой пробе, используя
формулу
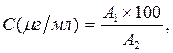
где А1 – поглощение исследуемой пробы;
А2 – поглощение стандартной пробы;
100 (mг/мл) – концентрация стандартного раствора РНК.
6. Объясняют получаемые результаты и делают выводы.
w Дифениламиновый метод определения ДНК
1. Аналитические пробы готовят в соответствии с таблицей:
| Опытная проба | Стандартная проба | Холостая проба | |
| Фильтрат, мл | 1,55 | – | – |
| Станд. раствор, мл | – | 1,55 | – |
| Дист. вода, мл | – | – | 1,55 |
| HClO4(конц.), мл | 0,05 | 0,05 | 0,05 |
| Дифениламиновый реагент, мл | 3,20 | 3,20 | 3,20 |
2. Пробы инкубируют в течение 30 мин при 40 °С.
3. Измеряют оптическую плотность опытной и стандартной проб при 660 нм относительно холостой пробы.
4. Рассчитывают концентрацию ДНК в опытной пробе, используя формулу

где А1 – поглощение опытной пробы;
А2 – поглощение стандартной пробы;
50 (mг/мл) –концентрация стандартного раствора ДНК.
5. Объясняют получаемые результаты и делают выводы.
Оформление работы
К занятию:
1. Кратко законспектировать теоретические данные по лабораторной работе.
Во время занятия:
2. Описать этапы работы.
3. Описать результаты.
4. Сделать выводы.
Приложение
Ряд наиболее важных длинноцепочечных жирных кислот
| Название | Состав | Формула |
| Насыщенные | ||
| Пальмитиновая | 16 атомов углерода | 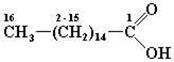
|
| Стеариновая | 18 атомов углерода | 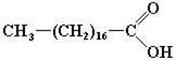
|
| Ненасыщенные | ||
| С одной двойной связью (моноеновые) | ||
| Пальмитолеи-новая | 16:1, 9*) | 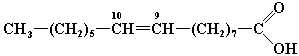
|
| Олеиновая | 18:1, 9 | 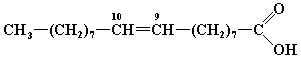
|
| С двумя двойными связями (диеновые) | ||
| Линолевая | 18:2, 9, 12 | 
|
| С тремя двойными связями (триеновые) | ||
| g-Линоленовая | 18:3, 6, 9, 12 | 
|
| a-Линоленовая | 18:3, 9, 12, 15 | 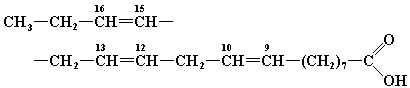
|
| С четырьмя двойными связями (тетраеновые) | ||
| Арахидоновая | 20:4, 5, 8, 11, 14 | 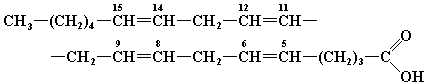
|
*) – 16:1, 9 – расшифровывается как – 16 атомов углерода: 1 двойная связь, двойная связь в 9-м положении.
Учебное издание
Авторы:
Бокуть Сергей Борисович,
Сяхович Виталий Эдуардович.
Практикум по общей и экологической биохимии
Часть IV
«Структура и функции липидов. Обмен липидов.
Нуклеиновые кислоты. Компоненты нуклеиновых кислот»
Учебно-методическое пособие
Редактор М.И. Авхимович
Корректор В.С. Мороз
Технический редактор М.Л. Шимкевич
Cдано в набор 11.11.2004. Подписано в печать 24.11.2004. Формат 60x84 1/16.
Гарнитура Times New Roman. Усл. печ. л. 4,19. Уч.-изд. л. 2,42. Тираж 50 экз.
Международный государственный экологический университет им. А.Д. Сахарова
ул. Долгобродская, 23, 220009, Минск, Республика Беларусь
|
|
|
|



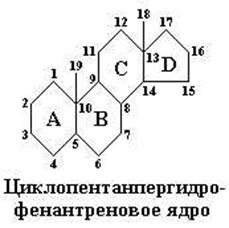 Рис. 10.3. Структура циклопентанпергидрофенантренового ядра стероидов. Показаны общепринятое обозначение колец и нумерация углеродных атомов стероидов
Рис. 10.3. Структура циклопентанпергидрофенантренового ядра стероидов. Показаны общепринятое обозначение колец и нумерация углеродных атомов стероидов